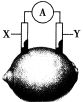
根据光合作用原理,设计如图原电池装置。下列说法正确的是


| A.a为正极,且发生还原反应 |
| B.b的电极反应式为:O2+2e-+2H+=H2O2 |
| C.电子流动的方向是b→导线→a |
| D.若a上生成22.4LO2,通过质子交换膜的H+为4mol |
更新时间:2021-01-31 19:22:16
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列实验装置或现象正确且能达到实验目的的是
| A | B | C | D |
 | 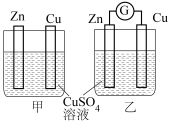 |  | 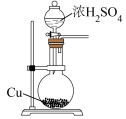 |
| 形成红色喷泉 | 甲中Zn片有红色固体析出,乙中铜片质量增加 | 制取得到干燥的NH3 | 制备SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】我国高铁技术全球领先。CRH380B型动车组使用是镍镉(Ni-Cd)可充电电池,它作为原电池时,发生的反应为:Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2。由此推断,该电池负极材料是
| A.Cd(OH)2 | B.Cd | C.Ni(OH)2 | D.NiO(OH) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】锌铜原电池装置如图所示,下列说法不正确的是
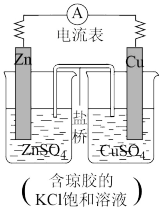

| A.电子从锌片流向铜片 |
| B.盐桥中 K+向负极移动 |
| C.锌电极上发生的反应:Zn − 2e- =Zn2+ |
| D.该装置实现了氧化反应和还原反应分开进行 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】碱性锌锰电池的总反应为:  。下列说法中正确的是
。下列说法中正确的是
 。下列说法中正确的是
。下列说法中正确的是A.锌为负极, 为正极 为正极 |
B.工作时 没有发挥作用 没有发挥作用 |
C.工作时电子由 经外电路流向 经外电路流向 。锌发生还原反应, 。锌发生还原反应, 发生氧化反应 发生氧化反应 |
D.锌发生还原反应, 发生氧化反应 发生氧化反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】有关下列装置的说法确的


| A.I、Ⅱ均构成原电池 |
| B.I、Ⅱ均产生气泡,且气泡均在Zn片表面 |
| C.一段时间后,I、Ⅱ的酸性均减弱,pH均增大 |
| D.如果I、Ⅱ中的稀硫酸浓度相同,则Zn片的溶解速率相同 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】为体现节能减排的理念,中国研制出了新型燃料电池汽车,该车装有“绿色心脏”——质子(H+)交换膜燃料电池。如图所示为某种质子交换膜燃料电池原理示意图,关于该电池的说法正确的是( )


| A.该电池的正极是b极 |
| B.写出该电池的正极反应式为H2-2e-=2H+ |
| C.H+通过质子交换膜从右向左移动 |
| D.OH-通过质子交换膜从右向左移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】我国科研团队借助氧化还原介质 ,将某锂离子电池的放电电压提高至
,将某锂离子电池的放电电压提高至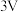 以上,该电池的工作原理如图所示。下列说法正确的是
以上,该电池的工作原理如图所示。下列说法正确的是

 ,将某锂离子电池的放电电压提高至
,将某锂离子电池的放电电压提高至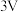 以上,该电池的工作原理如图所示。下列说法正确的是
以上,该电池的工作原理如图所示。下列说法正确的是
| A.多孔碳电极上发生氧化反应 |
B.负极反应: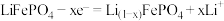 |
C. 电极每减重 电极每减重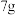 ,就有 ,就有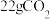 被固定 被固定 |
D.电子会在 介质内通过 介质内通过 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
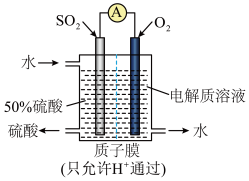

| A.通入SO2气体的一极是负极,发生还原反应 |
| B.正极的电极反应:O2+4e−=2O2− |
| C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4 |
| D.氢离子向负极区移动,与负极生成的SO42−结合形成硫酸 |
您最近一年使用:0次