(1)厨房中的调味品,①盐(主要成分氯化钠)、②碱面(主要成分碳酸钠)、③白醋(主要成分乙酸)。主要成分中属于盐类的是___________ (填序号,下同);相互间能发生反应的是___________ 。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是___________ 。
(3)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因___________ 。
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式___________ ,若生成6.72L气体(标准状况),则消耗铝的质量为___________ g。
(2)食盐不慎洒落在天然气的火焰上,观察的现象是
(3)FeSO4•7H2O俗称绿矾,在医药工业中可用于补铁剂的制造,而硫酸亚铁溶液在保存时需要加入适量的铁粉,请用离子方程式简述其原因
(4)铝合金具有广泛的用途,但铝制器具不宜盛放碱性食物,其请写出该反应的离子方程式
更新时间:2021-02-09 12:32:09
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有下列13种物质:①Fe;②CO2;③空气;④CaO;⑤HNO3;⑥Ca(OH)2;⑦碘酒;⑧CuSO4·5H2O;⑨乙醇;⑩NaHCO3;⑪Fe(OH)3胶体;⑫合金;⑬盐酸
(1)属于混合物的是__________ ((填序号,下同));
(2)属于氧化物的是__________ ;
(3)属于酸的是__________ ;
(4)属于碱的是__________ ;
(5)属于盐的是_______ ;
(6)可出现丁达尔效应的是_____ ;
(7)属于电解质的是______ ;属于非电解质的______ 。
(1)属于混合物的是
(2)属于氧化物的是
(3)属于酸的是
(4)属于碱的是
(5)属于盐的是
(6)可出现丁达尔效应的是
(7)属于电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】物质的分类有多种方法,下列对无机化合物分类如图:

(1)如图所示的物质分类方法的名称是________ 。
(2)以元素 Na、Ba、H、O、S、N 中任意两种或三种元素组成合适的物质,将化学式分别填在下表中④、⑥的后面________ 、__________
(3)⑦和⑧的水溶液可导电,它们________ (填“是”或“不是”)电解质;相同质量的两气体所含氧原子的个数比为________ ;标准状况下等体积两气体的质量比为________ 。
(4)少量⑧与足量④的溶液反应的离子方程式为________ 。
(5)写出⑦与⑨反应的化学方程式________ 。
(6)写出工业制造硝酸过程中⑩NH3 与氧气反应的化学方程式为________ ,若 16g 氧气全部被还原,则转移电子________ mol。
(7)现有由①与②混合的稀溶液 100mL,其中①的物质的量浓度为 2.0mol·L-1,②的物质的量浓度为 1.0mol·L-1。则该溶液能溶解铜的最大质量为________ g,同时,反应生成的气体在标准状况下的体积为________ L。

(1)如图所示的物质分类方法的名称是
(2)以元素 Na、Ba、H、O、S、N 中任意两种或三种元素组成合适的物质,将化学式分别填在下表中④、⑥的后面
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①H2SO4 ②HNO3 | ③NH3· H2O ④ | ⑤NaNO₃ ⑥ | ⑦CO2 ⑧SO2 ⑨Na2O2 | ⑩NH3 |
(4)少量⑧与足量④的溶液反应的离子方程式为
(5)写出⑦与⑨反应的化学方程式
(6)写出工业制造硝酸过程中⑩NH3 与氧气反应的化学方程式为
(7)现有由①与②混合的稀溶液 100mL,其中①的物质的量浓度为 2.0mol·L-1,②的物质的量浓度为 1.0mol·L-1。则该溶液能溶解铜的最大质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】分类是根据研究对象的共同点和差异点,将它们区分不同种类和层次的科学方法。运用分类的方法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。下图是对化学反应类型进行的分类。

①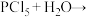 ___________
___________
②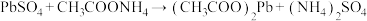
③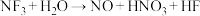
④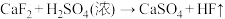
⑤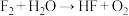
⑥
⑦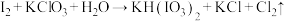
根据上面的化学反应(未配平)完成下列问题:
(1)图中分类方式为___________ 。
A.树状分类法 B.交叉分类法
(2)①反应属于非氧化还原反应,生成一种强酸和→种弱酸,弱酸的化学式为___________ 。
(3)②反应属于复分解反应且 可溶于水,由此推断
可溶于水,由此推断 属于
属于___________ (填“强电解质”或“弱电解质”)。
(4)反应③④⑤均生成 ,属于氧化还原反应的是
,属于氧化还原反应的是___________ (填序号)。
(5)将反应⑥和⑦配平:
⑥___________ ;
⑦___________ 。

①
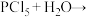 ___________
___________②
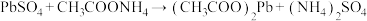
③
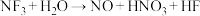
④
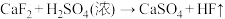
⑤
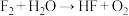
⑥

⑦
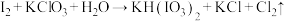
根据上面的化学反应(未配平)完成下列问题:
(1)图中分类方式为
A.树状分类法 B.交叉分类法
(2)①反应属于非氧化还原反应,生成一种强酸和→种弱酸,弱酸的化学式为
(3)②反应属于复分解反应且
 可溶于水,由此推断
可溶于水,由此推断 属于
属于(4)反应③④⑤均生成
 ,属于氧化还原反应的是
,属于氧化还原反应的是(5)将反应⑥和⑦配平:
⑥
⑦
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】央视《每周质量报告》曝光了少数明胶企业将皮革废料熬制成工业明胶,出售给个别制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。2010版《中国药典》明确规定,药用胶囊使用的明胶原料,重金属铬的含量均不得超过2mg•kg-1。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为___ ;如果某明胶原料100kg中含有铁元素的质量为0.56g,则药用胶囊使用的这种明胶原料重金属铬的含量___ (填“超标”或“不超标”)。
(2)区别明胶溶于水的分散系和Na2SO4溶液的方法是___ 。
(3)将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是___ 。
A.冷水 B.沸水 C.NaCl溶液 D.NaOH溶液
(4)已知胶体的分散质不能透过半透膜,但小分子或离子能透过半透膜。现将10mL明胶溶于水的分散系与5mLNa2SO4溶液混合后装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中。写出证明Na+能透过半透膜的实验方法(具体操作):___ 。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为
(2)区别明胶溶于水的分散系和Na2SO4溶液的方法是
(3)将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是
A.冷水 B.沸水 C.NaCl溶液 D.NaOH溶液
(4)已知胶体的分散质不能透过半透膜,但小分子或离子能透过半透膜。现将10mL明胶溶于水的分散系与5mLNa2SO4溶液混合后装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中。写出证明Na+能透过半透膜的实验方法(具体操作):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有以下几种物质:①液氧②硝酸钾溶液③ ④干冰⑤
④干冰⑤ ⑥熔融的
⑥熔融的 ⑦纯碱⑧
⑦纯碱⑧ ⑨
⑨ ⑩澄清石灰水
⑩澄清石灰水
(1)属于电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)将⑧慢慢滴入⑦的溶液的现象为:___________ 。
(3)少量⑥的与⑩混合的离子反应:___________ 。
(4)⑨在熔融状态下的电离方程式___________ 。
(5)如何鉴别②的阳离子(写出具体操作、现象、结论):___________ 。
 ④干冰⑤
④干冰⑤ ⑥熔融的
⑥熔融的 ⑦纯碱⑧
⑦纯碱⑧ ⑨
⑨ ⑩澄清石灰水
⑩澄清石灰水(1)属于电解质的是
(2)将⑧慢慢滴入⑦的溶液的现象为:
(3)少量⑥的与⑩混合的离子反应:
(4)⑨在熔融状态下的电离方程式
(5)如何鉴别②的阳离子(写出具体操作、现象、结论):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为化学“五元环”图案,在图案上分别写了 、Na、
、Na、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
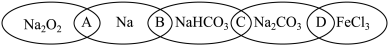
(1)分类依据A、B、C、D中可总结为“两种物质都是电解质”的是___________ (填代号)。
(2)写出除去 溶液中
溶液中 杂质的离子方程式:
杂质的离子方程式:___________ 。
(3)潜水艇和消防员的呼吸面具中, 所发生的主要反应的化学方程式为:
所发生的主要反应的化学方程式为:___________ 。
(4)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和 溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验名称是
溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验名称是___________ ,制备胶体的离子方程式为___________ 。
(5)用洁净的铂丝蘸取 溶液置于酒精灯火焰上灼烧,火焰呈
溶液置于酒精灯火焰上灼烧,火焰呈___________ 色。
(6)等质量的 和
和 分别与足量的盐酸反应,在相同条件下产生
分别与足量的盐酸反应,在相同条件下产生 的体积
的体积
___________  (填“大于”,“小于”或“等于)
(填“大于”,“小于”或“等于)
 、Na、
、Na、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
(1)分类依据A、B、C、D中可总结为“两种物质都是电解质”的是
(2)写出除去
 溶液中
溶液中 杂质的离子方程式:
杂质的离子方程式:(3)潜水艇和消防员的呼吸面具中,
 所发生的主要反应的化学方程式为:
所发生的主要反应的化学方程式为:(4)在烧杯中加入20mL蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和
 溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验名称是
溶液,继续加热至呈红褐色后停止加热。证明有胶体生成的实验名称是(5)用洁净的铂丝蘸取
 溶液置于酒精灯火焰上灼烧,火焰呈
溶液置于酒精灯火焰上灼烧,火焰呈(6)等质量的
 和
和 分别与足量的盐酸反应,在相同条件下产生
分别与足量的盐酸反应,在相同条件下产生 的体积
的体积
 (填“大于”,“小于”或“等于)
(填“大于”,“小于”或“等于)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)鉴别KCl溶液和K2CO3的试剂是________ ,离子方程式为________ 。
(2)除去混入FeCl3溶液混有中少量FeCl2杂质的试剂是_______ ,离子方程式为__________
(3)除去镁粉末中混入的铝粉剂是_______ ,化学方程式为__________ 。
(2)除去混入FeCl3溶液混有中少量FeCl2杂质的试剂是
(3)除去镁粉末中混入的铝粉剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)某化学小组为测定一定质量的某镁铝混合物中镁、铝的质量分数,设计了如下实验方案:
取ag镁铝混合物 测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为
测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为___________ 。
(2)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液。现做如下实验:
①取440mL甲溶液与120mL乙溶液反应,产生1.56g沉淀。
②取120mL甲溶液与440mL乙溶液反应,产生1.56g沉淀。
③取120mL甲溶液与400mL乙溶液反应,产生3.12g沉淀。
通过必要的计算和推理判定:甲溶液为____________ 溶液,理由是:____________________________________ 甲溶液的物质的量浓度是多少?
___________________________
取ag镁铝混合物
 测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为
测定剩余固体的质量为bg当溶液B为NOH溶液时,铝的质量分数为(2)现有甲、乙两瓶无色溶液,已知它们可能是AlCl3溶液和NaOH溶液。现做如下实验:
①取440mL甲溶液与120mL乙溶液反应,产生1.56g沉淀。
②取120mL甲溶液与440mL乙溶液反应,产生1.56g沉淀。
③取120mL甲溶液与400mL乙溶液反应,产生3.12g沉淀。
通过必要的计算和推理判定:甲溶液为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】用地壳中硅元素生产的多种产品在现代高科技中占重要位置,足见化学对现代物质文明的重要作用.例如:
(1)光导纤维的主要成分是________
(2)目前应用最多的太阳能电池的光电转化材料是________
(3)赏心悦目的雕花玻璃是用一种物质对玻璃进行化学刻蚀而制成的,该反应的化学方程式为________
(4)工业上制取粗硅是用石英和焦炭在高温电炉中反应制得,该反应中氧化剂与还原剂的质量比为________ ;用石英和焦炭在高温电炉中反应也可以制得金刚砂(SiC),并产生CO气体,该反应中氧化剂和还原剂的物质的量之比为________
(5)将表面已氧化的铝箔放入氢氧化钠溶液中,反应的离子方程式分别是________ 、________
(6)用铝箔包裹0.1mol金属钠,用针扎若干小孔后,放入水中,完全反应后,用排水法收集到标准状况下气体的体积________ (填字母序号).
a.等于1.12L b.大于1.12L c.小于1.12L.
(1)光导纤维的主要成分是
(2)目前应用最多的太阳能电池的光电转化材料是
(3)赏心悦目的雕花玻璃是用一种物质对玻璃进行化学刻蚀而制成的,该反应的化学方程式为
(4)工业上制取粗硅是用石英和焦炭在高温电炉中反应制得,该反应中氧化剂与还原剂的质量比为
(5)将表面已氧化的铝箔放入氢氧化钠溶液中,反应的离子方程式分别是
(6)用铝箔包裹0.1mol金属钠,用针扎若干小孔后,放入水中,完全反应后,用排水法收集到标准状况下气体的体积
a.等于1.12L b.大于1.12L c.小于1.12L.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据铁元素化合物的知识:
(1)在配制含有Fe2+溶液时,常常需要向溶液中加入少量铁粉,其原因是____ ;反应的离子方程式为____ 。
(2)为除去废水中的Fe2+,常加____ 将废水中的Fe2+氧化,再调节pH使Fe3+转化为_____ 除去。
(1)在配制含有Fe2+溶液时,常常需要向溶液中加入少量铁粉,其原因是
(2)为除去废水中的Fe2+,常加
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某班同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
的溶液。在FeCl2溶液中需加入少量铁屑,其目的是___________ ;
(2)甲组同学在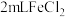 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,发生反应的离子方程式为
溶液,溶液变红,发生反应的离子方程式为___________ ;
(3)乙组同学向盛有H2O2溶液的试管和加入几滴酸化的 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为___________ ;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是___________ ;生成沉淀的原因是(用平衡移动原理解)___________ 。
(4)丙组同学模拟工业上用 和废液制备
和废液制备 溶液。
溶液。
①若酸性 废液中:
废液中: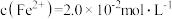 ,
,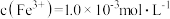 ,
,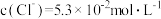 ,则该溶液的pH约为
,则该溶液的pH约为___________ 。
②完成 氧化
氧化 的离子方程式:
的离子方程式:____________
___________ +___________Fe2++___________→___________Cl-+___________
+___________Fe2++___________→___________Cl-+___________ +___________。
+___________。
③若该组同学在处理废水时消耗浓度为0.15 的
的 500mL,则该反应转移的电子数目为
500mL,则该反应转移的电子数目为___________ 。
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1
 的溶液。在FeCl2溶液中需加入少量铁屑,其目的是
的溶液。在FeCl2溶液中需加入少量铁屑,其目的是(2)甲组同学在
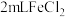 溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴
溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,发生反应的离子方程式为
溶液,溶液变红,发生反应的离子方程式为(3)乙组同学向盛有H2O2溶液的试管和加入几滴酸化的
 溶液,溶液变成棕黄色,发生反应的离子方程式为
溶液,溶液变成棕黄色,发生反应的离子方程式为(4)丙组同学模拟工业上用
 和废液制备
和废液制备 溶液。
溶液。①若酸性
 废液中:
废液中: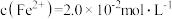 ,
,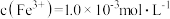 ,
,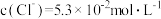 ,则该溶液的pH约为
,则该溶液的pH约为②完成
 氧化
氧化 的离子方程式:
的离子方程式:___________
 +___________Fe2++___________→___________Cl-+___________
+___________Fe2++___________→___________Cl-+___________ +___________。
+___________。③若该组同学在处理废水时消耗浓度为0.15
 的
的 500mL,则该反应转移的电子数目为
500mL,则该反应转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图是有关物质的转化图,有些反应物、生成物 已略去,它们之间的转化关系如下:
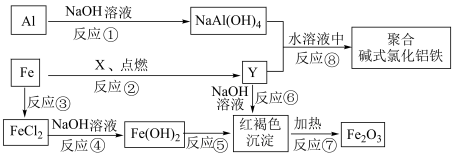
请填写有关空白。
(1) 的化学式是
的化学式是_______ ; 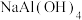 的名称是
的名称是_______ 。
(2)配制 溶液常常加入铁粉,原因是
溶液常常加入铁粉,原因是_______ 。
(3)在敞口容器中进行反应④,实验现象为_______ 。
(4)写出反应⑦的化学方程式:_______ 。
(5)写出下列反应的离子 方程式:
反应①的离子方程式为_______ ;
“聚合碱式氯化铝铁”的化学式为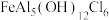 ,则反应③的离子方程式为
,则反应③的离子方程式为_______ 。

请填写有关空白。
(1)
 的化学式是
的化学式是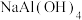 的名称是
的名称是(2)配制
 溶液常常加入铁粉,原因是
溶液常常加入铁粉,原因是(3)在敞口容器中进行反应④,实验现象为
(4)写出反应⑦的化学方程式:
(5)写出下列反应的
反应①的离子方程式为
“聚合碱式氯化铝铁”的化学式为
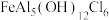 ,则反应③的离子方程式为
,则反应③的离子方程式为
您最近一年使用:0次



