写出下列物质在水溶液中的电离方程式。
Na2CO3:_______________________
CH3COOH:________________________ ;
NH4Cl:_________________________
H2SO4:__________________________ ;
H2CO3:__________________________ ;
Na2CO3:
CH3COOH:
NH4Cl:
H2SO4:
H2CO3:
更新时间:2021-01-13 21:42:59
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)①H3PO2是一元中强酸,写出其电离方程式___________ 。
②NaH2PO2为___________ (填“正盐”或“酸式盐”)。
③H3PO2中,P元素的化合价为___________ 。
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为________ 。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式______ 。
(1)①H3PO2是一元中强酸,写出其电离方程式
②NaH2PO2为
③H3PO2中,P元素的化合价为
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

请回答下列问题
(1)写出NaHSO4溶液的电离方程式___________ ;图中代表滴加H2SO4溶液的变化曲线___________ 。
(2)曲线①中从起始到a点反应的化学方程式___________ ;曲线②中bd段反应的离子方程式_________ 。
(3)b点对应溶液中大量存在的离子是___________ ;a点对应的溶液显___________ (填“酸性”、“中性”或“碱性”),此时溶液导电能力接近于0的原因是___________ 。

请回答下列问题
(1)写出NaHSO4溶液的电离方程式
(2)曲线①中从起始到a点反应的化学方程式
(3)b点对应溶液中大量存在的离子是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)写出下列物质在水中的电离方程式
碳酸氢钠______________________________________________________________ 。
亚硫酸________________________________ ,______________________________ 。
(2)已知25 ℃时有关弱酸的电离平衡常数如下:HCN:4.9×10-10,H2CO3:K1=4.4×10-7 K2=4.7×10-11,向NaCN溶液中通入少量二氧化碳气体,写出发生反应的离子方程式_____ 。
碳酸氢钠
亚硫酸
(2)已知25 ℃时有关弱酸的电离平衡常数如下:HCN:4.9×10-10,H2CO3:K1=4.4×10-7 K2=4.7×10-11,向NaCN溶液中通入少量二氧化碳气体,写出发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。如下表所示:
含氧酸酸性强弱与非羟基氧原子数的关系
(1)已知,亚磷酸是中强酸,亚砷酸是弱酸且有一定的弱碱性,则H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是①_____________________________ ,②__________________________________ 。
(2)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况______________ ,写出化学方程式:____________________________________________________ 。
含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl—OH |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
(2)在H3PO3和H3AsO3中分别加入浓盐酸,分析反应情况
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】双氧水(H2O2)和水都是极弱电解质,但H2O2比H2O更显酸性。
(1)若把H2O2看成是二元弱酸,请写出在水中的电离方程式:_______ 。
(2)鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成盐的两个化学方程式:___________________________________________________ ;_______________________________________________ 。
(3)水电离生成H3O+和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离的方程式:_________________ 。
(1)若把H2O2看成是二元弱酸,请写出在水中的电离方程式:
(2)鉴于H2O2显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出H2O2与Ba(OH)2作用形成盐的两个化学方程式:
(3)水电离生成H3O+和OH-叫做水的自偶电离。同水一样,H2O2也有极微弱的自偶电离,其自偶电离的方程式:
您最近一年使用:0次

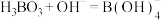 ,则硼酸的电离方程式为
,则硼酸的电离方程式为 ,写出下列反应的离子方程式
,写出下列反应的离子方程式 通入
通入 溶液
溶液 与
与 溶液混合
溶液混合

