我们知道海带中含有碘元素,工业上常以海带为原料提取碘单质。查有关资料可知碘单质易升华。下面是某校化学探究小组设计的从海带中提取单质碘的实验,请你完成下列实验。
(1)将干燥洁净的海带用酒精润湿后在__________ (填一种仪器名称)中灼烧成灰烬。
(2)将海带灰冷却至室温,然后转移到烧杯中,加蒸馏水后,搅拌、煮沸冷却、__________ (填一种操作名称)。
(3)在滤液中滴入几滴稀硫酸,再加入一定量的 溶液,把溶液注入分液漏斗中,然后再加入
溶液,把溶液注入分液漏斗中,然后再加入 振荡、静置,可以观察到
振荡、静置,可以观察到 层呈
层呈__________ 色。经分液得到碘的 溶液,在这一实验过程中,
溶液,在这一实验过程中, 起
起__________ 作用。
(4)取少量碘的 溶液于试管中,然后进行水浴加热,待
溶液于试管中,然后进行水浴加热,待 挥发完即可得到固体碘单质。不用酒精灯直接加热蒸发
挥发完即可得到固体碘单质。不用酒精灯直接加热蒸发 的原因是
的原因是____________________________________________________ 。
(5)证明得到的固体是碘单质的化学方法是_____________________________________________________ 。
(1)将干燥洁净的海带用酒精润湿后在
(2)将海带灰冷却至室温,然后转移到烧杯中,加蒸馏水后,搅拌、煮沸冷却、
(3)在滤液中滴入几滴稀硫酸,再加入一定量的
 溶液,把溶液注入分液漏斗中,然后再加入
溶液,把溶液注入分液漏斗中,然后再加入 振荡、静置,可以观察到
振荡、静置,可以观察到 层呈
层呈 溶液,在这一实验过程中,
溶液,在这一实验过程中, 起
起(4)取少量碘的
 溶液于试管中,然后进行水浴加热,待
溶液于试管中,然后进行水浴加热,待 挥发完即可得到固体碘单质。不用酒精灯直接加热蒸发
挥发完即可得到固体碘单质。不用酒精灯直接加热蒸发 的原因是
的原因是(5)证明得到的固体是碘单质的化学方法是
20-21高一·全国·课时练习 查看更多[5]
福建省漳州市华安县第一中学2023-2024学年高一上学期10月月考化学试题福建省南安市侨光中学2022-2023学年高一上学期12月月考化学试题(已下线)3.3.2 从海水中提取镁 从海水中提取碘-2021-2022学年高一化学课后培优练(苏教版2019必修第一册)(已下线)第4章 化学与自然资源的开发利用(培优提升卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)专题3 第三单元 海洋化学资源的综合利用-高中化学苏教2019版必修第一册
更新时间:2021-01-11 22:27:35
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室里需要纯净的NaCl溶液,但手边只有混有Na2SO4、NH4HCO3的NaCl。某学生设计了如图所示方案提取纯净的NaCl溶液。(已知:NH4HCO3 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)

如果此方案正确,那么:
(1)进行操作①可选择的最常用仪器是______________ 。
(2)操作②为什么不用硝酸钡溶液,其理由是_____________________________ 。
(3)进行操作②后,如何判断 已除尽,方法是
已除尽,方法是_________________________ 。
(4)操作③的目的是________________ ,为什么不先过滤后加碳酸钠溶液?理由是____________ 。
(5)操作④的目的是________________________________________________ 。
 NH3↑+CO2↑+H2O)
NH3↑+CO2↑+H2O)
如果此方案正确,那么:
(1)进行操作①可选择的最常用仪器是
(2)操作②为什么不用硝酸钡溶液,其理由是
(3)进行操作②后,如何判断
 已除尽,方法是
已除尽,方法是(4)操作③的目的是
(5)操作④的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某校探究学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如图所示:
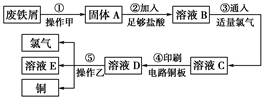
请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是________ 。
(2)步骤②中,除发生反应Fe+2HCl===FeCl2+H2↑外,其他可能反应的离子方程式为_______________________________________________________ 。
(3)溶液C的颜色是________ ,溶液D中可能含有的金属阳离子有_______________ 。
(4)可以验证溶液B中是否含有Fe2+的一种试剂是______ (填选项序号)。
a.稀硫酸 b.铁c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是________ ,步骤⑤产生金属铜的化学方程式为_______________________________________________________________________ 。

请回答下列问题:
(1)步骤①中先加入热的Na2CO3溶液除油污,操作甲的名称是
(2)步骤②中,除发生反应Fe+2HCl===FeCl2+H2↑外,其他可能反应的离子方程式为
(3)溶液C的颜色是
(4)可以验证溶液B中是否含有Fe2+的一种试剂是
a.稀硫酸 b.铁c.硫氰化钾 d.酸性高锰酸钾溶液
(5)操作乙的名称是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组用如图所示装置制取氯酸钾、次氯酸钠和氯水并进行有关探究实验。

实验Ⅰ.制取氯酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学方程式___________ 。
(2)制取实验结束后,取出装置B中试管,冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、___________ 、___________ 。为提高氯酸钾和次氯酸钠的产率,在实验装置中还需要改进的是___________ 。
(3)装置C中反应需要在冰水浴中进行,其原因是___________ 。
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为___________ 色。
实验Ⅱ.尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO 。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。
。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。
①提出合理假设
假设1:只存在SO ;假设2:即不存在SO
;假设2:即不存在SO ,也不存在ClO-;假设3:
,也不存在ClO-;假设3:___________ 。
②设计实验方案,进行实验。请完成下列表格,写出相应的实验步骤以及预期现象和结论。限选实验试剂:3 mol·L-1H2SO4、1 mol·L-1NaOH溶液、0.01 mol·L-1酸性KMnO4溶液、淀粉KI溶液。

实验Ⅰ.制取氯酸钾、次氯酸钠和氯水
(1)写出装置A实验室制取Cl2的化学方程式
(2)制取实验结束后,取出装置B中试管,冷却结晶、过滤、洗涤。该实验操作过程需要的玻璃仪器有胶头滴管、烧杯、
(3)装置C中反应需要在冰水浴中进行,其原因是
(4)装置D中的实验现象是溶液先变红后褪色,最后又变为
实验Ⅱ.尾气处理
实验小组利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(5)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH-和SO
 。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。
。请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气中CO2的影响)。①提出合理假设
假设1:只存在SO
 ;假设2:即不存在SO
;假设2:即不存在SO ,也不存在ClO-;假设3:
,也不存在ClO-;假设3:②设计实验方案,进行实验。请完成下列表格,写出相应的实验步骤以及预期现象和结论。限选实验试剂:3 mol·L-1H2SO4、1 mol·L-1NaOH溶液、0.01 mol·L-1酸性KMnO4溶液、淀粉KI溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液分置于A、B试管中 | |
| 步骤2:向A试管中滴加0.01 mol·L-1酸性KMnO4溶液 | (1)若溶液褪色,则假设1成立 (2)若溶液不褪色,则假设2或3成立 |
| 步骤3: | (1)若 (2)若 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】海洋资源的利用具有非常广阔的前景。
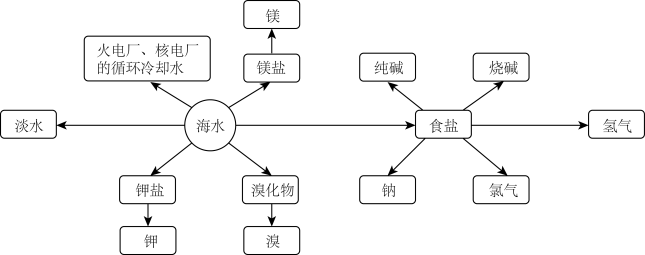
回答下列问题:
Ⅰ.海水制盐
(1)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式___________ 。
Ⅱ.海水提溴
(2)工业上常用“吹出法”提溴,请写出用 吸收
吸收 的化学反应方程式
的化学反应方程式___________ 。
(3)含 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是___________ 。
Ⅲ.从海带中提取碘的实验过程如下图所示:
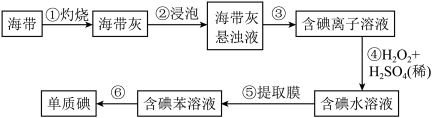
(4)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(5)请写出步骤④反应的离子方程式___________ 。
Ⅳ.海水淡化
(6)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是___________ 。

回答下列问题:
Ⅰ.海水制盐
(1)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式
Ⅱ.海水提溴
(2)工业上常用“吹出法”提溴,请写出用
 吸收
吸收 的化学反应方程式
的化学反应方程式(3)含
 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是Ⅲ.从海带中提取碘的实验过程如下图所示:

(4)步骤①中灼烧海带时,应将海带放入
(5)请写出步骤④反应的离子方程式
Ⅳ.海水淡化
(6)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.已知化学反应N2+3H2 2NH3的能量变化如图所示,回答下列问题:
2NH3的能量变化如图所示,回答下列问题:

(1)1molNH3(g)分解生成0.5molN2(g)和1.5molH2(g)的过程_______ (填“吸收”或“放出”)的能量为_______ 。
Ⅱ.海水中含有丰富的化学资源。将海水淡化与浓缩海水是综合利用海水资源的途径之一。从海水中提取镁的主要步骤如下:

(2)操作a的名称是_______ ;试剂X可以选用_______ 。
Ⅲ.碘在海水中主要以I-的形式存在,而在地壳中主要以IO 的形式存在,在常温下几种粒子之间的转化关系如图所示。
的形式存在,在常温下几种粒子之间的转化关系如图所示。

(3)对比反应Ⅰ和Ⅲ可知,以反应Ⅰ制取I2时应注意控制的反应条件是_______ 。
(4)用反应Ⅱ在溶液中制取I2,反应的离子方程式是(已知:反应后所得溶液显酸性)_______ 。
 2NH3的能量变化如图所示,回答下列问题:
2NH3的能量变化如图所示,回答下列问题:
(1)1molNH3(g)分解生成0.5molN2(g)和1.5molH2(g)的过程
Ⅱ.海水中含有丰富的化学资源。将海水淡化与浓缩海水是综合利用海水资源的途径之一。从海水中提取镁的主要步骤如下:

(2)操作a的名称是
Ⅲ.碘在海水中主要以I-的形式存在,而在地壳中主要以IO
 的形式存在,在常温下几种粒子之间的转化关系如图所示。
的形式存在,在常温下几种粒子之间的转化关系如图所示。
(3)对比反应Ⅰ和Ⅲ可知,以反应Ⅰ制取I2时应注意控制的反应条件是
(4)用反应Ⅱ在溶液中制取I2,反应的离子方程式是(已知:反应后所得溶液显酸性)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)现有8个微粒: ;
; ;
;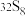 ;
;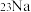 ;
;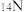 ;
; ;
; ;
; ;
;
表示核素的符号共______ 种;互为同位素的是______ 。
(2)现有以下物质:① ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。
其中由离子键和非极性共价键构成的物质是______ (填序号,下同),属于共价化合物的是______ 。
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是______ (填序号),仅离子键被破坏的是______ (填序号)。
(4)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式______ 。反应结束后,再加入 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为______ ,可以观察到 层呈
层呈______ 色。
(1)现有8个微粒:
 ;
; ;
;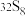 ;
;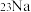 ;
;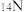 ;
; ;
; ;
; ;
;表示核素的符号共
(2)现有以下物质:①
 ;②
;② ;③NaOH;④
;③NaOH;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ 。
。其中由离子键和非极性共价键构成的物质是
(3)下列变化:①碘升华;②冰融化;③氯化钠溶于水;④氯化氢溶于水;⑤氢氧化钠溶于水。化学键未被破坏的是
(4)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为 层呈
层呈
您最近一年使用:0次



