下列热化学方程式中,正确的是
| A.甲烷燃烧热为890.3 kJ•mol-1,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=+890.3 kJ•mol-1 |
| B.稀硫酸和稀氢氧化钠溶液混合,其热化学方程式为:H++OH-=H2O △H=-57.3 kJ•mol-1 |
| C.H2燃烧热为285.8kJ•mol-1,燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ•mol-1 |
D.500℃、30 MPa下,将1 mol N2和3 mol H2置于密闭的容器中充分反应生成NH3(g),放热38.6 kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) △H=-38.6 kJ·mol-1 2NH3(g) △H=-38.6 kJ·mol-1 |
更新时间:2021-01-23 09:44:46
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于反应热和热化学反应的描述中正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则CH3COOH和NaOH反应的中和热ΔH=-57.3 kJ·mol-1 |
| B.CO(g)的燃烧热是283.0 kJ·mol-1,则反应2CO(g)+O2(g)===2CO2(g)的ΔH=+2×283.0 kJ·mol-1 |
C.氢气的燃烧热为285.5 kJ·mol-1,则电解水的热化学方程式为2H2O(l) 2H2(g)+O2(g) ΔH=+2×285.5 kJ·mol-1 2H2(g)+O2(g) ΔH=+2×285.5 kJ·mol-1 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳时所放出的热量是甲烷的燃烧热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验装置图可以实现对应实验目的的是
| 选项 | A | B |
| 实验目的 | 测定中和热 | 探究过氧化钠与水反应放热 |
| 实验装置 |  |  |
| 选项 | C | D |
| 实验目的 | 探究不同催化剂对 分解速率的影响 分解速率的影响 | 探究相同浓度的不同酸与大理石反应对速率的影响 |
| 实验装置 | 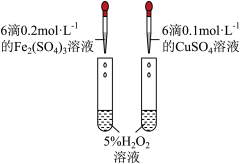 | 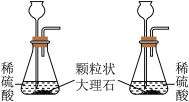 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列热化学方程式书写正确的是( )
A.S(s)+ O2(g)===SO3(g)ΔH=-315 kJ·mol-1(燃烧热) (ΔH的数值正确) O2(g)===SO3(g)ΔH=-315 kJ·mol-1(燃烧热) (ΔH的数值正确) |
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是CH3OH(g)+ O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1,则CH3OH(g)的燃烧热为192.9 kJ·mol-1 |
| C.已知常温常压下:HCl(aq)+NaOH(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则有:H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+2H2O(l) ΔH=-114.6 kJ·mol-1 |
| D.已知:S(s)+O2(g)===SO2(g) ΔH1=-Q1 kJ·mol-1,S(g)+O2(g)===SO2(g) ΔH2=-Q2 kJ·mol-1,则Q1<Q2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关热化学方程式书写及对应表述均正确的是
A.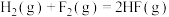 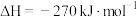 ,则相同条件下,2mol HF(g)的能量大于1mol ,则相同条件下,2mol HF(g)的能量大于1mol  (g)和1mol (g)和1mol  (g)的能量之和 (g)的能量之和 |
B.密闭容器中,9.6g硫粉与11.2g铁粉混合加热充分反应,放出19.12kJ热量,则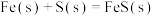 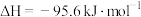 |
C.2g  完全燃烧生成液态水,放热285.8kJ,则表示氢气燃烧热的热化学方程式为 完全燃烧生成液态水,放热285.8kJ,则表示氢气燃烧热的热化学方程式为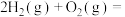 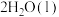 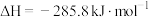 |
D.若  ; ;  ,则硫的燃烧热为 ,则硫的燃烧热为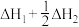 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
A.若 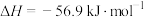 ,则1 mol ,则1 mol 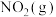 置于密闭容器中充分反应放出的热量为28.45kJ 置于密闭容器中充分反应放出的热量为28.45kJ |
B.若31 g白磷的能量比31 g红磷多b kJ,则白磷转化为红磷的热化学方程式为 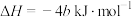 |
C.在稀溶液中,强酸与强碱反应的中和热为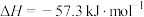 ,若将含有0.5 mol ,若将含有0.5 mol  的浓硫酸和含有1 mol NaOH的溶液混合,放出的热量等于57.3kJ 的浓硫酸和含有1 mol NaOH的溶液混合,放出的热量等于57.3kJ |
D. 的摩尔燃烧焓是 的摩尔燃烧焓是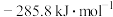 ,则 ,则 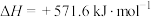 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式中,正确 的是( )
| A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g) + 2O2(g) = CO2(g) + 2H2O(g);ΔH=-890.3 kJ·mol-1 |
| B.稀盐酸与稀氢氧化钠溶液混合,其热化学方程式为:H+(aq) + OH-(aq) = H2O(l);ΔH=-57.3 kJ·mol-1 |
C.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g) 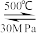 2NH3(g);ΔH=-38.6 kJ·mol-1 2NH3(g);ΔH=-38.6 kJ·mol-1 |
| D.1 mol H2完全燃烧放热142.9 kJ,则氢气燃烧的热化学方程式为:2H2(g) + O2(g) = 2H2O(l);ΔH=+285.8 kJ· mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和所得到的结论均正确的是
| 选项 | 实验内容 | 实验结论 |
| A | 将Fe(NO3)2样品溶于稀HNO3溶液中,加入KSCN溶液,显红色 | Fe(NO3)2已经氧化变质 |
| B | 用pH试纸测定同浓度的NaCl和NaF溶液的pH,pH(NaCl)<pH(NaF) | 结合H+能力:Cl-<F- |
| C | 取1mL0.1mol/LKI溶液于试管中,加入5mL0.1mol/LFeCl3,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI和FeCl3反应有一定限度 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关热化学方程式的叙述正确的是
A.已知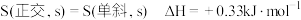 ,则单斜硫比正交硫稳定 ,则单斜硫比正交硫稳定 |
B.一定条件下,将 和 和 置于密闭容器中充分反应生成 置于密闭容器中充分反应生成 放热 放热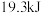 ,其热化学方程式为 ,其热化学方程式为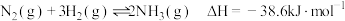 |
C. 稀硫酸和足量稀 稀硫酸和足量稀 溶液反应放出的热量就是中和热,为 溶液反应放出的热量就是中和热,为 |
D.已知乙醇的燃烧热为 ,则乙醇燃烧的热化学方程式可表示为 ,则乙醇燃烧的热化学方程式可表示为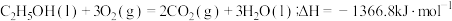 |
您最近一年使用:0次

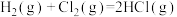 在光照和点燃条件下的△H相同
在光照和点燃条件下的△H相同 ,则1mol硫酸与足量氢氧化钡溶液反应放热114.6kJ
,则1mol硫酸与足量氢氧化钡溶液反应放热114.6kJ 与1mol
与1mol 充分反应后,释放出98kJ的热量,则其热化学方程式为
充分反应后,释放出98kJ的热量,则其热化学方程式为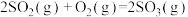
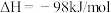
 H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)= 2SO3(g) ΔH= -Q1。在相同条件下,向一密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2,则Q1、Q2满足的关系是
2SO3(g) ΔH= -Q1。在相同条件下,向一密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2,则Q1、Q2满足的关系是

