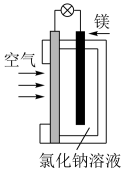
燃料电池在日常生活和科学研究中越来越得到广泛使用。镁-空气燃料电池是一种新型的燃料电池,可应用于电动汽车,其工作原理如图所示:
回答下列问题:
(1)通入空气的电极是______ (填“正”或“负”)极。
(2)镁电极发生______ (填“氧化”或“还原”)反应。
(3)电池总反应方程式为______ 。

回答下列问题:
(1)通入空气的电极是
(2)镁电极发生
(3)电池总反应方程式为
更新时间:2021-02-19 16:10:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】将锌片和铜片用导线相连插入稀硫酸溶液中,则锌片做___ 极,现象为_____ ;铜片做__ 极,现象为____ 。负极反应方程式为:___ 。正极反应方程式为:_____ 。当电路中通过3.01×1024个电子时,参与反应的Zn的质量是____ g。
您最近一年使用:0次
填空题
|
较易
(0.85)
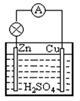
【推荐2】原电池是把__________ 转化成__________ 的装置,其反应的实质是_____________ 。在铜锌原电池(稀硫酸为介质)中:
正极材料是____ ,其电极反应式:___________ ;
负极材料是____ ,其电极反应式:___________ 。
正极材料是
负极材料是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】化学电源在生产生活中有着广泛的应用,回答下列问题:
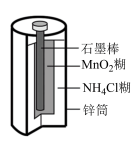
(1)常见的锌锰干电池其构造如图所示。常见的锌锰干电池属于___________ (填“一次电池”或“二次电池”),从氧化还原反应的角度分析,锌筒上发生的反应属于_________ 反应。
(2)为了探究化学反应中的能量变化,某同学设计了如图中的两个实验装置(装置中除连接的铜棒不同外,其他均相同),下列有关实验现象的说法正确的是_________ (填标号)。
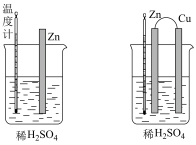
A.两装置温度计的示数相等,且均高于室温
B.两装置的气泡均产生于锌棒表面
C.连接铜棒的装置产生气体的速度快
(3)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸溶液中,乙同学将电极放入等浓度的 溶液中,如图所示。
溶液中,如图所示。
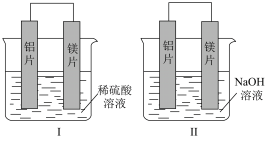
①装置Ⅰ中放电时氢离子向_________ (填“镁片”或“铝片”)移动。写出装置Ⅰ中正极的电极反应式:_________ 。
②装置Ⅱ中铝片为_________ 极,写出该电极的电极反应式_________ 。
③如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的结论。依据该实验得出的下列结论中,正确的有_________ (填标号)。
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(1)常见的锌锰干电池其构造如图所示。常见的锌锰干电池属于

(2)为了探究化学反应中的能量变化,某同学设计了如图中的两个实验装置(装置中除连接的铜棒不同外,其他均相同),下列有关实验现象的说法正确的是

A.两装置温度计的示数相等,且均高于室温
B.两装置的气泡均产生于锌棒表面
C.连接铜棒的装置产生气体的速度快
(3)有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入稀硫酸溶液中,乙同学将电极放入等浓度的
 溶液中,如图所示。
溶液中,如图所示。
①装置Ⅰ中放电时氢离子向
②装置Ⅱ中铝片为
③如果甲与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的结论。依据该实验得出的下列结论中,正确的有
A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动性顺序表已过时,没有实用价值了
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)利用多晶铜高效催化电解 制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现
制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现 的连续转化。
的连续转化。
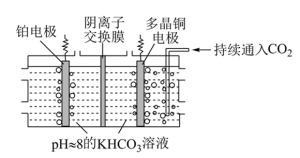
①电解过程中 向
向_______ (填“铂”或“多晶铜”)电极方向移动。
②多晶铜电极的电极反应式为_______ ;
③理论上当生产 乙烯时,铂电极产生的气体在标况下体积为
乙烯时,铂电极产生的气体在标况下体积为_______ (不考虑气体的溶解)。
(2)某钠离子电池结构如图所示,电极A为含钠过渡金属氧化物(NaxTMO2),电极B为硬碳,充电时Na+得电子成为Na嵌入硬碳中,NaTMO2失去电子生成Na1−xTMO2,充电时B极的电极反应:_______ ,放电时A极的电极方程式:_______ 。

(1)利用多晶铜高效催化电解
 制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现
制乙烯的原理如图所示。因电解前后电解液浓度几乎不变,故可实现 的连续转化。
的连续转化。
①电解过程中
 向
向②多晶铜电极的电极反应式为
③理论上当生产
 乙烯时,铂电极产生的气体在标况下体积为
乙烯时,铂电极产生的气体在标况下体积为(2)某钠离子电池结构如图所示,电极A为含钠过渡金属氧化物(NaxTMO2),电极B为硬碳,充电时Na+得电子成为Na嵌入硬碳中,NaTMO2失去电子生成Na1−xTMO2,充电时B极的电极反应:

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氢氧燃料电池
| 电解质 | H2SO4溶液 | KOH溶液 | 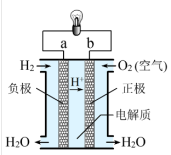 |
| 总反应 | 2H2+O2=2H2O | ||
| 负极反应式 | |||
| 正极反应式 | |||
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据元素周期表中短周期的下列内容回答问题:
(1)元素①~⑨形成的单质中,化学性质最稳定的是_____ (填化学式)。④在元素周期表中的位置是________ ,⑥的简单离子的结构示意图为________________
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为________________ ,⑤、⑧按原子个数比2:1形成的化合物的电子式为________________
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:________________
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为________________
| H | ① | ||||||
| ② | ③ | O | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素①~⑨形成的单质中,化学性质最稳定的是
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学小组探究不同条件下化学能转变为电能的装置如图。回答问题:
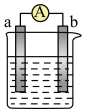
(1)若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:____ 。
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液为电解液;则CH4应通入____ 极(填a或b,下同),电子从_____ 极流出。电池的负极反应式为:_____ 。

(1)若电极a为Fe、电极b为Cu、电解质溶液为稀硫酸时,正极的电极反应式为:
(2)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所放出的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,CH4为燃料,采用酸性溶液为电解液;则CH4应通入
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.图为铜锌原电池的装置请回答:
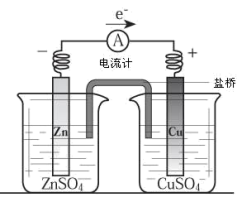
(1)铜是_________ 极,铜片上现象是_____________________
(2)锌为________ 极,电极反应式为_____________________
(3)电池反应式(离子反应)为____________________________________
II.氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定,请回答:
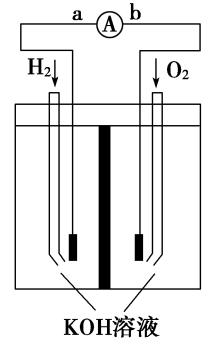
(4)在导线中电子流动方向为_________ (用a、b表示)。
(5)负极反应式为___________ 。正极反应式为___________ 。
(6)电极表面镀铂粉的原因为_____________________________________ 。

(1)铜是
(2)锌为
(3)电池反应式(离子反应)为
II.氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定,请回答:

(4)在导线中电子流动方向为
(5)负极反应式为
(6)电极表面镀铂粉的原因为
您最近一年使用:0次

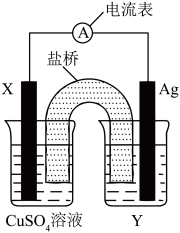
 C.Ag+ D.SO
C.Ag+ D.SO


