下列物质是生活生产中常见的物质:①NaHSO4晶体,②熔化Na2CO3,③冰醋酸(CH3COOH固体), ④石墨,⑤NaOH固体,⑥Fe(OH)3胶体,⑦酒精(C2H5OH) ,⑧液态O2 ,⑨盐酸,⑩金属钠,请回答下列问题(用序号):
(1)以上物质中能导电的是___________
(2)以上物质属于电解质的是___________
(3)以上物质中属于非电解质的是___________
(4)a.写出制备⑥的实验操作为___________ ; b.制备⑥的化学方程式为___________ ,
(5)足量盐酸与②溶液反应的离子方程式为___________
(6)写出③与⑤在溶液中反应的离子方程式___________
(1)以上物质中能导电的是
(2)以上物质属于电解质的是
(3)以上物质中属于非电解质的是
(4)a.写出制备⑥的实验操作为
(5)足量盐酸与②溶液反应的离子方程式为
(6)写出③与⑤在溶液中反应的离子方程式
更新时间:2021-03-02 14:45:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】I.请回答下列问题:
(1)现有以下物质:①NaCl晶体 ②SO2 ③液态醋酸 ④铜 ⑤固体BaSO4 ⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KHSO4 ⑨氨水 ⑩液氮。
①以上物质能导电但不是电解质的是_______ ;属于非电解质的是_______ ;(填相应序号)
②写出⑧的电离方程式:_______ 。
II. A、B、C、D四种物分别是NH3·H2O、CH3COOH、NaOH、HCl中的一种。常温下进行下列实验:
(2)0.001mol/L的A溶液pH=3,则A是_______ 。
(3)B溶液和D溶液显碱性,等浓度两者pH关系B<D;用水稀释0.1 mol/L B时,溶液中随着水量的增加而减小的是___________(填写序号)。
III.水溶液是中学化学的重点研究对象。
(4)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离的c(H+)=10-9 mol·L-1,则该电解质可能是_______ (填序号)。
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
(1)现有以下物质:①NaCl晶体 ②SO2 ③液态醋酸 ④铜 ⑤固体BaSO4 ⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KHSO4 ⑨氨水 ⑩液氮。
①以上物质能导电但不是电解质的是
②写出⑧的电离方程式:
II. A、B、C、D四种物分别是NH3·H2O、CH3COOH、NaOH、HCl中的一种。常温下进行下列实验:
(2)0.001mol/L的A溶液pH=3,则A是
(3)B溶液和D溶液显碱性,等浓度两者pH关系B<D;用水稀释0.1 mol/L B时,溶液中随着水量的增加而减小的是___________(填写序号)。
A. | B. | C.c(H+)与c(OH-)的乘积 | D.OH-的物质的量 |
III.水溶液是中学化学的重点研究对象。
(4)水是极弱的电解质,也是最重要的溶剂。常温下某电解质溶解在水中后,溶液中由水电离的c(H+)=10-9 mol·L-1,则该电解质可能是
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)按要求写出方程式:
①HNO3(电离方程式)_______ 。
②Fe2(SO4)3(电离方程式)_______ 。
③硫酸钠和氯化钡溶液反应(离子方程式_______ 。
④二氧化碳通入足量氢氧化钠溶液(离子方程式)_______ 。
(2)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有_______ ,属于非电解质的有_______ (填序号)。
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是_______ (用化学式表示,下同),_______ 元素被氧化,还原产物为_______ 。
②用单线桥在方程式中标出电子转移的情况:_______ 。
③当反应中有1 mol Na2FeO4生成,转移的电子有_______ mol。
④实验室欲配制250 mL 0.1 mol·L-1 NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为_______ ,下列操作配制的溶液浓度偏低的是_______ 。
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线
①HNO3(电离方程式)
②Fe2(SO4)3(电离方程式)
③硫酸钠和氯化钡溶液反应(离子方程式
④二氧化碳通入足量氢氧化钠溶液(离子方程式)
(2)以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有
(3)高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O
①该反应中氧化剂是
②用单线桥在方程式中标出电子转移的情况:
③当反应中有1 mol Na2FeO4生成,转移的电子有
④实验室欲配制250 mL 0.1 mol·L-1 NaOH溶液,除烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器为
A.称量NaOH时,将NaOH放在纸上称重
B.配制前,容量瓶中有少量蒸馏水
C.配制时,NaOH未冷却直接定容
D.向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
E.定容时俯视刻度线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有下列物质:
①熔融NaCl ② 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨
⑧铜 ⑨ ⑩
⑩
回答下列问题:
(1)上述物质中属于电解质的是_______ (填标号)。
(2)将②逐滴加入⑥中的现象是_______ 。
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为_______ 。
(4)③通入石灰乳中,发生反应的离子方程式为_______ 。
(5)向饱和食盐水中通入⑦和⑩,④会以沉淀的形式析出,反应的化学方程式为_______ 。
①熔融NaCl ②
 溶液 ③氯气 ④
溶液 ③氯气 ④ ⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦
⑤NaOH溶液 ⑥氢氧化铁胶体 ⑦ ⑧铜 ⑨
⑧铜 ⑨ ⑩
⑩
回答下列问题:
(1)上述物质中属于电解质的是
(2)将②逐滴加入⑥中的现象是
(3)④加入过量的氢氧化钡溶液中,发生反应的离子方程式为
(4)③通入石灰乳中,发生反应的离子方程式为
(5)向饱和食盐水中通入⑦和⑩,④会以沉淀的形式析出,反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有以下几种物质:①液氧 ②硝酸钾溶液 ③CuSO4 ④干冰 ⑤Fe
⑥熔融的NaCl ⑦纯碱 ⑧H2SO4 ⑨熟石灰 ⑩澄清石灰水
属于混合物的是______ ,属于盐的是______ ,属于酸的是______ ,属于碱的是______ ,属于酸性氧化物的是______ ,属于单质的是______ ,属于电解质的是______ ,属于非电解质的是______ ,能导电的是______ 。
⑥熔融的NaCl ⑦纯碱 ⑧H2SO4 ⑨熟石灰 ⑩澄清石灰水
属于混合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列物质:①Fe2(SO4)3溶液 ②酒精 ③二氧化硫 ④铜 ⑤过氧化钠 ⑥FeSO4溶液 ⑦CuO ⑧漂白粉,回答下列问题:
(1)在表格空白处填写符合条件物质的序号
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:_______ (用离子方程式表示)。
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为_________ 。
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=______ 。
(5)设计实验证明某溶液含有①、⑥中的两种阳离子_________ 。
(1)在表格空白处填写符合条件物质的序号
| 条件 | 序号 |
| 能导电 | |
| 属于碱性氧化物 | |
| 属于电解质 |
(2)从上述物质中选择试剂,证明氧化性Fe3+>Cu2+:
(3)⑥中混有少量的①,除杂过程中选用的试剂和操作方法为
(4)将1.12g铁粉加入25mL2 mol•L-1的①中,充分反应后溶液中n(Fe3+)∶n(Fe2+)=
(5)设计实验证明某溶液含有①、⑥中的两种阳离子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质,回答有关问题。
A.氢氧化铝胶体;B.食盐水;C.铜;D.硝酸;E.烧碱;F.蔗糖;G.泥水;H.一氧化碳;I. CuSO4·5H2O晶体;J. CO2 ;K.HCl气体;L.CaO固体;M.食醋(含醋酸的溶液)
(1)以上物质中属于电解质的是_________ (填序号)。
(2)以上物质中的酸性氧化物与足量氢氧化钠反应的方程式__________________ 。
(3)写出下列物质在水溶液中的电离方程式:
Ca(OH)2__________________ ;
K2CO3__________________ ;
NaHSO4__________________ ;
醋酸(CH3COOH)__________________ 。
A.氢氧化铝胶体;B.食盐水;C.铜;D.硝酸;E.烧碱;F.蔗糖;G.泥水;H.一氧化碳;I. CuSO4·5H2O晶体;J. CO2 ;K.HCl气体;L.CaO固体;M.食醋(含醋酸的溶液)
(1)以上物质中属于电解质的是
(2)以上物质中的酸性氧化物与足量氢氧化钠反应的方程式
(3)写出下列物质在水溶液中的电离方程式:
Ca(OH)2
K2CO3
NaHSO4
醋酸(CH3COOH)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①NaCl晶体②液态SO3③液态氯化氢④汞⑤BaSO4固体⑥纯蔗糖(C12H22O11) ⑦酒精(C2H5OH) ⑧熔化的KNO3,请回答下列问题(用序号):
(1)以上物质中能导电的是_________________ 。
(2)以上物质中属于电解质的是___________________ 。
(3)以上物质中属于非电解质的是____________________ 。
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】阅读下列科普短文并填空。
燃料电池具有能量转化率高、对环境友好等特点。燃料电池在工作时,从负极连续通入①氢气或②CH4等燃料,从正极连续通入③氧气,二者在电池内部(含有④H2SO4或⑤KOH等物质的溶液)发生反应生成⑥H2O、⑦CO2或⑧K2CO3溶液,同时产生电能。
(1)在上述短文标有序号(下划线)的物质中,能导电的是____ (填序号,下同);属于强电解质的是_______ ;属于非电解质的是_______ 。
(2)过量⑦通入⑤的溶液或⑧中均能生成同种物质,该物质与④的溶液反应的离子方程式为_____ 。
(3)将⑤的溶液逐滴加入10mL同浓度④的溶液中,此过程溶液的电导率变化曲线为下图中的____ (填“I”或“II”),a=_______ mL。
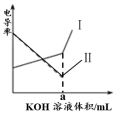
(4)甲烷燃料电池理论上负极通入②,将产生同温同压下相同体积的⑦,则②与⑦的质量比为___ 。
燃料电池具有能量转化率高、对环境友好等特点。燃料电池在工作时,从负极连续通入①氢气或②CH4等燃料,从正极连续通入③氧气,二者在电池内部(含有④H2SO4或⑤KOH等物质的溶液)发生反应生成⑥H2O、⑦CO2或⑧K2CO3溶液,同时产生电能。
(1)在上述短文标有序号(下划线)的物质中,能导电的是
(2)过量⑦通入⑤的溶液或⑧中均能生成同种物质,该物质与④的溶液反应的离子方程式为
(3)将⑤的溶液逐滴加入10mL同浓度④的溶液中,此过程溶液的电导率变化曲线为下图中的

(4)甲烷燃料电池理论上负极通入②,将产生同温同压下相同体积的⑦,则②与⑦的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知0.1mol·L-1的NaHSO4溶液中H+浓度为0.1mol·L-1,请回答下列问题:
(1)写出NaHSO4在水溶液中的电离方程式:_______ ;
(2)NaHSO4属于“酸”、“碱”、“盐”中的_______ ;
(3)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为2∶1混合,反应的化学方程式为_______ ;
(4)向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
①写出反应的离子方程式:_______ 。
②下列三种情况下,离子方程式与①相同的是_______ (填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
(5)向Ba(OH)2溶液中若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的_______ 曲线表示(填序号)。
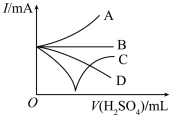
(6)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将_______ 。

(1)写出NaHSO4在水溶液中的电离方程式:
(2)NaHSO4属于“酸”、“碱”、“盐”中的
(3)若将NaHSO4与Ba(OH)2在溶液中按照物质的量之比为2∶1混合,反应的化学方程式为
(4)向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
①写出反应的离子方程式:
②下列三种情况下,离子方程式与①相同的是
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至
 恰好完全沉淀
恰好完全沉淀C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
(5)向Ba(OH)2溶液中若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用下图中的

(6)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学方程式是化学反应简明的表达形式。它从“质”和“量”两个方面表达了化学反应的意义。请根据题意完成以下方程式。
Ⅰ.写出下列物质在水溶液中的电离方程式。
①KNO3___ 。
②H2SO4__ 。
Ⅱ.写出下列反应的离子方程式
①实验室制备氢氧化铁胶体___ 。
②过氧化钠与水的反应__ 。
③NaHSO4和过量Ba(OH)2溶液混合___ 。
Ⅲ.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的原理:4Ag+2H2S+O2=2X+2H2O,则X的化学式为__ 。
Ⅰ.写出下列物质在水溶液中的电离方程式。
①KNO3
②H2SO4
Ⅱ.写出下列反应的离子方程式
①实验室制备氢氧化铁胶体
②过氧化钠与水的反应
③NaHSO4和过量Ba(OH)2溶液混合
Ⅲ.宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的原理:4Ag+2H2S+O2=2X+2H2O,则X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有以下物质:①NaOH溶液;②液氯;③Ba(OH)2固体,④熔融KHSO4;⑤Fe(OH)3胶体:⑥水银;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩NaHCO3;
Ⅰ.(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于电解质的是___________ (填序号);以上纯净物中能导电的是___________ (填序号)。以上物质中是非电解质的是___________ (填序号)。
(2)写出⑩在水溶液中的电离方程式___________ 。
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2 mol/L Ba(OH)2溶液中滴加0.1 mol/L盐酸,测定导电率的变化如图所示,回答下列问题:
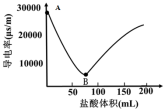
(3)该Ba(OH)2在水中导电率高,写出Ba(OH)2的电离方程式为___________ 。
(4)A—B段,发生的离子反应方程式是___________ 。
(5)B点恰好完全反应,此时溶液中存在的微粒有H2O、___________ 。
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是___________ 。
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
Ⅰ.(1)以上物质中属于混合物的是
(2)写出⑩在水溶液中的电离方程式
Ⅱ.将③Ba(OH)2固体配制成溶液,某小组实验室探究Ba(OH)2溶液与稀盐酸反应的实质。向0.2 mol/L Ba(OH)2溶液中滴加0.1 mol/L盐酸,测定导电率的变化如图所示,回答下列问题:

(3)该Ba(OH)2在水中导电率高,写出Ba(OH)2的电离方程式为
(4)A—B段,发生的离子反应方程式是
(5)B点恰好完全反应,此时溶液中存在的微粒有H2O、
(6)下列化学反应的实质与Ba(OH)2溶液和稀盐酸反应的实质相同的是
A.Ba(OH)2和H2SO4 B.NaOH 和H2SO4 C.Ba(OH)2与HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯及其化合物有重要用途,Cl2和ClO2气体均常用于自来水消毒。
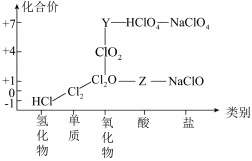
以上是氯元素的“价类二维图”的部分信息。请回答下列问题:
(1)根据图中信息写出 、
、 的化学式:
的化学式:____________________ 、__________________ 。
(2)请写出实验室制氯气的离子反应方程式:______________________________ 。
(3)氯气既有氧化性又还原性,结合上图说明理由:______________________________ 。
(4)工业常用 和
和 溶液混合酸化后反应制得
溶液混合酸化后反应制得 气体,该反应的离子方程式为:
气体,该反应的离子方程式为:__________________________ 。
(5)消毒效率可用单位质量消毒剂得到的电子数的相对大小来表示。 和
和 在消毒过程中均会被还原为
在消毒过程中均会被还原为 ,那么
,那么 的消毒效率是
的消毒效率是 的
的______ 倍。(计算结果保留至小数点后两位)
(6)84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原理为 ,反应产生的
,反应产生的 促进藻类快速生长。
促进藻类快速生长。
①该反应说明氧化性:NaClO______ H2O2(填“>”或“<”)。
②当标准状况下有11.2LO2生成时,转移电子______ mol。

以上是氯元素的“价类二维图”的部分信息。请回答下列问题:
(1)根据图中信息写出
 、
、 的化学式:
的化学式:(2)请写出实验室制氯气的离子反应方程式:
(3)氯气既有氧化性又还原性,结合上图说明理由:
(4)工业常用
 和
和 溶液混合酸化后反应制得
溶液混合酸化后反应制得 气体,该反应的离子方程式为:
气体,该反应的离子方程式为:(5)消毒效率可用单位质量消毒剂得到的电子数的相对大小来表示。
 和
和 在消毒过程中均会被还原为
在消毒过程中均会被还原为 ,那么
,那么 的消毒效率是
的消毒效率是 的
的(6)84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。其原理为
 ,反应产生的
,反应产生的 促进藻类快速生长。
促进藻类快速生长。①该反应说明氧化性:NaClO
②当标准状况下有11.2LO2生成时,转移电子
您最近一年使用:0次



