请根据要求书写出方程式。
(1)NO2与水形成酸雨的化学方程式为__ 。
(2)1754年,Briestly用硵砂(主要成分NH4Cl)和熟石灰共热制得了氨,化学反应方程式为__ 。
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式__ 。
(4)卫星发射时可用液态肼(N2H4)作燃料,16gN2H4(l)在氧气(g)中燃烧,生成氮气(g)和水蒸气,共放出255kJ热量。请写出该反应的热化学方程式__ 。
(1)NO2与水形成酸雨的化学方程式为
(2)1754年,Briestly用硵砂(主要成分NH4Cl)和熟石灰共热制得了氨,化学反应方程式为
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
(4)卫星发射时可用液态肼(N2H4)作燃料,16gN2H4(l)在氧气(g)中燃烧,生成氮气(g)和水蒸气,共放出255kJ热量。请写出该反应的热化学方程式
更新时间:2021-03-04 09:21:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】写出下列反应的化学方程式。
(1)NO2与水的反应:___________
(2)C与浓硫酸的反应:___________
(3)SiO2与NaOH溶液反应:___________
(4)实验室制氨气:___________
(5)NH3溶于水的反应:___________
(1)NO2与水的反应:
(2)C与浓硫酸的反应:
(3)SiO2与NaOH溶液反应:
(4)实验室制氨气:
(5)NH3溶于水的反应:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】依据图1中氮元素及其化合物的转化关系,回答问题:
(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为________________ .
(2)请从下图中选择正确的装置收集氨气_________
(3)下列试剂不能用于干燥NH3的是__ .A.浓硫酸 B.碱石灰 C.NaOH固体
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为__ .
②NO→NO2实验现象是__ .
③NO2 +H2O→HNO3氧化剂与还原剂物质的量之比为__ .
(5)将X转化为HNO3__ (填“是”或“不是”)氧化还原反应.
(6)若要将NH3→N2,从原理上看,下列试剂可行的是__ .
A.O2 B.Na C.NH4Cl D.NO2.

(1)实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为
(2)请从下图中选择正确的装置收集氨气
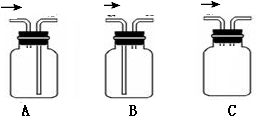
(3)下列试剂不能用于干燥NH3的是
(4)工业上以NH3、空气、水为原料生产硝酸分为三步:
①NH3→NO化学方程式为
②NO→NO2实验现象是
③NO2 +H2O→HNO3氧化剂与还原剂物质的量之比为
(5)将X转化为HNO3
(6)若要将NH3→N2,从原理上看,下列试剂可行的是
A.O2 B.Na C.NH4Cl D.NO2.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮是大气中含量最多的一种元素,氮及其化合物在生产、生活中有着重要作用。请回答下列问题:
(1)下列变化属于“氮的固定”的是___________ (填字母)
a.植物从土壤中吸收氮肥
b.硝酸和氨气反应生成氮肥
c.将空气中的氮气转变为氮的化合物
(2)下图是工业生产硝酸的流程。

①1909年化学家哈伯在实验室首次合成了氨。氨的电子式是___________ 。实验室用NH4Cl和Ca(OH)2制取氨气的化学方程式为:___________ 。
②2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

 、
、 、
、 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面。用文字描述图②→③表示的变化过程
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面。用文字描述图②→③表示的变化过程___________ 。
③写出氧化炉内反应的化学方程式___________ 。
④吸收塔中通入空气的目的是___________ 。
(1)下列变化属于“氮的固定”的是
a.植物从土壤中吸收氮肥
b.硝酸和氨气反应生成氮肥
c.将空气中的氮气转变为氮的化合物
(2)下图是工业生产硝酸的流程。

①1909年化学家哈伯在实验室首次合成了氨。氨的电子式是
②2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意如下:

 、
、 、
、 分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面。用文字描述图②→③表示的变化过程
分别表示N2、H2、NH3。图⑤表示生成的NH3离开催化剂表面。用文字描述图②→③表示的变化过程③写出氧化炉内反应的化学方程式
④吸收塔中通入空气的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】研究NO、NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)与氮氧化物有关的全球或区域性大气环境问题有_______ (填字母序号)。
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为___________ 。若该反应有0.6NA个电子转移,则参加反应的NO2的物质的量为___________ 。
(3)NH3也是重要的含氮化合物,实验室用NH4Cl和Ca(OH)2制取NH3。
①写出反应的化学方程式_________________
②若用下图所示装置收集氨气,气体由_____ 口进入。
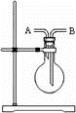
(4)硝酸可与不活泼金属铜发生反应。将过量的铜置入一定量的浓硝酸中,微热,充分反应后,待反应停止,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式解释 )_____________________
(5)若将12.8 g铜跟一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则整个反应过程中,被还原的HNO3总的物质的量是___________ mol。
(1)与氮氧化物有关的全球或区域性大气环境问题有
a.酸雨 b.沙尘暴 c.光化学烟雾 d.白色污染
(2)NO2可与水发生反应,反应的化学方程式为
(3)NH3也是重要的含氮化合物,实验室用NH4Cl和Ca(OH)2制取NH3。
①写出反应的化学方程式
②若用下图所示装置收集氨气,气体由

(4)硝酸可与不活泼金属铜发生反应。将过量的铜置入一定量的浓硝酸中,微热,充分反应后,待反应停止,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用
(5)若将12.8 g铜跟一定质量的浓硝酸反应,铜耗完时,共产生气体5.6 L(标准状况),则整个反应过程中,被还原的HNO3总的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以下是氮循环的一部分:

(1)通常状况下,NO2的颜色是___________ ,NO的颜色是___________ 。
(2)反应①的化学方程式是___________ 。
(3)NO2易溶于水,并和水发生化学反应。该反应中,氧化剂是___________ 。
(4)化合物A的化学式是___________ 。
(5)铜与稀硝酸反应的离子方程式为___________ 。
(6)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO 2CO2+N2,当生成2molN2时,被还原的NO为
2CO2+N2,当生成2molN2时,被还原的NO为___________ mol。

(1)通常状况下,NO2的颜色是
(2)反应①的化学方程式是
(3)NO2易溶于水,并和水发生化学反应。该反应中,氧化剂是
(4)化合物A的化学式是
(5)铜与稀硝酸反应的离子方程式为
(6)治理汽车尾气的一种方法是用催化剂使NO与CO发生反应:2NO+2CO
 2CO2+N2,当生成2molN2时,被还原的NO为
2CO2+N2,当生成2molN2时,被还原的NO为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)汽车尾气中的主要污染物是NO、NO2和CO。用NaOH溶液可吸收NO、NO2,当n(NO)﹕n(NO2)=1时只生成一种盐,这种盐的化学式为__________ 。
(2)金属铬(Cr)的英文是Chromium,原意是颜色,因为它的化合物都有美丽的颜色。如表是几种常见铬的化合物或离子的水溶液的颜色:
含铬元素的化合物可以发生如图一系列变化:

①写出反应④的离子方程式:______________________________________ 。
②结合上述转化图及所学知识,请分析向NaCrO2溶液中逐滴加入过量稀硫酸的现象为______ 。
(2)金属铬(Cr)的英文是Chromium,原意是颜色,因为它的化合物都有美丽的颜色。如表是几种常见铬的化合物或离子的水溶液的颜色:
| 离子或化合物 | Cr2O72- | Cr(OH)3 | Cr3+ | CrO2- | CrO42- |
| 颜色 | 橙色 | 灰蓝色 | 蓝紫色 | 绿色 | 黄色 |
含铬元素的化合物可以发生如图一系列变化:

①写出反应④的离子方程式:
②结合上述转化图及所学知识,请分析向NaCrO2溶液中逐滴加入过量稀硫酸的现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】由于人类的活动向大气排放 对环境造成了一定的污染,我国严格控制其排放总量,标志着国家已经从单纯控制
对环境造成了一定的污染,我国严格控制其排放总量,标志着国家已经从单纯控制 向全面控制酸性气体排放的方向走出了新的一步。
向全面控制酸性气体排放的方向走出了新的一步。
用 催化还原
催化还原 可以消除氮氧化合物的污染。例如:
可以消除氮氧化合物的污染。例如:
①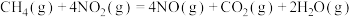 ;
; kJ/mol
kJ/mol
②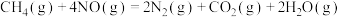 ;
; kJ/mol
kJ/mol
(1)根据上述信息推断正确的是___________
(2)正确的选项是___________
 对环境造成了一定的污染,我国严格控制其排放总量,标志着国家已经从单纯控制
对环境造成了一定的污染,我国严格控制其排放总量,标志着国家已经从单纯控制 向全面控制酸性气体排放的方向走出了新的一步。
向全面控制酸性气体排放的方向走出了新的一步。用
 催化还原
催化还原 可以消除氮氧化合物的污染。例如:
可以消除氮氧化合物的污染。例如:①
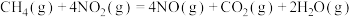 ;
; kJ/mol
kJ/mol②
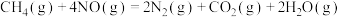 ;
; kJ/mol
kJ/mol(1)根据上述信息推断正确的是___________
A.等物质的量的 在反应①、②中转移电子数相同 在反应①、②中转移电子数相同 |
B.由反应②可推知: ; ; kJ/mol kJ/mol |
C. ; ; kJ/mol kJ/mol |
D.若用标准状况下4.48 L  把 把 还原为 还原为 ,整个过程中转移的电子总数为 ,整个过程中转移的电子总数为 |
| A.化学反应中,吸热反应需不断从外界获得能量,放热反应不需从外界获得能量 |
B.甲烷的燃烧热 kJ/mol,则甲烷燃烧的热化学方程式为: kJ/mol,则甲烷燃烧的热化学方程式为:  kJ/mol kJ/mol |
C.常温常压下: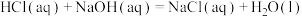 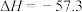 kJ/mol,则: kJ/mol,则: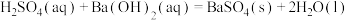  kJ/mol kJ/mol |
D.已知  kJ·mol kJ·mol , ,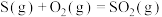  kJ/mol,则 kJ/mol,则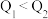 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知: 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。

(1)写出C2H4完全燃烧生成气态水的热化学方程式___________ 。
(2)H2的燃烧热ΔH=___________ 。
(3)相同条件下,C2H4的稳定性比C2H6___________ (填“强”“弱”或“相同”),等物质的量的C2H4和C2H6完全燃烧放热较多的是___________ 。
(4) 是
是___________ 反应(填“吸热”或“放热”)。
(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
已知: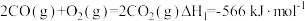 ;则a =
;则a =___________ 。
 时,1mol相关物质的相对能量如图所示。
时,1mol相关物质的相对能量如图所示。
(1)写出C2H4完全燃烧生成气态水的热化学方程式
(2)H2的燃烧热ΔH=
(3)相同条件下,C2H4的稳定性比C2H6
(4)
 是
是(5)已知键能是指气态分子中1mol化学键解离成气态原子所吸收的能量,相关的化学键键能如下。
| 化学键 | C O(CO) O(CO) | O=O | C=O |
| 键能(KJ/mol) | a | 500 | 1075 |
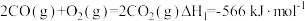 ;则a =
;则a =
您最近一年使用:0次

 和液态
和液态 ,放出890.3kJ的热量,
,放出890.3kJ的热量, 的燃烧热为
的燃烧热为

