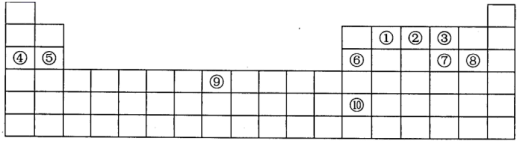
图为元素周期表的一部分,表中每一序号分别代表一种元素。_______ 。
(2)在元素①、②、③、⑦、⑧中,非金属性最强的是_______ (用所对应的元素符号表示)。
(3)元素⑩的单质可能具有的性质是_______ (填字母)。
a.能导电导热 b.能与稀盐酸反应生成氢气 c.能与氧气反应
(4)在元素④、⑤、⑨的最高价氧化物的水化物中,碱性最强的是_______ (填化学式)。
(5)元素②的一种氢化物为NH2NH2,写出该化合物分子的电子式_______ ,该分子内存在的共价键类型有_______ 。
(6)元素②同族中的另一元素P能呈现多种化合价,其中+3价氧化物对应的水化物为H3PO3,已知该酸与足量NaOH溶液反应所得产物化学式为Na2HPO3,则Na2HPO3是_______ (填“正盐”或“酸式盐”)。
(2)在元素①、②、③、⑦、⑧中,非金属性最强的是
(3)元素⑩的单质可能具有的性质是
a.能导电导热 b.能与稀盐酸反应生成氢气 c.能与氧气反应
(4)在元素④、⑤、⑨的最高价氧化物的水化物中,碱性最强的是
(5)元素②的一种氢化物为NH2NH2,写出该化合物分子的电子式
(6)元素②同族中的另一元素P能呈现多种化合价,其中+3价氧化物对应的水化物为H3PO3,已知该酸与足量NaOH溶液反应所得产物化学式为Na2HPO3,则Na2HPO3是
更新时间:2021-03-04 10:52:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素周期表是学习物质结构和性质的重要工具,下图是元素周期表的一部分,表中所列字母A、D、F、G、Q、M、R、N、T分别代表某种化学元素。请依据这9种元素回答下列问题。

(1)以上9种元素中金属性最强的元素是_______ (填元素符号)。
(2)元素的非金属性:M______ R(填“>”或“<”)。
(3)R的最高价氧化物对应水化物的化学式是_____________ 。
(4)F、G两元素形成的淡黄色固体物质的电子式为_____________ 。
(5)表中M、R、N元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是_____________ (用离子符号表示)。

(1)以上9种元素中金属性最强的元素是
(2)元素的非金属性:M
(3)R的最高价氧化物对应水化物的化学式是
(4)F、G两元素形成的淡黄色固体物质的电子式为
(5)表中M、R、N元素可形成与Ar具有相同电子层结构的简单离子,这些离子的半径由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是5种元素的相关信息,W、X都位于第三周期。
(1)Q在周期表中的位置是__ 。
(2)W的最高价氧化物对应的水化物的化学式是___ 。
(3)X单质与水反应的离子方程式是__ 。
(4)金属性Y强于X,用原子结构解释原因:__ ,失电子能力Y大于X,金属性Y强于X。
(5)下列对于Z及其化合物的推断中,正确的是__ (填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
| 元素 | 信息 |
| Q | 地壳中含量最高的元素 |
| W | 最高化合价为+7价 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)火焰呈紫色 |
| Z | 原子结构示意图为: |
(2)W的最高价氧化物对应的水化物的化学式是
(3)X单质与水反应的离子方程式是
(4)金属性Y强于X,用原子结构解释原因:
(5)下列对于Z及其化合物的推断中,正确的是
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属钼在工业和国防建设中有重要的作用,其化合物钼酸钠晶体(Na2MoO4•10H2O)可制造金属缓蚀剂。由钼精矿(主要成分为MoS2,含有少量不反应的杂质)制备钼及钼酸钠晶体的工艺流程如图。回答下列问题:

(1)S位于元素周期表中_____ 区。
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,图1为焙烧时各炉层固体物料的物质的量百分数(φ)。

①“多层逆流焙烧”的优点是______ (任答一点),x=______ 。
②某些生产工艺在焙烧时加入CaCO3会更环保,其原因是______ (用化学方程式表示)。
(3)写出碱浸时发生反应的离子方程式:______ 。
(4)操作3为______ ,本流程中,金属钼的冶炼方法为_____ (填字母)。
a.热还原法 b.热分解法 c.电解法 d.物理方法
(5)已知钼酸钠的溶解度曲线如图2所示,要获得钼酸钠晶体Na2MoO4•10H2O的操作2为______ 、______ 、过滤、洗涤、烘干。


(1)S位于元素周期表中
(2)焙烧过程中采用“多层逆流(空气从炉底进入,钼精矿经粉碎后从炉顶进入)焙烧”,图1为焙烧时各炉层固体物料的物质的量百分数(φ)。

①“多层逆流焙烧”的优点是
②某些生产工艺在焙烧时加入CaCO3会更环保,其原因是
(3)写出碱浸时发生反应的离子方程式:
(4)操作3为
a.热还原法 b.热分解法 c.电解法 d.物理方法
(5)已知钼酸钠的溶解度曲线如图2所示,要获得钼酸钠晶体Na2MoO4•10H2O的操作2为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】随原子序数的递增,八种短周期元素原子半径的相对大小、最高正价或最低负价的变化如图所示,根据判断出的元素回答问题:

(1)g在元素周期表中的位置是___________ 。
(2)比较d、e常见离子的半径的大小(用化学式表示、下同):___________ >___________ ,比较g、h的最高价氧化物对应的水化物的酸性强弱:___________ >___________ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:___________ 。
(4)f的单质能在y的最高价氧化物中燃烧,写出该反应的化学方程式:___________ 。

(1)g在元素周期表中的位置是
(2)比较d、e常见离子的半径的大小(用化学式表示、下同):
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)f的单质能在y的最高价氧化物中燃烧,写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。钛铁矿主要成分为FeTiO3(含有少量MgO、SiO2等杂质),Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制备,工艺流程如下:
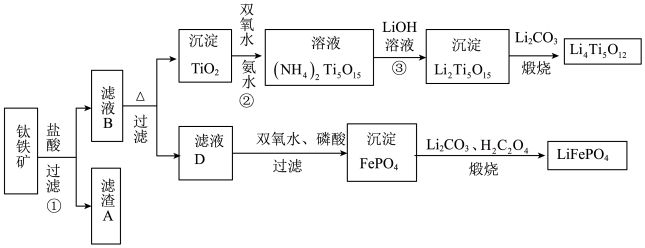
(1)Ti位于元素周期表中的位置为________ 。钛铁矿在预处理时需要进行粉碎,其原因是_______ 。
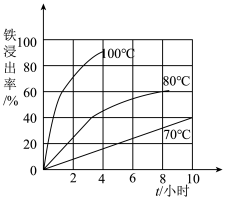
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是_________ 。
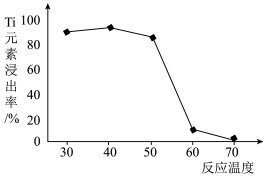
(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是___________ 。
(4)写出由滤液D生成FePO4的离子方程式____________________________________ 。
(5)由流程图可知FePO4制备LiFePO4的化学方程式是_________________________ 。

(1)Ti位于元素周期表中的位置为
(2)过程①中,铁的浸出率结果如图所示。由图可知,当铁的浸出率为80%时,所采用的实验条件是

(3)过程②中固体TiO2与双氧水、氨水反应转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示,反应温度过高时,Ti元素浸出率下降的原因是

(4)写出由滤液D生成FePO4的离子方程式
(5)由流程图可知FePO4制备LiFePO4的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】某一元素具有如下性质,请你推测该元素在元素周期表中的位置。
(1)其最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液。
(2)其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应。
(3)1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。_____
(1)其最高价氧化物既可以溶于浓盐酸,也可以溶于NaOH溶液。
(2)其最高价氧化物对应的水化物既可以与酸反应,也可以与碱反应。
(3)1mol该元素最高价氧化物对应的水化物在与盐酸反应时,最多能消耗4molHCl。
您最近一年使用:0次



