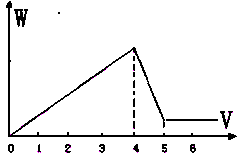
等体积的NaOH和AlCl3两种溶液混合后,沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则AlCl3和NaOH两种溶液物质的量浓度之比是
①7∶2 ②2∶3 ③3∶2 ④2∶7
①7∶2 ②2∶3 ③3∶2 ④2∶7
| A.①③ | B.②④ | C.①④ | D.③④ |
更新时间:2021-03-04 08:02:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中含铝元素的质量与溶液中含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是
①1∶3 ②2∶3 ③1∶4 ④2∶7 ⑤任意比
①1∶3 ②2∶3 ③1∶4 ④2∶7 ⑤任意比
| A.①④ | B.⑤ | C.②③ | D.②④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列各项操作中,不会发生“先产生沉淀,然后沉淀又溶解”现象的是
① 向饱和碳酸钠溶液中通入过量的CO2;
② 向NaAlO2溶液中逐滴加入过量的稀盐酸,
③ 向AlC13溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硝酸银溶液中逐滴加入过量的盐酸
① 向饱和碳酸钠溶液中通入过量的CO2;
② 向NaAlO2溶液中逐滴加入过量的稀盐酸,
③ 向AlC13溶液中逐滴加入过量的稀氢氧化钠溶液;
④向硝酸银溶液中逐滴加入过量的盐酸
| A.①② | B.①④ | C.①③ | D.②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】25℃时,某实验小组同学向铝与过量稀盐酸反应后的残留液中滴加氢氧化钠溶液,并用pH传感器测得pH变化曲线如图所示(B点开始出现白色沉淀)。下列说法错误的是( )


| A.A 点前发生中和反应 |
| B.BC 段沉淀质量逐渐增加 |
| C.D 点后的反应为:Al(OH)3+OH﹣=AlO2﹣+2H2O |
| D.E 点溶液中溶质主要是NaAlO2和NaOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某实验小组对一含有Al3+的未知溶液进行分析,经定量分析后,绘出沉淀的物质的量与滴入氢氧化钠体积的关系图:
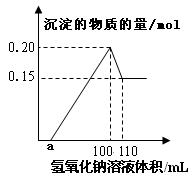
则下列说法中错误的是

则下列说法中错误的是
| A.该未知溶液中至少含有3种阳离子 |
| B.滴加的NaOH溶液的物质的量浓度为5mol/L |
| C.若另一种离子为二价阳离子,则a="10" |
| D.若将最终沉淀过滤、洗涤、灼烧,其质量一定为6g |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列反应的离子方程式书写正确的是
| A.将少量氯气通入FeI2溶液中:Cl2+2Fe2+=2Cl-+2Fe3+ |
B.一小块金属铜投入稀硝酸中:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
C.往AlCl3溶液中加入过量NaOH溶液:Al3++4OH-=AlO +2H2O +2H2O |
D.酸性KMnO4溶液遇H2C2O4而褪色:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
您最近一年使用:0次