(1)当光束通过下列物质时,会出现丁达尔效应的是_______ 。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来_______
②分离柴油和水的混合物_______
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物_______
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是_______ 。
Ⅱ、以上物质中属于非电解质的是_______ 。
Ⅲ、请写出①在水溶液中的电离方程式_______ 。
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有_______ (写仪器名称)。
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为_______ mL。
①Fe(OH)3胶体,②水,③蔗糖溶液,④Ca(OH)2悬浊液
(2)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(3)下列各组混合物的分离或提纯选用哪种方法最合适?(把选用的标号填入括号内)
A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏 H.升华
①把溴水中的溴提取出来
②分离柴油和水的混合物
③分离四氯化碳(沸点为 76.75℃)和甲苯(沸点为 110.6℃)的混合物
(4)现有以下物质:①Ba(OH)2晶体,②盐酸,③冰醋酸(固态醋酸),④石墨,⑤酒精(C2H5OH),请回答下列问题(填序号):
Ⅰ、以上物质中属于电解质的是
Ⅱ、以上物质中属于非电解质的是
Ⅲ、请写出①在水溶液中的电离方程式
(5)某学校实验室有一瓶浓硫酸试剂,标签上标有密度1.84g·cm-3,质量分数98%,现用该浓硫酸配制480 mL 1mol·L﹣1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒。请回答下列问题:
a.配制稀硫酸时,除了上述仪器,还缺少的仪器有
b.经计算,配制480mL 1mol·L-1的稀硫酸,需要用量筒量取上述浓硫酸的体积为
更新时间:2021-03-06 11:45:34
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】现有9种物质:①Na;②盐酸;③ ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦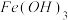 胶体;⑧NaOH;⑨
胶体;⑧NaOH;⑨
(1)属于电解质的是_______ (用序号填空,下同);属于非电解质的是_______ ;属于碱性氧化物的是_______ 。
(2)实验室中少量①通常保存在_______ 中;④在工业上大量用于_______ (写出一种用途即可)。
(3)⑧物质的水溶液常常用来吸收④,请写出此反应的化学方程式_______ 。
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式_______ 。
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生_______ ,随后沉淀溶解,得到黄色溶液,原因_______ (用离子方程式表示)。
 ;④
;④ ;⑤空气;⑥
;⑤空气;⑥ ;⑦
;⑦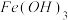 胶体;⑧NaOH;⑨
胶体;⑧NaOH;⑨
(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)⑧物质的水溶液常常用来吸收④,请写出此反应的化学方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有下列八种物质:
①铝 ②酒精 ③ ④稀
④稀 ⑤
⑤ 固体 ⑥氢氧化铁固体 ⑦氨水 ⑧熔融氢氧化钠
固体 ⑥氢氧化铁固体 ⑦氨水 ⑧熔融氢氧化钠
(1)上述物质中能导电的有_______ (填序号)。
(2)向⑥的胶体中逐渐滴加④的溶液,看到的现象是_______ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为: ,则该反应的化学方程式为
,则该反应的化学方程式为_______ 。
(4)保存硫酸的试剂瓶上最适合贴上的一个标签是_______ (填字母代号)。

(5)书写下列反应的离子方程式:
①将铝投入 溶液中:
溶液中:_______ 。
②醋酸溶液和 溶液混合:
溶液混合:_______ 。
①铝 ②酒精 ③
 ④稀
④稀 ⑤
⑤ 固体 ⑥氢氧化铁固体 ⑦氨水 ⑧熔融氢氧化钠
固体 ⑥氢氧化铁固体 ⑦氨水 ⑧熔融氢氧化钠(1)上述物质中能导电的有
(2)向⑥的胶体中逐渐滴加④的溶液,看到的现象是
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:
 ,则该反应的化学方程式为
,则该反应的化学方程式为(4)保存硫酸的试剂瓶上最适合贴上的一个标签是

(5)书写下列反应的离子方程式:
①将铝投入
 溶液中:
溶液中:②醋酸溶液和
 溶液混合:
溶液混合:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空:
Ⅰ.现有7种物质:①Na、②FeCl3溶液、③CH3COOH、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl晶体。
(1)能导电的电解质有___ (填序号)。
(2)属于盐的物质有质有___ (填序号)。
(3)区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是___ 。
(4)FeCl3在溶液中的电离方程式是___ 。
Ⅱ.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量NaOH溶液吸收含SO2的尾气,该反应的离子方程式是___ 。
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为___ 。
Ⅰ.现有7种物质:①Na、②FeCl3溶液、③CH3COOH、④熔融的KNO3、⑤CO2、⑥Fe(OH)3胶体、⑦NH4Cl晶体。
(1)能导电的电解质有
(2)属于盐的物质有质有
(3)区分Fe(OH)3胶体和FeCl3溶液的常用物理方法是
(4)FeCl3在溶液中的电离方程式是
Ⅱ.依据信息书写下列反应的离子方程式。
(5)SO2是一种酸性氧化物,可用过量NaOH溶液吸收含SO2的尾气,该反应的离子方程式是
(6)市场上出售的抗酸药复方氢氧化铝片主要用于缓解人体胃酸(主要成分是盐酸)过多,相关反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】分类法是一种重要的学习方法。
(1)请按要求对下列物质进行分类:①铝片②熔融的硝酸钾③氯气④硫酸钡固体⑤氯化氢气体⑥澄清的石灰水⑦无水乙醇⑧氧化钠固体⑨二氧化碳气体,其中能导电的是_______ ,属于电解质的是_______ (均填序号)。
(2)下列4组物质中均有一种物质的类别与其它三种不同,请分别填出其化学式。
甲:CaO、Na2O、CO2、CuO
乙:NaOH、Ca(OH)2、KHCO3、KOH
丙:C、Fe、Cu、Zn
丁:CO、H2、SO2、HCl
甲_______ ;乙_______ ;丙_______ ;丁_______ 。
(1)请按要求对下列物质进行分类:①铝片②熔融的硝酸钾③氯气④硫酸钡固体⑤氯化氢气体⑥澄清的石灰水⑦无水乙醇⑧氧化钠固体⑨二氧化碳气体,其中能导电的是
(2)下列4组物质中均有一种物质的类别与其它三种不同,请分别填出其化学式。
甲:CaO、Na2O、CO2、CuO
乙:NaOH、Ca(OH)2、KHCO3、KOH
丙:C、Fe、Cu、Zn
丁:CO、H2、SO2、HCl
甲
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】填空。
(1)按要求写出方程式:
①NaHCO3(电离方程式):_______ 。
②二氧化碳通入足量氢氧化钠溶液中(离子方程式):_______ 。
(2)以下为中学化学中常见的几种物质:
①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水
其中属于电解质的有_______ (填序号,下同),属于非电解质的有_______ 。
(3)食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。“石灰干燥剂”的主要成分生石灰是_______ ,“生石灰”所属的物质类型是_______ (填字母)。
a.金属氧化物 b.碱性氧化物 c.碱 d.盐 f.化合物
(1)按要求写出方程式:
①NaHCO3(电离方程式):
②二氧化碳通入足量氢氧化钠溶液中(离子方程式):
(2)以下为中学化学中常见的几种物质:
①二氧化碳②熔融KCl③NaHSO4固体④铜⑤稀硫酸⑥澄清石灰水
其中属于电解质的有
(3)食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。“石灰干燥剂”的主要成分生石灰是
a.金属氧化物 b.碱性氧化物 c.碱 d.盐 f.化合物
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有下列物质:①铜②CO2③稀硝酸④CH4⑤氯化铁溶液⑥氢氧化铁胶体⑦氨水⑧NH3⑨NaHSO4固体⑩NaCO3•10H2O晶体⑪BaSO4⑫酒精溶液
(1)上述物质可导电的有___________ (填编号,下同);
(2)属于电解质的有___________ ,属于非电解质的有___________ 。
(3)将⑨溶于水配成溶液,其电离方程式为___________ 。
(4)下列关于⑤和⑥的说法正确的是___________ (填字母序号)。
a.都不稳定,密封静置会产生沉淀 b.⑥能产生丁达尔效应,而⑤不能
c.分散质粒子都可以通过滤纸 d.加入盐酸都会先产生沉淀,后溶解
(5)向Fe(OH)3胶体中加入Na2SO4饱和溶液,主要由于___________ (填离子符号)的作用,使胶体形成了沉淀,这个过程叫作___________ 。
(1)上述物质可导电的有
(2)属于电解质的有
(3)将⑨溶于水配成溶液,其电离方程式为
(4)下列关于⑤和⑥的说法正确的是
a.都不稳定,密封静置会产生沉淀 b.⑥能产生丁达尔效应,而⑤不能
c.分散质粒子都可以通过滤纸 d.加入盐酸都会先产生沉淀,后溶解
(5)向Fe(OH)3胶体中加入Na2SO4饱和溶液,主要由于
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】配制1 mol/L的CuSO4溶液500mL,需胆矾_______ g;把称好的胆矾放入_______ 里,用适量蒸馏水使它完全溶解,把制得的溶液小心地注入容量瓶中,用适量蒸馏水洗涤烧杯2~3次,把每次的洗涤液都注入容量瓶中,然后慢慢地加入蒸馏水到液面距刻线_______ 处,改用_______ 滴加蒸馏水到液面与刻线相切;把瓶塞盖好,颠倒摇匀。从配好的溶液中取出10mL,此时溶液的物质的量浓度为_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某化学镀镍试剂的化学式为MxNi(SO4)y(M为+1价阳离子,Ni为+2价,x、y均为正整数)。为测定该镀镍试剂的组成,进行如下实验:
Ⅰ.称量28.7 g镀镍试剂,配制100 mL溶液A
Ⅱ.准确量取10.00 mL溶液A,用0.40 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00 mL
Ⅲ.另取10.00 mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66 g
(1)配制100 mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要___________
(2)该镀镍试剂的化学式为___________
Ⅰ.称量28.7 g镀镍试剂,配制100 mL溶液A
Ⅱ.准确量取10.00 mL溶液A,用0.40 mol·L-1的EDTA(Na2H2Y)标准溶液滴定其中的Ni2+(离子方程式为Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00 mL
Ⅲ.另取10.00 mL溶液A,加入足量的BaCl2溶液,得到白色沉淀4.66 g
(1)配制100 mL镀镍试剂时,需要的仪器除药匙、托盘天平、玻璃棒、烧杯、量筒、胶头滴管外,还需要
(2)该镀镍试剂的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】如图是实验室中浓硫酸试剂瓶标签上的数据。
(1)该浓硫酸的物质的量浓度为_______ 。
(2)某学生实验时,需要用到240mL 1.0mol•L﹣1的稀硫酸,欲用该浓硫酸和蒸馏水配制该稀硫酸。试回答:
①该稀硫酸溶液应在_______ mL _______ (填仪器名称)中配制。
②定容时,应改用_______ (填仪器名称)加水,使溶液凹液面恰好与刻度线相切。
③该实验中多次用到玻璃棒,其作用分别有_______ 和_______ 。
④配制时,量筒量取该浓硫酸的体积应为_______ mL(保留 1位小数)。
(3)配制过程中,下列实验操作会导致所配稀硫酸物质的量浓度偏大的是_______ (填选项前字母)。
A.定容后经振荡、摇匀、静置,发现液面低于刻度线,再滴加蒸馏水至刻度线
B.用量筒量取浓硫酸时仰视刻度线
C.溶液没有冷却至室温就注入容量瓶定容
(4)取上述配制的稀硫酸时,下列物理量中不随所取体积的多少而变化的是_______(填选项前字母)。
硫酸 分子式:H2SO4 相对分子质量:98 密度:1.84 g•mL-1 质量分数:98% |
(2)某学生实验时,需要用到240mL 1.0mol•L﹣1的稀硫酸,欲用该浓硫酸和蒸馏水配制该稀硫酸。试回答:
①该稀硫酸溶液应在
②定容时,应改用
③该实验中多次用到玻璃棒,其作用分别有
④配制时,量筒量取该浓硫酸的体积应为
(3)配制过程中,下列实验操作会导致所配稀硫酸物质的量浓度偏大的是
A.定容后经振荡、摇匀、静置,发现液面低于刻度线,再滴加蒸馏水至刻度线
B.用量筒量取浓硫酸时仰视刻度线
C.溶液没有冷却至室温就注入容量瓶定容
(4)取上述配制的稀硫酸时,下列物理量中不随所取体积的多少而变化的是_______(填选项前字母)。
| A.溶液的浓度 | B.溶液中SO 的数目 的数目 |
| C.溶液中H2SO4的物质的量 | D.溶液的密度 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】2017年10月23日,十九大新闻中心在梅地亚举行以“践行绿色发展理念,建设美丽中国”为主题的记者招待会,聚焦环保话题。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(1)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是________ 。
A 建在西部干旱区可以脱贫致富
B 应建在水资源丰富和交通方便且远离城市的郊区
C 企业有权自主选择厂址
D 不宜建在人稠密的居民区
(2)某化工厂排放的污水中含有 、
、 、
、 、
、 四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。



在能制得纯铜的方案中,哪一步操作会导致环境污染?_______ 。应增加什么措施防止污染?_______ 。
(1)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是
A 建在西部干旱区可以脱贫致富
B 应建在水资源丰富和交通方便且远离城市的郊区
C 企业有权自主选择厂址
D 不宜建在人稠密的居民区
(2)某化工厂排放的污水中含有
 、
、 、
、 、
、 四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。


在能制得纯铜的方案中,哪一步操作会导致环境污染?
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】Na2CO3和NaHCO3是重要的化工原料,请回答:
(1)两物质的水溶液分别与足量盐酸混合,反应的化学方程式分别为____ 、_____ 。
(2)除去Na2CO3固体中少量NaHCO3的方法是_____ ,反应的化学方程式是_____ 。
(3)除去NaHCO3溶液中少量的Na2CO3的方法是____ 。反应的化学方程式是_____ 。
(4)除去NaCl溶液中的Na2CO3,可加入适量的____ ,反应的离子方程式是_____ 。
(5)除去NaCl溶液中的MgCl2,可加入适量的____ ,反应的离子方程式是_____ 。
(1)两物质的水溶液分别与足量盐酸混合,反应的化学方程式分别为
(2)除去Na2CO3固体中少量NaHCO3的方法是
(3)除去NaHCO3溶液中少量的Na2CO3的方法是
(4)除去NaCl溶液中的Na2CO3,可加入适量的
(5)除去NaCl溶液中的MgCl2,可加入适量的
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】除去下列物质中混有的少量杂质,把适当的试剂、操作方法的序号写在相应的横线上。
A.加适量盐酸、过滤
B.加适量水、过滤、蒸发
C.加适量水、过滤
D.加热(高温或灼烧)
E.加适量盐酸、蒸发
F.冷却热的饱和溶液、结晶
(1)氯化钾粉末中混有碳酸钾_______________ ;
(2)氧化钙中混有少量的碳酸钙______________ ;
(3)氯化钠中混有少量的木炭粉_____________________ ;
(4)硝酸钾中混有少量的食盐______________________ 。
A.加适量盐酸、过滤
B.加适量水、过滤、蒸发
C.加适量水、过滤
D.加热(高温或灼烧)
E.加适量盐酸、蒸发
F.冷却热的饱和溶液、结晶
(1)氯化钾粉末中混有碳酸钾
(2)氧化钙中混有少量的碳酸钙
(3)氯化钠中混有少量的木炭粉
(4)硝酸钾中混有少量的食盐
您最近一年使用:0次



