“太阳水”电池装置如图所示,该电池由三个电极组成,其中a为TiO2电极,b为Pt电极,c为WO3电极,电解质溶液为pH=3的Li2SO4-H2SO4溶液。锂离子交换膜将电池分为A、B两个区,A区与大气相通,B区为封闭体系并有N2保护。下列关于该电池的说法不正确的是


| A.利用该装置,无法实现太阳能向电能转化 |
| B.若用导线连接a、c,则a为负极,该电极附近pH减小 |
| C.若用导线连接a、c,则c电极的电极反应式为WO3+xe-+xH+=HxWO3 |
| D.若用导线连接b、c,则b电极的电极反应式为O2+4H++4e-=2H2O |
更新时间:2021-03-22 12:37:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】小明做完铜锌原电池(稀硫酸为电解质溶液)的实验后,得出的下列结论和认识中正确的是
| A.构成原电池正极和负极的材料必须是两种金属 |
| B.由铜、锌作电极与稀硫酸溶液组成的原电池中铜是负极 |
| C.电子通过稀硫酸溶液由锌流向铜,通过溶液时被氢离子得到而放出氢气 |
| D.铜锌原电池工作时,溶液的酸性降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】锌—空气电池(原理如右图)适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时下列说法正确的是


| A.氧气在石墨电极上发生氧化反应 |
| B.该电池的负极反应为Zn+H2O-2e-=ZnO+2H+ |
| C.该电池放电时OH-向Zn电极移动 |
| D.若Zn电极消耗6.5 g,外电路转移0.1 mol e- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】铁碳微电解技术是处理酸性废水的一种工艺,装置如下图所示。若上端口打开,并鼓入空气,可得到强氧化性中间体羟基自由基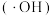 ;若上端口关闭,可得到强还原性中间体氢原子
;若上端口关闭,可得到强还原性中间体氢原子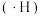 。下列说法正确的是
。下列说法正确的是
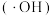 ;若上端口关闭,可得到强还原性中间体氢原子
;若上端口关闭,可得到强还原性中间体氢原子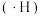 。下列说法正确的是
。下列说法正确的是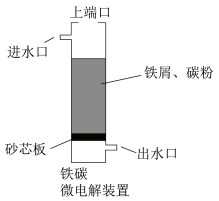
A.无论上端口是关闭还是打开,正极反应式均为: |
B. 完全转化为羟基自由基 完全转化为羟基自由基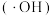 时转移了 时转移了 电子 电子 |
| C.若处理含酚类的酸性废水,则上端口应关闭 |
D.若处理含 的酸性废水,则上端口应打开并鼓入空气 的酸性废水,则上端口应打开并鼓入空气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】卤族元素单质及其化合物应用广泛。氟在自然界主要存在于萤石( )中,
)中, 与浓
与浓 反应可制取HF;氯、溴主要存在于海水中,工业常通过电解NaCl饱和溶液制备
反应可制取HF;氯、溴主要存在于海水中,工业常通过电解NaCl饱和溶液制备 ,
, 可用于制取漂白粉。卤水中
可用于制取漂白粉。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收;BrCl能发生水解反应。
溶液吸收;BrCl能发生水解反应。 易升华,一种
易升华,一种 二次电池正极界面反应机理如图所示。
二次电池正极界面反应机理如图所示。
 )中,
)中, 与浓
与浓 反应可制取HF;氯、溴主要存在于海水中,工业常通过电解NaCl饱和溶液制备
反应可制取HF;氯、溴主要存在于海水中,工业常通过电解NaCl饱和溶液制备 ,
, 可用于制取漂白粉。卤水中
可用于制取漂白粉。卤水中 可通过
可通过 氧化、
氧化、 溶液吸收;BrCl能发生水解反应。
溶液吸收;BrCl能发生水解反应。 易升华,一种
易升华,一种 二次电池正极界面反应机理如图所示。
二次电池正极界面反应机理如图所示。
A. 电池正极放电时的电极反应有: 电池正极放电时的电极反应有: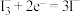 |
B.电解饱和NaCl溶液: |
C.BrCl与 反应: 反应: |
D. 用 用 溶液吸收: 溶液吸收: |
您最近一年使用:0次



