现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已知A、D位于同一主族,D是短周期中原子半径最大的元素。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是___________ (用元素符号填写);
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写);
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有___________ ;
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是___________ (填字母序号)。
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G的最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1:1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a.G单质与Na2S溶液反应溶液变浑浊
b.F氢化物的酸性比G的氢化物酸性弱
c.G和F两元素的简单氢化物受热分解,前者的分解温度高
更新时间:2021-03-31 23:21:20
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答问题。
(1)⑦、⑧分别生成的气态氢化物中,较稳定的是___ (填化学式)。
(2)②的最高价氧化物的空间结构为____ (用文字描述)。
(3)①和⑤可形成含离子键的化合物,写出该化合物的电子式____ 。
(4)③的简单气态氢化物在催化剂条件下与④的单质发生反应的化学方程式是___ 。
(5)写出⑥的氧化物与⑤的最高价氧化物的水化物反应的离子方程式___ 。
(6)已知硒(Se)的原子序数为34,且与④同主族,硒在周期表中的位置是__ ;其最高价氧化物对应水化物的化学式是___ 。
| 族 周期 | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)②的最高价氧化物的空间结构为
(3)①和⑤可形成含离子键的化合物,写出该化合物的电子式
(4)③的简单气态氢化物在催化剂条件下与④的单质发生反应的化学方程式是
(5)写出⑥的氧化物与⑤的最高价氧化物的水化物反应的离子方程式
(6)已知硒(Se)的原子序数为34,且与④同主族,硒在周期表中的位置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图l所示,物质A与物质B之间的反应不在溶液中进行。
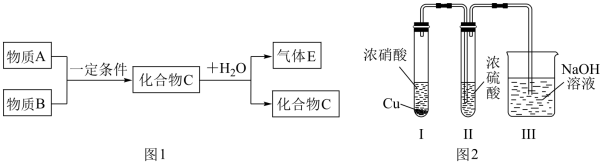
请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是__________________ ;(填化学式)
②化合物C的电子式为__________ ;化合物D中所含化学键的类型是_________ 。
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为_________________ (填化学式)。
②化合物C与水反应时的化学方程式为________________ ,其氧化剂与还原剂的质量比为_______________ 。
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:_________________________ 。
II.试管中观察到_______________________ 的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2。Ⅲ.装置Ⅲ的用途是:____________________________

请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是
②化合物C的电子式为
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为
②化合物C与水反应时的化学方程式为
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:
II.试管中观察到
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,C原子最外层电子数是电子层数的3倍,E和C同主族,A、B组成的气态化合物的水溶液呈碱性,D与C能按原子个数比为1∶1或2∶1形成离子化合物。
(1)画出D的原子结构示意图____ 。
(2)A与C形成的化合物中,原子个数比为2∶1的化合物的结构式为___ ,此化合物与A的单质含有化学键的区别为___ 。
(3)D与C按原子个数比为1∶1形成化合物的电子式是___ ,含有的化学键为____ 。
(4)C、E所形成氢化物的沸点由高到低的顺序是___ >___ (填化学式),原因是___ 。
(1)画出D的原子结构示意图
(2)A与C形成的化合物中,原子个数比为2∶1的化合物的结构式为
(3)D与C按原子个数比为1∶1形成化合物的电子式是
(4)C、E所形成氢化物的沸点由高到低的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知X、Y、Z、W是短周期元素中的四种非金属元素,它们的原子序数依次增大。X元素的原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)Z分子的电子式为:_______ ;Y的单质有多种,其中可以导电的一种是:_____ 。
(2)在一定条件下,由x单质与z单质反应生成1molE放出的热量为46.2kJ,写出该反应的热化学方程式:________ ;E在催化剂存在的条件下,可用于还原汽车尾气中的___________ ,以减少对大气的污染。
(3)仅由X、Z、W三种元素组成的某种盐是一种速效化肥,但长期施用会使土壤酸化,有关的离子方程式为________________ 。
(4)工业上可用E的浓溶液来检验输送氯气的管道是否漏气,若漏气时可观察到大量白烟,同时有单质z生成,写出相应的化学方程式:____ 。该反应中被氧化的E与参与反应的E的质量之比为_______________________ 。
(1)Z分子的电子式为:
(2)在一定条件下,由x单质与z单质反应生成1molE放出的热量为46.2kJ,写出该反应的热化学方程式:
(3)仅由X、Z、W三种元素组成的某种盐是一种速效化肥,但长期施用会使土壤酸化,有关的离子方程式为
(4)工业上可用E的浓溶液来检验输送氯气的管道是否漏气,若漏气时可观察到大量白烟,同时有单质z生成,写出相应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D四种元素,其中A和B原子都有1个未成对电子,A+比B-少一个电子层。B原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子,其气态氢化物的水溶液的pH在同族氢化物中最大,D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D 40%,且其核内质子数等于中子数,据此判断:
(1)A是_______ ,B是_______ ,C是_______ ,D是_______ 。(填元素名称)
(2)B-的电子排布式_______ ,A+ 的结构示意图_______ ,D原子的价层电子排布图_______ 。
(3)题中元素“C”的原子中有_______ 种不同运动状态的电子,能量最高的是_______ 电子,其原子轨道呈_______ 状。
(4)用电子式表示化合物AB的形成过程_______ 。
(1)A是
(2)B-的电子排布式
(3)题中元素“C”的原子中有
(4)用电子式表示化合物AB的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E五种前四周期元素,原子序数依次增大。A为自然界中形成化合物种类最多的元素;C为地壳中含量最多的元素;D与A为同主族元素,且原子的质子数相差8;E是日常生活中用途最广、用量最大的金属元素。请回答下列问题:
(1)A的一种同位素具有放射性,在考古学上常用来测定文物的历史年代,写出该核素的符号:___ 。
(2)B的简单气态氢化物的电子式为___ ,若用玻璃棒蘸取浓盐酸靠近盛满该气体的集气瓶瓶口,则观察到的现象为___ 。
(3)C元素有16C、17C、18C三种核素,这三种核素的质子数之和为__ 。
(4)D元素在元素周期表中的位置为__ ,写出工业上制备含少量杂质的D单质的化学方程式: ___ 。
(5)写出少量E的单质与B的最高价氧化物对应的水化物的稀溶液反应的离子方程式:__ 。
(1)A的一种同位素具有放射性,在考古学上常用来测定文物的历史年代,写出该核素的符号:
(2)B的简单气态氢化物的电子式为
(3)C元素有16C、17C、18C三种核素,这三种核素的质子数之和为
(4)D元素在元素周期表中的位置为
(5)写出少量E的单质与B的最高价氧化物对应的水化物的稀溶液反应的离子方程式:
您最近一年使用:0次



