(1)最外层电子数为次外层电子数 的原子
的原子___________ ;(填元素符号,下同)
(2)根据下列微粒回答问题: H、
H、 H、
H、 H、
H、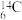 、
、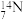 、
、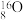 、35Cl2、37Cl2。以上8种微粒共有
、35Cl2、37Cl2。以上8种微粒共有___________ 种核素,互为同位素的___________ ,中子数相等的是___________ 。
(3)写出次氯酸结构式___________ 。
(4) H、
H、 H分别用H、D符号表示,HD则属于
H分别用H、D符号表示,HD则属于___________ (单质、化合物)。
 的原子
的原子(2)根据下列微粒回答问题:
 H、
H、 H、
H、 H、
H、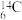 、
、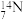 、
、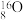 、35Cl2、37Cl2。以上8种微粒共有
、35Cl2、37Cl2。以上8种微粒共有(3)写出次氯酸结构式
(4)
 H、
H、 H分别用H、D符号表示,HD则属于
H分别用H、D符号表示,HD则属于
更新时间:2021-04-04 07:20:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是_______(填字母,下同)。
(2)下列说法正确的是_______。
(3)比较下列多电子原子的原子轨道的能量高低。
①1s,3d_______ ;
②3s,3p,3d_______ ;
③2p,3p,4p_______ ;
④3px,3py,3pz_______ 。
(4)符号3px所代表的含义是_______。
(1)在基态多电子原子中,关于核外电子能量的叙述错误的是_______(填字母,下同)。
| A.最易失去的电子能量最高 |
| B.同一个电子层上的不同能级上的原子轨道,能量大小不同 |
| C.p轨道电子能量一定高于s轨道电子能量 |
| D.在离核最近区域内运动的电子能量最低 |
| A.一个原子轨道上只能有1个电子 |
| B.处在同一原子轨道上的电子运动状态完全相同 |
| C.处在同一电子层上的电子(基态)能量一定相同 |
| D.处在同一能级中的电子(基态)能量一定相同 |
①1s,3d
②3s,3p,3d
③2p,3p,4p
④3px,3py,3pz
(4)符号3px所代表的含义是_______。
| A.3px轨道上有3个电子 |
| B.第3个电子层3px轨道有三个伸展方向 |
| C.px电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢(H),氧(O),硅(Si),钠(Na),镁(Mg),铝(Al),钾(K),钙(Ca),钛(Ti),铁(Fe),是地壳中含量前十的元素,请回答下列有关问题:
(1)依据原子核外电子排布,可将元素周期表分为_______ 个区,按此标准分类,上述十种元素可分为_______ (填数字)类,其中属于s区的元素有_______ (填元素符号)。
(2)地壳中含量最多的金属元素是_______ (填元素符号),其基态原子的电子排布式为_______ 。
(3)上述十种元素中,非金属元素的电负性从小到大的排列顺序为_______ (填元素符号);某激发态氢原子核外电子排布式为2p1,由该激发态跃迁到基态时,其原子发射光谱中能得到_______ 条谱线。
(1)依据原子核外电子排布,可将元素周期表分为
(2)地壳中含量最多的金属元素是
(3)上述十种元素中,非金属元素的电负性从小到大的排列顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1∶2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________ 种不同运动状态的电子,基态T原子有________ 种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为_______________ (用元素符号表示)。
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为_______________________ 。
(4)Z与R能形成化合物甲,1 mol甲中含________ mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为___________________ 。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为_________________ 。
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为___________ ,
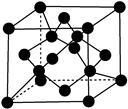
(7)X单质的晶胞如图所示,一个X晶胞中有________ 个X原子。
(1)Y原子核外共有
(2)X、Y、Z的第一电离能由小到大的顺序为
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为
(4)Z与R能形成化合物甲,1 mol甲中含
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为
(7)X单质的晶胞如图所示,一个X晶胞中有

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氢氟酸可用于半导体工业,也常用来蚀刻玻璃,其刻蚀反应原理如下:6HF + Na2SiO3 =2NaF + SiF4↑+ 3H2O完成下列填空:
(1)根据HF的________ (选填编号)大于H2O,可推断氟元素的非金属性强于氧元素。
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含___ 键的_____ 分子(均选填“极性”或“非极性”)。刻蚀反应中的三种元素可组成同时含离子键和共价键的化合物,该化合物的电子式为__________ 。
(3)Si原子核外电子有_____ 种不同能量的电子,其中最高能量的电子处于______ 轨道。
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是__________________________ 。
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3_____ HF(选填“>”或“<”)。浓度均为0.01 mol/L 的H2SO3和HF的1L混合溶液中,通入0.02 mol NH3充分反应后,SO32-、HSO3-、F-、NH4+浓度从大到小的顺序为:____________________ 。
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
(1)根据HF的
A.酸性 B.熔沸点 C.稳定性 D.键的极性
(2)SiF4与甲烷结构相似,SiF4是含
(3)Si原子核外电子有
(4)在相同条件下,Na2SiO3、CaSiO3分别与等浓度等体积的氢氟酸反应,两个反应原理相似,但前者的反应速率明显大于后者。原因是
(5)同浓度的H2SO3和HF两溶液的pH为:H2SO3
已知:H2SO3 Ki1=1.54×10-2 Ki2=1.02×10-7 HF Ki=6.8×10-4 NH3·H2O Ki=1.8×10-5
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜是人类最早发现的金属,也是人类广泛使用的一种金属。铜及其化合物在工业、工程技术和工艺上有着广泛的应用。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的____ 区。基态Al原子的L层电子排布图为___________ 。
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为_________ ,1mol乙酸分子中含有的σ键的数目为____________ 。
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为____ 。碳、硼、氮元素的电负性由大到小的顺序是_____ 。(用元素符号表示)
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为_________ 。
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为____ g·cm-3(设阿伏伽德罗常数的值为NA)。
(1)早期发现的天然准晶颗粒由Cu、Fe、Al三种金属元素组成。Fe元素位于元素周期表的
(2)Cu2O为半导体材料,可由乙醛(CH3CHO)和新制氢氧化铜反应得到,同时可得到乙酸。乙醛中碳原子的杂化轨道类型为
(3)制造单晶硅太阳能电池片时,一般掺杂微量的铜、碳、硼、氮等。一价铜离子的电子排布式为
(4)在络离子[Cu(NH3)4]2+中NH3的VSEPR模型为
(5)铜银合金晶体具有面心立方最密堆积结构。在晶胞中,Cu原子位于面心,Ag原子位于顶点,若该晶胞边长为r pm,则合金的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列物质中,互为同系物的有_______ ,互为同分异构体的有_______ ,互为同素异形体的有_______ ,属于同位素的有_______ ,是同一种物质的有_______ 。
①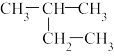 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④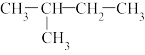 ;⑤
;⑤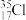 ;⑧红磷;⑦
;⑧红磷;⑦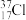 ;⑧
;⑧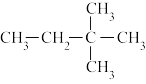
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为_______ ;
②发生1,4-加成反应的化学方程式为_______ 。
(1)下列物质中,互为同系物的有
①
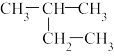 ②白磷;③2,3-二甲基丁烷;④
②白磷;③2,3-二甲基丁烷;④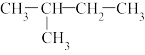 ;⑤
;⑤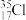 ;⑧红磷;⑦
;⑧红磷;⑦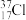 ;⑧
;⑧
(2)已知2-甲基-1,3-丁二烯可与溴水发生加成反应,按要求作答:
①发生1,2-加成所得有机产物的结构简式为
②发生1,4-加成反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)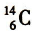 的放射性可用于考古断代,根据测定出土文物标本中
的放射性可用于考古断代,根据测定出土文物标本中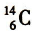 的含量,就可以推算出文物的年代。
的含量,就可以推算出文物的年代。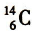 的中子数是
的中子数是______________ 。
(2)碘元素的一种核素12553I可用于治疗肿瘤。该核素的质子数为__________ ,中子数为_____________ ,质量数为____________ 。
(3)写出铝原子的原子结构示意图___________________ 。
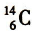 的放射性可用于考古断代,根据测定出土文物标本中
的放射性可用于考古断代,根据测定出土文物标本中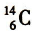 的含量,就可以推算出文物的年代。
的含量,就可以推算出文物的年代。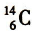 的中子数是
的中子数是(2)碘元素的一种核素12553I可用于治疗肿瘤。该核素的质子数为
(3)写出铝原子的原子结构示意图
您最近一年使用:0次

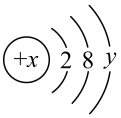
 、②
、②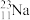 、③
、③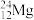 、④
、④ 。用①、②、③、④回答:
。用①、②、③、④回答: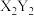 型化合物的是
型化合物的是

