科学家对碱金属的认识始终在不断的探索中前进。
(1)1807年,英国化学家戴维在无氧条件下电解熔融的KOH,最后成功地得到了银白色的金属钾,实验中产生的金属液珠一接触水就剧烈反应,放出___________ 色气体,向溶液中滴入紫色石蕊试液,显______ 色,因为_______ (写出化学方程式)。
(2)利用碱金属与水的反应可测定某碱金属的相对原子质量。如下图所示,仪器本身连同水和干燥管以及其内的无水氯化钙的总质量为480.0g。

现将1.4 g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质量为481.2 g。
①该金属元素的相对原子质量是___________ (结果保留两位小数),该元素可能是___________ 。
②若不用干燥管,测得的相对原子质量比实际相对原子质量___________ (填“偏大”“偏小”或“相等”),理由是___________ 。
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第___________ 周期___________ 族。
Ⅱ.关于铷的下列说法中正确的是___________ (填序号,下同)。
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳
③Rb2O2与水能剧烈反应并释放出O2 ④它是极强的还原剂
⑤RbOH的碱性比同浓度的NaOH弱
(1)1807年,英国化学家戴维在无氧条件下电解熔融的KOH,最后成功地得到了银白色的金属钾,实验中产生的金属液珠一接触水就剧烈反应,放出
(2)利用碱金属与水的反应可测定某碱金属的相对原子质量。如下图所示,仪器本身连同水和干燥管以及其内的无水氯化钙的总质量为480.0g。

现将1.4 g某碱金属单质投入水中,立即用带有干燥管的塞子塞紧瓶口,反应完毕后,测得整套仪器的总质量为481.2 g。
①该金属元素的相对原子质量是
②若不用干燥管,测得的相对原子质量比实际相对原子质量
(3)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
Ⅰ.铷位于元素周期表的第
Ⅱ.关于铷的下列说法中正确的是
①与水反应比钠更剧烈 ②Rb2O在空气中易吸收水和二氧化碳
③Rb2O2与水能剧烈反应并释放出O2 ④它是极强的还原剂
⑤RbOH的碱性比同浓度的NaOH弱
更新时间:2021-04-09 18:11:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】Li3N是一种储氢材料,可以用Li和N2在450℃反应制备。已知Li3N易水解,细粉状的Li3N在空气中加热可发生剧烈燃烧。下图是某实验小组设计的实验室制备少量Li3N的装置图。请回答下列问题:
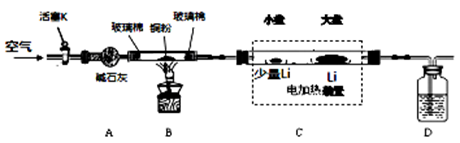
(1)B装置的作用是_________________ ,如果B装置中玻璃管两端没有玻璃棉可能造成的后果是____________________________ 。
(2)D装置中的试剂是_____________ ,作用是 __________________________ 。
(3)C装置的小盘中放有少量Li的作用是____________________________ 。
(4)实验步骤如下:安装好仪器,检查装置气密性,装入药品;_________________________ 。 (请按正确的顺序填入下列步骤的标号);拆除装置,取出产物。
①点燃B中酒精灯加热B中试管;
②打开活塞K;
③关闭电加热装置停,充分冷却;
④调节电加热装置控制温度为450℃;
⑤关闭活塞K;
⑥熄灭B中酒精灯;
(5)请你设计一个实验,用化学方法区分Li与Li3N,写出实验简要步骤及观察到的现象___________________________________ 。
(6)Li3N在H2中加热时可得到氨基锂(LiNH2),该反应在270℃可逆,所以Li3N可作为储氢材料,该反应的化学方程式为:___________________________________ 。

(1)B装置的作用是
(2)D装置中的试剂是
(3)C装置的小盘中放有少量Li的作用是
(4)实验步骤如下:安装好仪器,检查装置气密性,装入药品;
①点燃B中酒精灯加热B中试管;
②打开活塞K;
③关闭电加热装置停,充分冷却;
④调节电加热装置控制温度为450℃;
⑤关闭活塞K;
⑥熄灭B中酒精灯;
(5)请你设计一个实验,用化学方法区分Li与Li3N,写出实验简要步骤及观察到的现象
(6)Li3N在H2中加热时可得到氨基锂(LiNH2),该反应在270℃可逆,所以Li3N可作为储氢材料,该反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】黄色超氧化钾(KO2)可作为宇宙飞船舱的氧源。某学习小组设计以下实验探究KO2的性质,请回答相关问题:
I.探究KO2与水的反应
II. 探究KO2与SO2的反应

(4)正确的操作依次是___________________ 。
①打开K1通入N2 ,排尽装置内原气体后关闭
②拆卸装置至实验完成
③检查装置气密性,然后装入药品
④打开分液漏斗活塞K2
(5)A装置发生的化学方程式为____________________ 。
(6)用上述装置验证“KO2与SO2反应生成O2”还存在不足,你的改进措施是_____ 。
(7)改进后再实验,待KO2完全反应后,将装置C中固体加水溶解,配成50.00mL溶液,等分为M、N两份。
①向M溶液中加入足量的盐酸酸化的BaCl2溶液,充分反应后,将沉淀过滤、洗涤、__ ,称重为2.33g。
②将N溶液移入_______ (填仪器名称)中,用0.40mol/L酸性KMnO4溶液滴定,终点时消耗酸性KMnO4溶液20.00mL。
③依据上述现象和数据,请写出该实验总反应的化学方程式___________ 。
I.探究KO2与水的反应
| 实验操作 | 现象 | 结论与解释 |
| (1)取少量KO2固体于试管中,滴加少量水,将带火星的木条靠近试管口,反应结束后,溶液分成两份 | 快速产生气泡,木条复燃 | 产生的气体是 |
| (2)一份滴加酚酞试液 | 先变红后褪色 | 可能的产物是 |
| (3)另一份滴加FeCl3溶液 | 观察到 |
II. 探究KO2与SO2的反应

(4)正确的操作依次是
①打开K1通入N2 ,排尽装置内原气体后关闭
②拆卸装置至实验完成
③检查装置气密性,然后装入药品
④打开分液漏斗活塞K2
(5)A装置发生的化学方程式为
(6)用上述装置验证“KO2与SO2反应生成O2”还存在不足,你的改进措施是
(7)改进后再实验,待KO2完全反应后,将装置C中固体加水溶解,配成50.00mL溶液,等分为M、N两份。
①向M溶液中加入足量的盐酸酸化的BaCl2溶液,充分反应后,将沉淀过滤、洗涤、
②将N溶液移入
③依据上述现象和数据,请写出该实验总反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】将2.84 g化合物A的粉末(含两种元素)投入足量水中剧烈反应后微热至无气泡现象,标准状况下共收集到0.672 L能使带火星木条复燃的气体B,同时得到溶液C (溶液C中只含三种元素);所得C溶液能被含0.04 mol HCl的盐酸溶液恰好中和,取中和后溶液进行焰色反应,火焰显浅紫色(隔蓝色钻玻璃观察)。试回答:
(1)A的化学式是______________ 。
(2)A的粉末与水反应的离子方程式为_______________ 。
(3)某些特殊场合下A可用作供氧剂,供氧过程中呼吸面具里有酸式盐生成,写出相关反应的化学方程式________ 。
(1)A的化学式是
(2)A的粉末与水反应的离子方程式为
(3)某些特殊场合下A可用作供氧剂,供氧过程中呼吸面具里有酸式盐生成,写出相关反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】根据下图所示实验,回答问题:
(1)实验①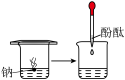 观察到的现象是
观察到的现象是________________________ 。实验②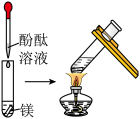 观察到的现象是
观察到的现象是________________________ 。
(2)实验③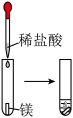 观察到的现象是
观察到的现象是________________________ 。实验④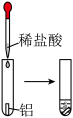 观察到的现象是
观察到的现象是________________________ 。
(3)由上述实验,你能得出的结论是________________________ 。
(4)请总结同周期元素金属性的变化规律__________ ,并用原子结构解释其原因_________ 。
(1)实验①
 观察到的现象是
观察到的现象是 观察到的现象是
观察到的现象是(2)实验③
 观察到的现象是
观察到的现象是 观察到的现象是
观察到的现象是(3)由上述实验,你能得出的结论是
(4)请总结同周期元素金属性的变化规律
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变化规律。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是__ 。
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:__ 。
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,__ 。
④补充实验证实了③中的分析。
a是__ ,b是__ 。
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是__ ,从原子结构角度说明理由__ 。
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是__ 。
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越___ (选填“强”或“弱”,下同),还原产物(氧化产物)的浓度越大,对应的氧化剂(还原剂)的氧化性(还原性)越___ 。
(1)浓盐酸与MnO2混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO2。
①反应的离子方程式是
②电极反应式:i.还原反应:MnO2+2e-+4H+=Mn2++2H2O;ii.氧化反应:
③根据电极反应式,分析A中仍存在盐酸和MnO2的原因。
i.随c(H+)降低或c(Mn2+)浓度升高,MnO2氧化性减弱。ii.随c(Cl-)降低,
④补充实验证实了③中的分析。
| 实验操作 | 试剂 | 产物检测 | |
| I | 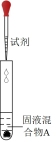 | 较浓H2SO4 | 有Cl2 |
| II | a | 有Cl2 | |
| III | a+b | 无Cl2 |
(2)利用c(H+)浓度对MnO2氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与MnO2反应所需的最低c(H+)最小的是
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高Br2的氧化性,将Mn2+氧化为MnO2。经实验证实了推测,该化合物是
(4)总结:物质氧化性和还原性随反应物和生成物浓度变化的一般规律是:氧化剂(还原剂)的浓度越大,其氧化性(还原性)越
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ、(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:____________ 与盐酸反应最剧烈,__________ 与盐酸反应最慢。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?_________ ;说明理由:___________ 。
Ⅱ、利用下图装置可以验证非金属性的变化规律。

(3)仪器A的名称为________ ,干燥管D的作用是_____________________ 。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为________ 、_______ 、______ ,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为____________________________ 。
(5)已知C中是硅酸钠溶液,如要证明非金属性:C > Si,请选择相应的试剂,则A中加________ 、B中加________ 。
Ⅰ、(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?
Ⅱ、利用下图装置可以验证非金属性的变化规律。

(3)仪器A的名称为
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为
(5)已知C中是硅酸钠溶液,如要证明非金属性:C > Si,请选择相应的试剂,则A中加
您最近一年使用:0次



