名校
解题方法
1 . 下列说法正确的是
| A.I2的升华破坏了共价键 |
| B.氢键是一种特殊的共价键 |
| C.Na2O2中的阴阳离子个数比为1:2 |
| D.卤素单质的熔点从F2到I2逐渐升高,则碱金属单质的熔点从Li到Cs也逐渐升高 |
您最近半年使用:0次
名校
解题方法
2 . 类推思想在化学学习和研究中经常被采用,但是类推出的结论是否正确最终要经过实验验证。下列类推的结论,正确的是
A.Cu和 反应生成 反应生成 ,则Cu和S反应生成CuS ,则Cu和S反应生成CuS |
B.Na在空气的燃烧产物为 ,则Li在空气中的燃烧产物为 ,则Li在空气中的燃烧产物为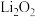 |
C. 的空间构型为正四面体形,则 的空间构型为正四面体形,则 的空间构型也是正四面体形 的空间构型也是正四面体形 |
D. 和NaOH反应生成 和NaOH反应生成 ,则相同条件下 ,则相同条件下 和NaOH反应生成 和NaOH反应生成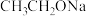 |
您最近半年使用:0次
3 . 碱金属锂和镁的性质相似,下列有关锂及其化合物的说法不正确的是
A. 易溶于水 易溶于水 | B. 在氧气中加热生成 在氧气中加热生成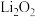 |
C. 的熔点比钠高 的熔点比钠高 | D. 受热分解,生成 受热分解,生成 和 和 |
您最近半年使用:0次
解题方法
4 . 下列物质久置于空气中不易变质的是
| A.NaOH固体 | B.氯水 | C.Na2SO4粉末 | D.漂白粉 |
您最近半年使用:0次
名校
5 . 同主族的元素既有相似性也有递变性,有关碱金属和卤素说法正确的是
| A.钠在氧气中加热生成Na2O2,可推测Li在氧气中加热也生成Li2O2 |
| B.还原性:K>Na,可推测Na不能把K从其化合物中置换出来 |
| C.非金属性:Cl>Br>I,可推测出还原性:HCl<HBr<HI |
| D.HF能和SiO2反应而HCl与SiO2不反应,可推测出酸性:HF>HCl |
您最近半年使用:0次
6 . 下列关于碱金属的叙述中,错误的是
| A.单质具有强还原性 | B.单质与水反应生成氢氧化物和氢气 |
| C.在自然界中没有游离态 | D.单质可从硫酸铜稀溶液中置换出铜 |
您最近半年使用:0次
23-24高一下·吉林·开学考试
名校
解题方法
7 . 第87号元素钫,它位于碱金属族,根据元素周期表结构及元素性质变化趋势,下列关于碱金属某些元素原子结构和性质的判断错误的是
①锂与水反应比钠剧烈
②金属单质都可以密封保存在煤油中
③钾的氧化物暴露在空气中吸收二氧化碳
④锂的阳离子的最外层电子数和钠离子的相同
⑤钫单质是强还原剂
⑥钫在化合物中显+1价
⑦钫单质的密度大于钠单质的密度
⑧钫单质有较高的熔点
①锂与水反应比钠剧烈
②金属单质都可以密封保存在煤油中
③钾的氧化物暴露在空气中吸收二氧化碳
④锂的阳离子的最外层电子数和钠离子的相同
⑤钫单质是强还原剂
⑥钫在化合物中显+1价
⑦钫单质的密度大于钠单质的密度
⑧钫单质有较高的熔点
| A.①②④⑧ | B.①②③⑦ | C.③④⑤⑧ | D.①③④⑥ |
您最近半年使用:0次
名校
8 . 关于碱金属元素与卤族元素,下列叙述正确的是
| A.碱金属与卤族元素单质的密度均随核电荷数的增大而增大 |
| B.碱金属与卤族元素单质的熔沸点均随核电荷数的增大而升高 |
| C.碱金属与卤族元素原子的半径大小均随核电荷数的增大而增大 |
| D.碱金属元素最高价氧化物对应水化物的碱性及卤族元素最高价氧化物对应水化物的酸性均随核电荷数的增大而增强 |
您最近半年使用:0次
9 . 在学习中,我们经常应用类推。下列左边正确,类推法应用于右边也正确的是
| A | 向FeCl2溶液中滴入氯水:2Fe2++Cl2=2Fe3++2Cl- | 向FeCl2溶液中滴入碘水:2Fe2++I2=2Fe3++2I- |
| B | 向澄清石灰水中通入少量CO2气体:Ca2++2OH-+CO2=CaCO3↓+H2O | 向澄清石灰水中通入少量SO2气体:Ca2++2OH-+SO2=CaSO3↓+H2O |
| C | 向Na2CO3溶液中滴入稀HNO3: +2H+=CO2↑+H2O +2H+=CO2↑+H2O | 向Na2SO3溶液中滴入稀HNO3: +2H+=SO2+H2O +2H+=SO2+H2O |
| D | Na在氧气中燃烧:2Na+O2=Na2O2 | Li在氧气中燃烧:2Li+O2=Li2O2 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024高三下·全国·专题练习
10 . 电池级碳酸锂是制造LiCoO2等锂离子电池必不可少的原材料。享誉“亚洲锂都”的宜春拥有亚洲储量最大的锂云母矿,以锂云母浸出液(含Li+、Fe3+、Mg2+、SO 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
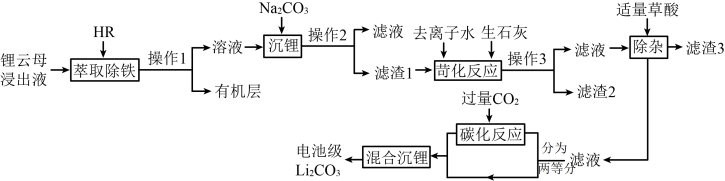
(1)“混合沉锂”的离子方程式为___________ 。
(2)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式___________ 。
 等)为原料制取电池级Li2CO3的工艺流程如图:
等)为原料制取电池级Li2CO3的工艺流程如图:
(1)“混合沉锂”的离子方程式为
(2)Li2CO3与Co3O4在空气中加热可以制备重要的电极材料钴酸锂(LiCoO2)。写出对应的化学方程式
您最近半年使用:0次



