解题方法
1 . 一种化合物的结构如图所示,Q、X、Y、Z、W为相邻两个短周期主族元素,原子序数依次增大,W元素的最外层电子数等于其电子总数的三分之一。下列说法正确的是
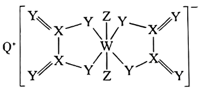

| A.通常所用的农药中含有Z、W等元素 |
| B.氢化物的沸点一定是Y>Z>X |
| C.由Q、Y、W形成的正盐只有一种 |
| D.Q的单质在空气中燃烧的产物具有强氧化性 |
您最近一年使用:0次
解题方法
2 . 钾、铷、铯在过量的氧气中燃烧均生成黄色的超氧化物(如KO2)。 下列说法不正确的是( )
| A.在450℃ 、15MPa 的压力下, Na 与 O2反应也能够得纯净的 NaO2,常温下Na2O2的稳定性比 NaO2好 |
| B.CsO2具有强氧化性,能与水反应生成O2,其中水作还原剂 |
| C.4KO2+2CO2= 2K2CO3+3O2,因此可用来作氧气源 |
| D.KO2与水反应后的溶液呈强碱性 |
您最近一年使用:0次
2020-09-09更新
|
1280次组卷
|
3卷引用:浙江省名校新高考研究联盟(Z20联盟)2021届高三第一次联考化学试题
浙江省名校新高考研究联盟(Z20联盟)2021届高三第一次联考化学试题湖北省武汉市汉阳、江夏2021-2022学年高一上学期12月联考化学试题(已下线)考点09 钠及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
解题方法
3 . Li—SOCl2电池是迄今具有最高能量比的电池。该电池的电极材料分别为锂和碳,电解液(熔点-110℃、沸点78.8℃)是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2。下列说法正确的是( )
| A.该电池不能在寒冷地区正常工作 |
| B.SOCl2分子的空间构型是平面三角形 |
| C.该电池工作时,正极反应为:2SOCl2+4e-=4Cl-+S+SO2 |
| D.该电池组装时,必须在无水无氧条件下进行 |
您最近一年使用:0次
19-20高一·浙江·阶段练习
解题方法
4 . 查找资料得知:大多数碳酸盐难溶于水。但雨水、河水中溶有CO2后,就会与土壤、岩石中的CaCO3等反应生成可溶性的碳酸氢盐进入水中,从而提高了水的硬度,这些可溶性的碳酸氢盐,加热时又易分解为CaCO3等难溶物质而形成水垢,绝大多数碳酸盐都具有类似的性质。请你结合所学知识分析,下列说法中正确的是( )
| A.除去CO2中的HCl气体,可以用饱和碳酸钠溶液 |
| B.向NaOH溶液通入过量的CO2,生成碳酸钠 |
| C.已知相同条件下,碳酸氢钠的溶解度远小于碳酸钠的溶解度。在一定温度下,向一定量的饱和碳酸钠溶液中通入足量的CO2,会有固体析出 |
D.可用加热方法除去碳酸氢钠固体中混有少量碳酸钠,该反应的化学方程式可以表示为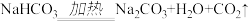 |
您最近一年使用:0次
名校
5 . 下列对碱金属的叙述,其中完全不 正确的组合是 ( )
①K通常保存在煤油中,以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最强的是钾
④碱金属阳离子,氧化性最强的是Li+
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大
⑥从Li到Cs,碱金属的密度越来越大,熔、沸点越来越低
①K通常保存在煤油中,以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最强的是钾
④碱金属阳离子,氧化性最强的是Li+
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大
⑥从Li到Cs,碱金属的密度越来越大,熔、沸点越来越低
| A.②③⑥ | B.②③④ | C.④⑤⑥ | D.①③⑤ |
您最近一年使用:0次
2019-06-18更新
|
1594次组卷
|
5卷引用:【全国百强校】黑龙江省鹤岗市第一中学2018-2019学年高一下学期第二次月考化学试题
名校
解题方法
6 . 实验室回收利用废旧锂离子电池正极材料锰酸锂(LiMn2O4)的一种流程如下:

(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是_________ 。
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为Mn(NO3)2、LiNO3等产物。请写出该反应离子方程式_________ 。
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是_________ 。
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是_________ 。
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成LiMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是________ 。
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH]:向Mn(OH)2中边搅拌边加入_________ 。

(1)废旧电池可能残留有单质锂,拆解不当易爆炸、着火,为了安全,对拆解环境的要求是
(2)“酸浸”时采用HNO3和H2O2的混合液体,可将难溶的LiMn2O4转化为Mn(NO3)2、LiNO3等产物。请写出该反应离子方程式
如果采用盐酸溶解,从反应产物的角度分析,以盐酸代替HNO3和H2O2混合物的缺点是
(3)“过滤2”时,洗涤Li2CO3沉淀的操作是
(4)把分析纯碳酸锂与二氧化锰两种粉末,按物质的量1:4混合均匀加热可重新生成LiMn2O4,升温到515℃时,开始有CO2产生,同时生成固体A,比预计碳酸锂的分解温度(723℃)低很多,可能的原因是
(5)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀的pH=7.7。请补充由上述过程中,制得的Mn(OH)2制备高纯MnCO3的操作步骤[实验中可选用的试剂:H2SO4、Na2CO3、C2H5OH]:向Mn(OH)2中边搅拌边加入
您最近一年使用:0次
2018-05-30更新
|
1317次组卷
|
3卷引用:【全国校级联考】江苏省南京市金陵中学、海安高级中学、南京外国语学校2018届高三第四次模拟考试化学试题



