名校
1 . 下列物质都能与浓热氢氧化钠溶液反应,产生气体与众不同的是
| A.Al | B.Si | C.P | D.B |
您最近半年使用:0次
名校
解题方法
2 . 下列反应的化学或离子方程式错误的是
A. 制 制 的离子方程式: 的离子方程式: |
B.白磷与 溶液反应: 溶液反应: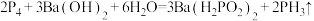 |
C. 与足量的 与足量的 溶液反应的离子方程式: 溶液反应的离子方程式: |
D.雌黄制备雄黄的方程式: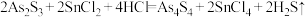 |
您最近半年使用:0次
3 . 磷化氢是常用的高效熏蒸杀虫剂。一种制备 的流程如下图所示:
的流程如下图所示:
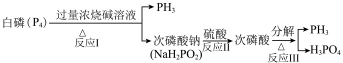
下列说法正确的是
A. 分子是正四面体结构, 分子是正四面体结构,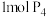 中含有 中含有 共价键 共价键 |
B.次磷酸钠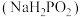 属于酸式盐 属于酸式盐 |
C.反应Ⅰ为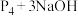 (浓) (浓) |
D.理论上,每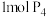 可生产 可生产 |
您最近半年使用:0次
4 . P2O5常用作气体的干燥剂,易吸水转化为H3PO4。下列说法不正确的是
| A.P2O5中P元素化合价为+5价 | B.P2O5属于碱性氧化物 |
| C.P2O5能与CaO反应 | D.P2O5能与NaOH反应 |
您最近半年使用:0次
5 . 回答下列问题
(1)下图为铁及其化合物的“价-类”二维图。
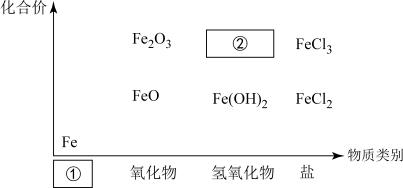
填写二维图缺失的类别 ①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2 ②Fe ③NaOH ④H2SO4 ⑤AgNO3
从物质类别 上看,FeCl3属于___________ ,可能与___________ 发生反应(填序号);从化合价角度看,Fe3+具有___________ 性,可能与___________ 发生反应(填序号)。
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),
经千年色彩依然,其中绿色来自蓝铜矿(主要成分为Cu(OH)2·2CuCO3)。其中Cu(OH)2·2CuCO3属于___________ (填“纯净物”或“混合物”),请写出Cu(OH)2·2CuCO3与盐酸反应的化学方程式 ___________
(4)酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
①H3PO2属于___________ 酸;NaH2PO2为___________ 盐(填序号)
a. 一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸 f.正盐 g.酸式盐
②写出H3PO2溶液与足量NaOH溶液反应的化学方程式___________ 。
(1)下图为铁及其化合物的“价-类”二维图。

填写二维图缺失的
(2)某同学利用以下试剂研究FeCl3性质,进行了如下预测:
①Cl2 ②Fe ③NaOH ④H2SO4 ⑤AgNO3
从物质
(3)宋代《千里江山图》描绘了山清水秀的美丽景色,来自孔雀石颜料(主要成分为Cu(OH)2·CuCO3),
经千年色彩依然,其中绿色来自蓝铜矿(主要成分为Cu(OH)2·2CuCO3)。其中Cu(OH)2·2CuCO3属于
(4)酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
①H3PO2属于
a. 一元酸 b.二元酸 c.三元酸 d.强酸 e.弱酸 f.正盐 g.酸式盐
②写出H3PO2溶液与足量NaOH溶液反应的化学方程式
您最近半年使用:0次
6 . 已知:①能量越低的物质就越稳定,②白磷转化成红磷的反应是放热反应。据此,下列判断或说法中正确的是
| A.在相同的条件下,红磷比白磷能量高 | B.在相同的条件下,白磷比红磷稳定 |
| C.红磷和白磷互为同素异形体 | D.白磷在空气中能自发转化成红磷 |
您最近半年使用:0次
7 . 大多数离子液体含有体积很大的阴、阳离子(如图所示)。其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。下列说法正确的是
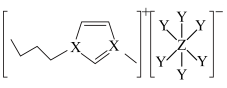

| A.Z的氯化物的分子式一定为ZCl3 | B.气态氢化物的熔沸点:Z>Y>X |
| C.电负性:Y>X>Z | D.此阴离子中Y、Z均满足8电子稳定结构 |
您最近半年使用:0次
解题方法
8 . 氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。
请回答下列问题。
(1)下列属于氮的固定的是___________ 。
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为___________ 。
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途___________ 。
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是___________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3>CH3COOH>H2PO ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为___________ 。
请回答下列问题。
(1)下列属于氮的固定的是
a.工业上N2和H2合成NH3 b.NH3催化氧化生成NO
c.N2和O2放电条件下生成NO d.NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)实验室中向浓氨水中加CaO固体可以快速制备氨气,请解释其反应原理
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a.制作坩埚 b.用作建筑陶瓷 c.制作耐高温轴承 d.制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0gNaOH最多可中和100mL1mol·L−1H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3>CH3COOH>H2PO
 ,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
您最近半年使用:0次
名校
9 . 已知,磷酸(H3PO4)是三元酸,Ka1=7.0×10-3,亚磷酸(H3PO3)是二元酸,Ka1=6.0×10-2,Ka2=2.5×10-7。亚磷酸易溶于水和醇,加热到180℃时分解成磷酸和磷化氢,亚磷酸在生产生活中还有很多其他用途。下列推测不正确的是
| A.Na2HPO3是酸式盐 | B.磷酸的酸性比亚磷酸弱 |
| C.亚磷酸既有氧化性又有还原性 | D.磷酸可以用于生产农药 |
您最近半年使用:0次
名校
10 .  是一种易自燃的气体,能被
是一种易自燃的气体,能被 溶液吸收生成
溶液吸收生成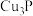 。实验室利用白磷与过量的NaOH溶液制备
。实验室利用白磷与过量的NaOH溶液制备 (反应过程中同时有
(反应过程中同时有 生成)。下列说法不正确的是
生成)。下列说法不正确的是
 是一种易自燃的气体,能被
是一种易自燃的气体,能被 溶液吸收生成
溶液吸收生成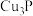 。实验室利用白磷与过量的NaOH溶液制备
。实验室利用白磷与过量的NaOH溶液制备 (反应过程中同时有
(反应过程中同时有 生成)。下列说法不正确的是
生成)。下列说法不正确的是A.熔沸点: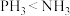 |
B.制取 时, 时, |
| C.装置中加入白磷前应先通入氮气 |
D. 溶液吸收 溶液吸收 表现了 表现了 的氧化性 的氧化性 |
您最近半年使用:0次



