下列对碱金属的叙述,其中完全不 正确的组合是 ( )
①K通常保存在煤油中,以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最强的是钾
④碱金属阳离子,氧化性最强的是Li+
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大
⑥从Li到Cs,碱金属的密度越来越大,熔、沸点越来越低
①K通常保存在煤油中,以隔绝与空气的接触
②碱金属常温下呈固态,取用时可直接用手拿
③碱金属中还原性最强的是钾
④碱金属阳离子,氧化性最强的是Li+
⑤碱金属的原子半径和离子半径都随核电荷数的增大而增大
⑥从Li到Cs,碱金属的密度越来越大,熔、沸点越来越低
| A.②③⑥ | B.②③④ | C.④⑤⑥ | D.①③⑤ |
更新时间:2019-06-18 07:13:48
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】查找资料得知:大多数碳酸盐难溶于水。但雨水、河水中溶有CO2后,就会与土壤、岩石中的CaCO3等反应生成可溶性的碳酸氢盐进入水中,从而提高了水的硬度,这些可溶性的碳酸氢盐,加热时又易分解为CaCO3等难溶物质而形成水垢,绝大多数碳酸盐都具有类似的性质。请你结合所学知识分析,下列说法中正确的是( )
| A.除去CO2中的HCl气体,可以用饱和碳酸钠溶液 |
| B.向NaOH溶液通入过量的CO2,生成碳酸钠 |
| C.已知相同条件下,碳酸氢钠的溶解度远小于碳酸钠的溶解度。在一定温度下,向一定量的饱和碳酸钠溶液中通入足量的CO2,会有固体析出 |
D.可用加热方法除去碳酸氢钠固体中混有少量碳酸钠,该反应的化学方程式可以表示为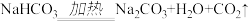 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】一种化合物的结构如图所示,Q、X、Y、Z、W为相邻两个短周期主族元素,原子序数依次增大,W元素的最外层电子数等于其电子总数的三分之一。下列说法正确的是
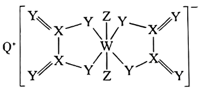

| A.通常所用的农药中含有Z、W等元素 |
| B.氢化物的沸点一定是Y>Z>X |
| C.由Q、Y、W形成的正盐只有一种 |
| D.Q的单质在空气中燃烧的产物具有强氧化性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】同主族元素的性质较为相似,下列关于同主族元素性质推测正确的是
| A.Li、Na同主族,因为Na在空气中加热生成Na2O2,所以Li在空气中加热生成Li2O2 |
| B.F、Cl同主族,因为HCl是强酸,所以HF也是强酸 |
| C.Ca、Ba同主族,因为Ca(OH)2微溶于水,所以Ba(OH)2也微溶于水 |
| D.F、Cl同主族,因为Cl2能与水反应,所以F2也能与水反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是( )
| A.微粒X+和Y-的核外电子排布相同,则离子半径:X+<Y- |
| B.Cs和Ba分别位于第六周期I A和IIA族,则碱性:CsOH>Ba(OH)2 |
| C.由水溶液的酸性:HCl>HF,可以推断出元素的非金属性:C1>F |
| D.Be与Al同处于同周期表金属与非金属交界处,可推出:Be(OH)2+2OH-=BeO22- +2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列说法正确的是
| A.Br的非金属性比I强,HBr比HI的稳定性强 |
| B.P的原子半径比N大,H3PO4 比HNO3 的酸性强 |
| C.Na熔点比K高, NaOH的碱性比KOH强 |
| D.非金属性Cl>Br>I,沸点HCl>HBr>HI |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】如图是部分短周期元素的单质及其化合物(或溶液)的转化关系,已知单质B2、C2、D2、E2在常温常压下都是气体,化合物G的焰色反应为黄色;化合物I、J、K通常状况下呈气态。下列说法正确的是
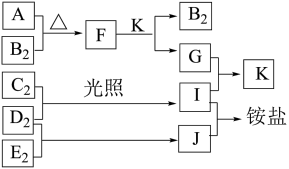

| A.B氢化物的沸点高于其同主族其它元素氢化物的沸点 |
| B.原子半径大小:A>C>B>E>D |
| C.F中既含有离子键又含有极性共价键 |
| D.G中的阴离子能抑制水的电离 |
您最近一年使用:0次




