NO2是一种红棕色气体,沸点为21℃。机动车尾气、锅炉废气是NO2的重要的排放源。完成下列填空:
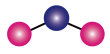
(1)NO2的分子模型如图所示,该模型的类型为_______ 。
(2)下列说法正确的是_____
A.N原子和O原子2p亚层的电子能量相同
B.N原子和O原子核外电子都有4种伸展方向
C.NO2和O2均为非极性分子
D.NO2和O2分子中各原子最外层电子数均为8
(3)元素非金属性:氮<氧,从原子结构的角度分析其原因:_______ 。列举一个事实说明N、O元素非金属性强弱:_______ 。
(4)点燃的镁条可以在NO2中继续燃烧,实验现象为_______ 。
(5)硝酸铜在1000℃时分解,其转化关系为:Cu(NO3)2→Cu+NO2↑+O2↑,该反应中断裂的化学键类型为_______ 。所得气体的平均分子量为_______ 。
(6)学生甲为了探究NO2对非金属的助燃性,利用排空气法收集上述反应生成的气体,并插入带火星的木条。学生乙认为该方法并不能达到其实验目的,原因是_______ 。
学生丙查阅文献得知,NO2不能使带火星的木条复燃。
(7)请在学生甲设计的实验方案基础上加以改进,帮助学生丙验证其所查文献描述NO2的性质:_______ 。
(1)NO2的分子模型如图所示,该模型的类型为

(2)下列说法正确的是
A.N原子和O原子2p亚层的电子能量相同
B.N原子和O原子核外电子都有4种伸展方向
C.NO2和O2均为非极性分子
D.NO2和O2分子中各原子最外层电子数均为8
(3)元素非金属性:氮<氧,从原子结构的角度分析其原因:
(4)点燃的镁条可以在NO2中继续燃烧,实验现象为
(5)硝酸铜在1000℃时分解,其转化关系为:Cu(NO3)2→Cu+NO2↑+O2↑,该反应中断裂的化学键类型为
(6)学生甲为了探究NO2对非金属的助燃性,利用排空气法收集上述反应生成的气体,并插入带火星的木条。学生乙认为该方法并不能达到其实验目的,原因是
学生丙查阅文献得知,NO2不能使带火星的木条复燃。
(7)请在学生甲设计的实验方案基础上加以改进,帮助学生丙验证其所查文献描述NO2的性质:
更新时间:2021-04-09 20:03:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用符号填空:a质子数;b中子数;c核外电子数;d最外层电子数。
(1)原子种类由___ 决定,
(2)元素种类由___ 决定,
(3)核电荷数由___ 决定,
(4)相对原子质量由___ 决定,
(5)元素的化合价主要由____ 决定,
(6)元素的化学性质主要由____ 决定。
(1)原子种类由
(2)元素种类由
(3)核电荷数由
(4)相对原子质量由
(5)元素的化合价主要由
(6)元素的化学性质主要由
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A_______ ,B_______ ,C_______ ,D______ ,E_______ 。
(2)B微粒的结构示意图________ ,D微粒的结构示意图_________ 。
(3)A的单质与EB溶液反应的离子方程式:_______________ 。
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A
(2)B微粒的结构示意图
(3)A的单质与EB溶液反应的离子方程式:
您最近一年使用:0次
【推荐3】A、B、C、D、代表4种元素,请完成下列问题:
(1)A元素的负一价离子的电子层结构与氩相同,B元素的正一价离子的电子层结构与氙相同,A、B形成的化合物的化学式为____________ .
(2)C元素的正三价离子的3d轨道为半充满状态,C元素的符号为_________ .在同期表中位置_________ ,其基态原子的价电子排布图为____________ .
(3)D元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,其硫酸盐逐滴加入氨水生成难溶物的离子方程式为__________________________ ,继续添加氨水,难溶物溶解,得到深蓝色溶液的离子方程为_______________________ ,写出阳离子的结构式____________ .
(1)A元素的负一价离子的电子层结构与氩相同,B元素的正一价离子的电子层结构与氙相同,A、B形成的化合物的化学式为
(2)C元素的正三价离子的3d轨道为半充满状态,C元素的符号为
(3)D元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,其硫酸盐逐滴加入氨水生成难溶物的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用序号按要求回答下列问题:
(1)下列各组微粒: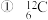 与
与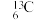
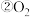 和
和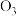
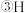 、D、
、D、 金刚石和石墨
金刚石和石墨 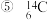 和
和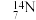 ,互为同位素的是
,互为同位素的是_________ ;互为同素异形体的是________ ;质量数相等,但不能互称为同位素的是 ______ 。
(2)下列各种物质:
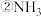
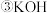 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 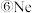 ,不存在化学键的是
,不存在化学键的是______ ;只存在离子键的是______ ;属于共价化合物的是________ ;含非极性键的离子化合物是 _________ 。
(3)下列变化过程: 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是__________ ; 仅破坏离子键的是__________ ;仅破坏共价键的是__________ 。
(1)下列各组微粒:
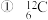 与
与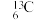
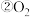 和
和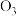
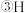 、D、
、D、 金刚石和石墨
金刚石和石墨 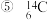 和
和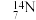 ,互为同位素的是
,互为同位素的是(2)下列各种物质:

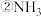
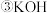 ④Na2O2 ⑤MgCl2
④Na2O2 ⑤MgCl2 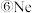 ,不存在化学键的是
,不存在化学键的是(3)下列变化过程:
 碘的升华
碘的升华  NaCl固体溶于水
NaCl固体溶于水  O2溶于水
O2溶于水  HCl气体溶于水
HCl气体溶于水 烧碱熔化
烧碱熔化  氯化铵受热分解,化学键没有被破坏的是
氯化铵受热分解,化学键没有被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.下列是中学化学中熟悉的物质,请用序号完成下列问题
①O2②Na2O2③NH4Cl④HCl⑤NaOH⑥CaCl2⑦氦气
(1)这些物质中,只含共价键的是_______ 。只含离子键的是_______ 。既含共价键又含离子键的是_______ 。
(2)属于离子化合物的是_______ 。
II.已知拆开1 mol H﹣H键、1 mol I﹣I、1 mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1 mol HI需要_______ (填“放出”或“吸收”)_______ kJ的热量。
①O2②Na2O2③NH4Cl④HCl⑤NaOH⑥CaCl2⑦氦气
(1)这些物质中,只含共价键的是
(2)属于离子化合物的是
II.已知拆开1 mol H﹣H键、1 mol I﹣I、1 mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1 mol HI需要
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)已知固态NH3、H2O、HF中的氢键的键能和结构示意图如表所示:

H2O、HF、NH3沸点依次降低的原因是____ 。
(2)已知:常温时H2A的Ka1=5×10-5,Ka2=3×10-9,请判断NaHA溶液的酸碱性并说明原因:____ 。
(1)已知固态NH3、H2O、HF中的氢键的键能和结构示意图如表所示:
| 物质及其氢键 | HF(s):F—H…F | H2O(s):O—H…O | NH3(s):N—H…N |
| 键能/(kJ·mol-1) | 28.1 | 18.8 | 5.4 |

H2O、HF、NH3沸点依次降低的原因是
(2)已知:常温时H2A的Ka1=5×10-5,Ka2=3×10-9,请判断NaHA溶液的酸碱性并说明原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)短周期某主族元素,M的电离能情况如图A所示,则M在元素周期表的第_______ 族。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是_______ (写化学式)。a点所在折线元素氢化物的沸点变化规律如图B,呈现这种变化关系的原因是_______

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键_______ 。
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
亚磷酸 (H3PO3) 也是中强酸,它的结构式为_______ ;亚磷酸 (H3PO3)为_______ 元酸。

(2)如图B所示,每条折线表示周期表ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)用氢键表示式写出氨水中NH3分子与水分子间可能存在的氢键
(4)表中列出了含氧酸酸性强弱与非羟基氧原子数的关系。
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 |  |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】
(1)对于A.MgO;B.He;C.NH3;D.CaO;E.干冰;F.Ar五种物质:
①熔沸点最低的是________ ;液态时能导电的是________ (填字母编号)。
②上述物质的晶体中,属于离子晶体且熔点最高的是_______________ (填字母编号)。
③上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是______ (填字母编号)。
(2)已知熔融的BeCl2不导电,则BeCl2属于______ 晶体,中心原子的杂化类型为______ 。
(3)氮、磷、砷在农药、肥料等农业生产方面有广泛的应用。请回答相关问题:氨水是一种速效氮肥,氨水中含有配位键的粒子有H3O+和X,则X的离子符号为_________________ ,X离子中形成的配位键中提供孤电子对的原子是________________ 。
(1)对于A.MgO;B.He;C.NH3;D.CaO;E.干冰;F.Ar五种物质:
①熔沸点最低的是
②上述物质的晶体中,属于离子晶体且熔点最高的是
③上述物质的晶体熔化时,所克服的微粒间的作用力与冰熔化时所克服的作用力类型完全相同的是
(2)已知熔融的BeCl2不导电,则BeCl2属于
(3)氮、磷、砷在农药、肥料等农业生产方面有广泛的应用。请回答相关问题:氨水是一种速效氮肥,氨水中含有配位键的粒子有H3O+和X,则X的离子符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】装置B是安全瓶,可监测实验进行时D中是否发生堵塞,若发生堵塞,装置B的玻璃管中可能出现的现象是_______ 。


您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】碱式碳酸铜可表示为:xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。现采用氢气还原法,实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是_______ (填入仪器接口字母编号):(a)→→→→→→(l)


您最近一年使用:0次



