按要求填空。
(1)电子式: O2:_______ CO2:_______ NH4Cl:_______ Mg(OH)2:_______
(2)用电子式写出K2S的形成过程_______ 。
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是_______ (填序号,下同),属于电解质的是_______ ,上述条件下能导电的是_______ 。
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是_______ (填序号,下同),互为同素异形体的一组是_______ 。
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成_______ 种不同的氯化氢分子,其对应的相对分子质量有_______ 种。
(1)电子式: O2:
(2)用电子式写出K2S的形成过程
(3)有以下物质:①CO2②熔融KOH③生铁④稀硫酸⑤铜⑥Na2O2⑦苏打⑧CaO⑨无水乙醇⑩CO。上述物质中属于碱性氧化物的是
(4)已知①234U、236U、238U②16O2、17O3、18O4③12C16O、13C16O、14C16O,其中互为同位素的一组是
(5)已知氢有3种核素:1H、2H、3H,氯有3种核素:35Cl、36Cl、37Cl,上述核素能形成
更新时间:2021-04-16 02:16:23
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列物质:①空气②H2O③Fe④CO2⑤H2SO4⑥Mg(OH)2⑦NaHSO4⑧碘酒⑨CaSO4·2H2O⑩CH3CH2OH,其中属于混合物的是___________ (填写序号,下同);属于氧化物的是___________ ,属于酸的是___________ ,属于碱的是___________ ,属于盐的是___________ ,属于电解质的是___________
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】对于数以千万计的化学物质和为数众多的化学反应,分类法的作用几乎是无可代替的。现有以下物质:①液氯;② ;③
;③ ;④澄清石灰水;⑤
;④澄清石灰水;⑤ 溶液;⑥干冰;⑦氢氧化钾溶液;⑧碳酸钾固体;⑨碳酸氢钠固体;⑩
溶液;⑥干冰;⑦氢氧化钾溶液;⑧碳酸钾固体;⑨碳酸氢钠固体;⑩ 胶体。回答下列问题:
胶体。回答下列问题:
(1)以上物质中属于电解质的是___________ 。
(2)向⑨中加入少量水后,固体溶解,并伴有___________ (填“吸热”或“放热”)现象。
(3)写出过量的⑥和④发生反应的总的离子方程式___________ 。
(4)将物质的量均为1mol的②和⑨混合固体加热充分反应,所得的固体的物质的量为___________ mol。
(5)将⑤溶液滴加到③固体中,反应的离子方程式为___________ 。
(6)鉴别⑧和⑨两种固体,现象明显的定性分析操作为___________ 。
(7)将2molHCl气体通入到溶质物质的量均为1mol的⑦和⑧的混合溶液中充分反应,则得到的溶质为___________ 。
(8)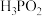 (次磷酸)与足量的⑦反应只生成一种盐
(次磷酸)与足量的⑦反应只生成一种盐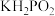 ,则
,则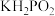 属于
属于___________ 。(填写“正盐”、“酸式盐”、“碱式盐”)
 ;③
;③ ;④澄清石灰水;⑤
;④澄清石灰水;⑤ 溶液;⑥干冰;⑦氢氧化钾溶液;⑧碳酸钾固体;⑨碳酸氢钠固体;⑩
溶液;⑥干冰;⑦氢氧化钾溶液;⑧碳酸钾固体;⑨碳酸氢钠固体;⑩ 胶体。回答下列问题:
胶体。回答下列问题:(1)以上物质中属于电解质的是
(2)向⑨中加入少量水后,固体溶解,并伴有
(3)写出过量的⑥和④发生反应的总的离子方程式
(4)将物质的量均为1mol的②和⑨混合固体加热充分反应,所得的固体的物质的量为
(5)将⑤溶液滴加到③固体中,反应的离子方程式为
(6)鉴别⑧和⑨两种固体,现象明显的定性分析操作为
(7)将2molHCl气体通入到溶质物质的量均为1mol的⑦和⑧的混合溶液中充分反应,则得到的溶质为
(8)
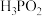 (次磷酸)与足量的⑦反应只生成一种盐
(次磷酸)与足量的⑦反应只生成一种盐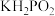 ,则
,则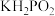 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.以下8种为中学化学中常见的物质,请按下列分类标准回答问题:(填序号)
① CaCO3 ②液态SO2 ③胆矾 ④熔融氢氧化钠 ⑤H2SO4 ⑥氨水 ⑦酒精 ⑧Cu
(1)属于电解质的是_______________ ;(2)属于盐的是____________________ ;
(3)能导电的是___________________ ;(4)属于非电解质的是_______________ ;
II.(1)2015年10月,屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。青蒿素(化学式为C15H22O5)是治疗疟疾的特效药,青蒿素的摩尔质量是_____________ ,青蒿素中碳、氧元素的质量比为____________ ,56.4g青蒿素中含有的氧原子数目为_____________ ;
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为____________ ,推断的依据为_____________________ ;
(3)完全中和相同体积、相同物质的量浓度的Ba(OH)2溶液,需要相同物质的量浓度的盐酸、硫酸溶液的体积比为_____________ 。
① CaCO3 ②液态SO2 ③胆矾 ④熔融氢氧化钠 ⑤H2SO4 ⑥氨水 ⑦酒精 ⑧Cu
(1)属于电解质的是
(3)能导电的是
II.(1)2015年10月,屠呦呦因发现青蒿素和双氢青蒿素治疗疟疾的新疗法而获得诺贝尔生理学或医学奖。青蒿素(化学式为C15H22O5)是治疗疟疾的特效药,青蒿素的摩尔质量是
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10 mL A受热分解生成15 mL O2和10 mL F2,则A的化学式为
(3)完全中和相同体积、相同物质的量浓度的Ba(OH)2溶液,需要相同物质的量浓度的盐酸、硫酸溶液的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】甲烷的组成与结构
| 化学式 | 电子式 | 结构式 | 分子结构示意图 | 球棍模型 |
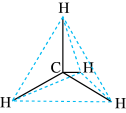 | 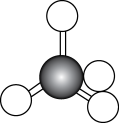 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】如图是元素周期表的一部分,回答下列问题。
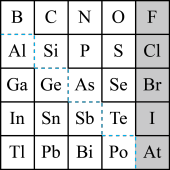
(1)元素 在元素周期表中的位置为
在元素周期表中的位置为_______ (写明周期数和族序数)。
(2) 的最高正价为
的最高正价为_______ , 的最高价氧化物为
的最高价氧化物为_______ (填化学式)。
(3)根据元素周期律推断:
①阴影部分元素最容易与氢气化合的是_______ (填元素符号)。
②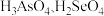 的酸性强弱:
的酸性强弱:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③氢化物的还原性:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4)可在图中分界线(虚线部分)附近寻找_______(填序号)。
(5)① 常用作溶剂,其电子式为
常用作溶剂,其电子式为_______ 。
②镓( )的化合物氮化镓(
)的化合物氮化镓( )和砷化镓(
)和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是_______ (填序号)。
A.原子半径: B.N的非金属性比O强
B.N的非金属性比O强
C. 的金属性比
的金属性比 弱 D.
弱 D. 和
和 的氧化物可能是两性氧化物
的氧化物可能是两性氧化物
(6)用如图装置证明酸性: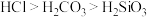 ,则溶液b为
,则溶液b为_______ 。下列事实可用于比较元素C与 非金属性相对强弱的是
非金属性相对强弱的是_______ (填序号)。
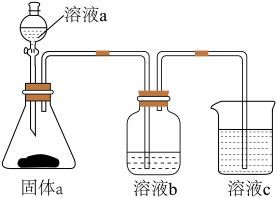
A.最高正化合价
B. 的氢化物比C的简单氢化物稳定
的氢化物比C的简单氢化物稳定
C. 的氢化物比C的简单氢化物沸点高
的氢化物比C的简单氢化物沸点高
D.最高价氧化物对应的水化物的酸性: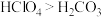

(1)元素
 在元素周期表中的位置为
在元素周期表中的位置为(2)
 的最高正价为
的最高正价为 的最高价氧化物为
的最高价氧化物为(3)根据元素周期律推断:
①阴影部分元素最容易与氢气化合的是
②
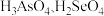 的酸性强弱:
的酸性强弱:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③氢化物的还原性:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)可在图中分界线(虚线部分)附近寻找_______(填序号)。
| A.农药 | B.合金材料 | C.半导体材料 | D.优良的催化剂 |
 常用作溶剂,其电子式为
常用作溶剂,其电子式为②镓(
 )的化合物氮化镓(
)的化合物氮化镓( )和砷化镓(
)和砷化镓( )作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是
)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。下列说法正确的是A.原子半径:
 B.N的非金属性比O强
B.N的非金属性比O强C.
 的金属性比
的金属性比 弱 D.
弱 D. 和
和 的氧化物可能是两性氧化物
的氧化物可能是两性氧化物(6)用如图装置证明酸性:
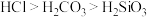 ,则溶液b为
,则溶液b为 非金属性相对强弱的是
非金属性相对强弱的是
A.最高正化合价

B.
 的氢化物比C的简单氢化物稳定
的氢化物比C的简单氢化物稳定C.
 的氢化物比C的简单氢化物沸点高
的氢化物比C的简单氢化物沸点高D.最高价氧化物对应的水化物的酸性:
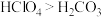
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)写出下列物质的电子式: HClO_____________ ;
(2)用电子式表示下列物质的形成过程:MgCl2___________________ 。
(2)用电子式表示下列物质的形成过程:MgCl2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有①BaCl2、②金刚石、③KOH、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是__ (填写物质的序号,下同),熔化时需要破坏共价键的是___ 。
(2)属于离子化合物的是____ ,只有离子键的物质是___ 。
(1)熔化时不需要破坏化学键的是
(2)属于离子化合物的是
您最近一年使用:0次
【推荐3】按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是_______
(2)写出下列物质的电子式:N2_______ NH4I_______
(3)用电子式表示下列化合物的形成过程:Na2S:_______
(4)1L烷烃A的蒸气完全燃烧时,生成同温同压下9L水蒸气,则烷烃A含有6个甲基的结构简式_______ ;
(5)烷烃B在同温同压下蒸气密度是H2的50倍,则烷烃B主链有5个碳原子的同分异构体有_______ 种,
(6)C4H8Cl2的二氯代物有_______ 种。
(7)有下列各组物质:
①O2和O3②H2 D2 T2③12C和14C ④CH3CH2CH2CH3和(CH3)2CHCH3⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 ⑦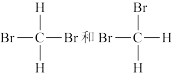
互为同位素的是_______ (填序号,下同);互为同分异构体的是_______ ;互为同素异形体的是_______ ;为同一物质的是_______ ;互为同系物的是_______
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:N2
(3)用电子式表示下列化合物的形成过程:Na2S:
(4)1L烷烃A的蒸气完全燃烧时,生成同温同压下9L水蒸气,则烷烃A含有6个甲基的结构简式
(5)烷烃B在同温同压下蒸气密度是H2的50倍,则烷烃B主链有5个碳原子的同分异构体有
(6)C4H8Cl2的二氯代物有
(7)有下列各组物质:
①O2和O3②H2 D2 T2③12C和14C ④CH3CH2CH2CH3和(CH3)2CHCH3⑤癸烷和十六烷 ⑥CH3(CH2)5CH3和CH3CH2CH2CH(CH3)C2H5 ⑦
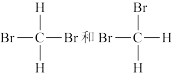
互为同位素的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】碳及其化合物广泛存在于自然界中,碳在形成化合物时,其键型以共价键为主,原因是_______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)硫酸镍溶于过量的氨水可形成[Ni(NH3)6]SO4溶液。
①[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为_____ ,中心原子(离子)是____ ;
②SO42-中,中心原子的轨道杂化类型为_______ ;
③写出一种与SO42-互为等电子体的分子的化学式______ ;
(2)NH3极易溶于水,除因为它们都是极性分子外,还因为__________ 。
(3)已知H—H键能为436kJ/mol,N≡N键的键能为945kJ/mol,根据化学方程式:N2+3H2 ==2NH3 ΔH=-92.4kJ/mol,则H—N键能为____ kJ/mol。
(4)下列分子既存在p-sp σ键,也存在p-p π键的是_____ 。
A.NH3 B.H2 C.CO2 D.C2H2
(5)根据已经掌握的共价键知识判断,键的极性N—H___ O—H(“>”,“=”或“<”)
①[Ni(NH3)6]SO4中Ni2+与NH3之间形成的化学键称为
②SO42-中,中心原子的轨道杂化类型为
③写出一种与SO42-互为等电子体的分子的化学式
(2)NH3极易溶于水,除因为它们都是极性分子外,还因为
(3)已知H—H键能为436kJ/mol,N≡N键的键能为945kJ/mol,根据化学方程式:N2+3H2 ==2NH3 ΔH=-92.4kJ/mol,则H—N键能为
(4)下列分子既存在p-sp σ键,也存在p-p π键的是
A.NH3 B.H2 C.CO2 D.C2H2
(5)根据已经掌握的共价键知识判断,键的极性N—H
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】碳原子最外层有4个电子,可以形成4对共用电子对,因此碳原子的成键方式有多种。
(1)请根据碳原子的成键情况,写出对应物质的结构式(只要求能写出一种)
①形成4个单键:___________
②形成2个单键和一个双键:___________
③形成1个单键和1个叁键:___________
④形成2个双键:___________
(2)氮原子最外层有5个电子,可以形成___________ 对共用电子对。请对照碳原子的成键情况,分析氮原子的成键情况,并举例说明_________
(3)水分子的组成为什么是H2O而不是H3O?_________
(1)请根据碳原子的成键情况,写出对应物质的结构式(只要求能写出一种)
①形成4个单键:
②形成2个单键和一个双键:
③形成1个单键和1个叁键:
④形成2个双键:
(2)氮原子最外层有5个电子,可以形成
(3)水分子的组成为什么是H2O而不是H3O?
您最近一年使用:0次

 ;
;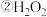 ;
;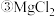 ;
;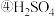 ;
;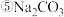 ;
; ;
;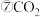 ;
; ;
;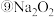 ;⑩NaOH
;⑩NaOH 填序号,下同
填序号,下同 ;只含有离子键的是
;只含有离子键的是

