A、B、D、E、F为原子序数依次增大的五种短周期主族元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B单质在D单质中充分燃烧能生成其最高价化合物BD2,E+与D2-具有相同的电子数。A单质在F单质中燃烧,产物溶于水得到一种强酸。用相应的化学用语回答下列问题:
(1)F在周期表中的位置是____ ,EFD的电子式为_____ 。
(2)A2D2的分子中化学键类型为___ 。
(3)元素D、E、F形成的简单离子的半径由大到小为_____ (用离子符号表示)。
(4)B、D的最简单气态氢化物的稳定性:___ (用化学式表示)。
(5)设计一个简单的实验证明F和B的非金属性强弱:___ (用化学方程式表示)。
(1)F在周期表中的位置是
(2)A2D2的分子中化学键类型为
(3)元素D、E、F形成的简单离子的半径由大到小为
(4)B、D的最简单气态氢化物的稳定性:
(5)设计一个简单的实验证明F和B的非金属性强弱:
更新时间:2021-04-20 09:37:53
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F六种短周期元素,其原子序数依次增大。A原子的最外层电子数是次外层电子数的2倍,C的氢化物在常温下为液体,D能形成DF型离子化合物,0.9 g E与足量的稀硫酸反应生成的氢气在标准状况下的体积为1.12 L,F的族序数与周期序数之差为4。请回答下列问题:
(1)写出元素符号:A________ ;B________ ; F________ 。
(2)六种元素中,单质还原性最强的是______ (写化学式,下同);最高价氧化物对应水化物中酸性最强的酸是______ 。
(3)写出C与D形成的原子个数比为1:1的化合物的电子式:______ 所含化学键类型为______ 。
(4)六种元素中的三种元素组成的某种盐的水溶液呈碱性,是家用消毒剂的主要成分,请用离子方程式解释该盐溶液呈碱性的原因:_________________________ 。
(5)D、E元素的最高价氧化物对应的水化物发生反应的离子方程式为__________ 。
(6)写出用惰性电极电解饱和DF溶液的化学方程式:________________________ 。
(1)写出元素符号:A
(2)六种元素中,单质还原性最强的是
(3)写出C与D形成的原子个数比为1:1的化合物的电子式:
(4)六种元素中的三种元素组成的某种盐的水溶液呈碱性,是家用消毒剂的主要成分,请用离子方程式解释该盐溶液呈碱性的原因:
(5)D、E元素的最高价氧化物对应的水化物发生反应的离子方程式为
(6)写出用惰性电极电解饱和DF溶液的化学方程式:
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,B是最活泼的非金属元素,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是周期表中最强的含氧酸。
(1)元素B在周期表中的位置是_________ ,甲的电子式是_______ 。
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是___________ 。
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是________ 。
(4)物质乙与水反应的化学方程式____________ 。
(1)元素B在周期表中的位置是
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是
(4)物质乙与水反应的化学方程式
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】联合国大会将2019年定为“化学元素周期表国际年”,表明了元素周期律的重要性。以下短周期主族元素中,含元素a的化合物被广泛用于制作手机电池,古迪纳夫因在该领域做出了杰出贡献荣获2019年诺贝尔化学奖。
(1)a原子结构示意图为_______ 。
(2)d在周期表中的位置是_______ 。
(3)元素g的单质与NaOH溶液反应的离子方程式为_______ 。
(4)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为_______ 。
(5)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为_______ 。
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应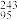 Am+
Am+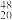 Ca→Mc+3
Ca→Mc+3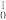 n得到。Mc用核素符号表示为
n得到。Mc用核素符号表示为_______ 。
| a | … | b | c | d | |||
| e | … | g | h | j |
(2)d在周期表中的位置是
(3)元素g的单质与NaOH溶液反应的离子方程式为
(4)由单质a制成的电池需要注意防水,其原因用化学反应方程式表示为
(5)科学家在研究元素周期表时,预言了在元素h的下一周期存在一种“类h”元素,该元素多年后被德国化学家文克勒发现,命名为锗(Ge),锗在周期表的位置为
(6)2016年IUPAC确认了四种新元素,其中一种为Mc,中文为“镆”、Mc可由反应
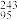 Am+
Am+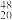 Ca→Mc+3
Ca→Mc+3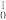 n得到。Mc用核素符号表示为
n得到。Mc用核素符号表示为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种短周期元素,A元素原子的外围电子排布式为2s22p2;B元素与A元素位于同一周期,其原子的原子核外有三个未成对电子;C元素位于第2周期,电负性仅次于氟;D元素在短周期元素中第一电离能最小。
(1)A、B、C、D四种元素分别是_______ 。
(2)A的最高价氧化物的电子式是_______ 。
(3)A、B、C、D四种元素电负性由大到小的顺序是_______ 。
(4)B、C两种元素气态氢化物的稳定性大小的顺序是_______ 。
(1)A、B、C、D四种元素分别是
(2)A的最高价氧化物的电子式是
(3)A、B、C、D四种元素电负性由大到小的顺序是
(4)B、C两种元素气态氢化物的稳定性大小的顺序是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】现有四种短周期元素X、Y、Z、W,其中:①X、W原子的电子层数与最外层电子数之比分别为3:1和1:3,②Y元素的某原子核内无中子,③Z元素原子的最外层电子数是其内层电子总数的2倍。回答下列问题:
(1)X元素在周期表中的位置是__________ 。
(2)化合物X2W2的电子式是__________ 。
(3)向含1molNa2SiO3的溶液中缓慢通入2mol的ZO2,反应的离子方程式是__________ 。
(4)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是__________ (只需填一个化学式)。
(5)用KMnO4溶液可以通过滴定来测定Y2Z2W4溶液的物质的量浓度。向2500mL的Y2Z2W4溶液中加入500mL050mol/L酸性KMnO4溶液恰好完全反应,得到ZO2和Mn2+,则此种Y2Z2W4溶液的物质的量浓度是__________ mol/L。
(1)X元素在周期表中的位置是
(2)化合物X2W2的电子式是
(3)向含1molNa2SiO3的溶液中缓慢通入2mol的ZO2,反应的离子方程式是
(4)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是
(5)用KMnO4溶液可以通过滴定来测定Y2Z2W4溶液的物质的量浓度。向2500mL的Y2Z2W4溶液中加入500mL050mol/L酸性KMnO4溶液恰好完全反应,得到ZO2和Mn2+,则此种Y2Z2W4溶液的物质的量浓度是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
(1)元素①和②形成的最简单有机化合物是___________ (填分子式)。
(2)元素③的原子结构示意图为___________ ,其最简单氢化物的电子式是___________ 。
(3)元素④、⑤形成的简单离子半径较大的是___________ (填离子符号)。
(4)元素⑥的最高价氧化物对应的水化物与元素⑦最高价氧化物对应的水化物稀溶液反应的离子方程式为___________ 。
(5)⑦原子的得电子能力___________ (填“强于”“弱于”或“等于”)⑧原子,其原因是(从原子结构的角度分析)___________ ,写出一个能证明该结论的离子方程式___________ 。
(6)向 的水溶液中通入⑧单质并充分振荡,混合溶液逐渐褪为无色,若
的水溶液中通入⑧单质并充分振荡,混合溶液逐渐褪为无色,若 还原剂转移
还原剂转移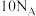 电子,上述反应的化学方程式为
电子,上述反应的化学方程式为___________ 。
| 周期\族 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③的原子结构示意图为
(3)元素④、⑤形成的简单离子半径较大的是
(4)元素⑥的最高价氧化物对应的水化物与元素⑦最高价氧化物对应的水化物稀溶液反应的离子方程式为
(5)⑦原子的得电子能力
(6)向
 的水溶液中通入⑧单质并充分振荡,混合溶液逐渐褪为无色,若
的水溶液中通入⑧单质并充分振荡,混合溶液逐渐褪为无色,若 还原剂转移
还原剂转移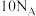 电子,上述反应的化学方程式为
电子,上述反应的化学方程式为
您最近半年使用:0次



