(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d能级,该能层有_______ 个原子轨道,该元素基态原子的价电子排布图为_______ 。
(2)B为第三周期金属元素。依据下表数据,写出B原子的核外电子排布式:_______ 。
(2)B为第三周期金属元素。依据下表数据,写出B原子的核外电子排布式:
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| B | 738 | 1451 | 7733 | 10540 |
更新时间:2021-05-08 12:57:22
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】解题技巧:粒子半径比较的一般思路
(1)“一层”:先看能层数,能层数越_______ ,一般微粒半径越_______ 。
(2)“二核”:若能层数相同,则看核电荷数,核电荷数越_______ ,微粒半径越_______ 。
(3)“三电子”:若能层数、核电荷数均相同,则看核外电子数,电子数_______ 的半径_______ 。
(1)“一层”:先看能层数,能层数越
(2)“二核”:若能层数相同,则看核电荷数,核电荷数越
(3)“三电子”:若能层数、核电荷数均相同,则看核外电子数,电子数
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.回答下列问题:
(1)核外电子排布时遵循一定的原则:在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理称为泡利不相容原理;对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同称为洪特规则。依据以上原则,下列原子或离子的核外电子排布正确的是_______ ,违反能量最低原理的是_______ ,违反洪特规则的是_______ ,违反泡利不相容原理的是_______ 。
①Ca2+:1s22s22p63s23p6 ②F-:1s22s22p5 ③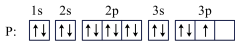 ④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
Ⅱ.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(2)写出铜的基态原子的电子排布式:______ 。
(3)Fe3+的电子排布式为______ 。
(4)p电子的原子轨道呈______ 形。
(1)核外电子排布时遵循一定的原则:在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反,这个原理称为泡利不相容原理;对于基态原子,核外电子在能量相同的原子轨道上排布时,将尽可能分占不同的原子轨道并且自旋状态相同称为洪特规则。依据以上原则,下列原子或离子的核外电子排布正确的是
①Ca2+:1s22s22p63s23p6 ②F-:1s22s22p5 ③
 ④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
④Cr:1s22s22p63s23p63d44s2 ⑤K:1s22s22p63s23p63d1 ⑥Mg:1s22s22p63s2 ⑦C:
Ⅱ.2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
(2)写出铜的基态原子的电子排布式:
(3)Fe3+的电子排布式为
(4)p电子的原子轨道呈
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)在短周期元素中基态原子的p轨道有1个未成对电子的元素可能是_______ (填元素符号,下同),其核外电子排布式分别是_______ 。
(2)基态原子的N层有1个未成对电子,M层未成对电子最多的元素是_______ ,其价电子排布式为_______ 。
(3)最外层电子数是次外层电子数3倍的元素是_______ ,其电子排布图为_______ 。
(4)Cu原子的结构示意图为_______ 。
(5)下列表示的为一激发态原子的是_______ 。
A.1s12s1 B.1s22s22p1 C.1s22p53s1D.1s22s22p63s2
(2)基态原子的N层有1个未成对电子,M层未成对电子最多的元素是
(3)最外层电子数是次外层电子数3倍的元素是
(4)Cu原子的结构示意图为
(5)下列表示的为一激发态原子的是
A.1s12s1 B.1s22s22p1 C.1s22p53s1D.1s22s22p63s2
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素周期表的分区
(1)按电子排布分区
(2)按金属元素与非金属元素分区_______ 与_______ 之间画一条线,线的左边是金属元素(氢除外),线的右边是非金属元素。
金属与非金属交界处元素的性质特点:在元素周期表中位于金属和非金属分界线上的元素兼有金属和非金属的性质,位于此处的元素(如硼、硅、锗、砷、锑等)常被称为半金属或类金属(一般可用作半导体材料)。
(1)按电子排布分区
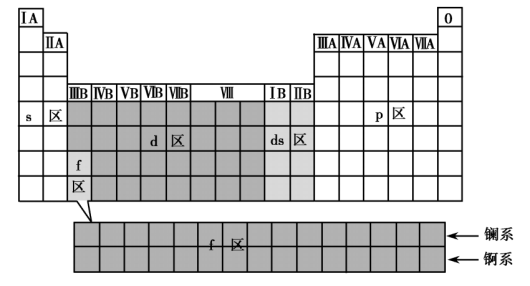
| 分区 | 元素分布 | 价层电子排布式 | 元素性质特点 |
| s区 | 除氢外都是活泼金属元素 | ||
| p区 | 最外层电子参与反应 | ||
| d区 | d轨道不同程度地参与化学键的形成 | ||
| ds区 | 金属元素 |
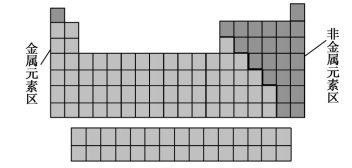
金属与非金属交界处元素的性质特点:在元素周期表中位于金属和非金属分界线上的元素兼有金属和非金属的性质,位于此处的元素(如硼、硅、锗、砷、锑等)常被称为半金属或类金属(一般可用作半导体材料)。
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】随着原子序数的递增,元素的第一电离能呈周期性变化:同周期元素从左到右,第一电离能有逐渐_______ 的趋势,稀有气体的第一电离能最_______ ,氢和碱金属的第一电离能最_______ 。同族元素从上到下,第一电离能逐渐_______ 。
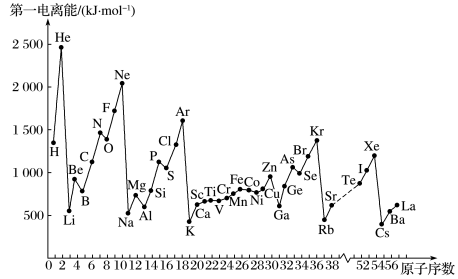

您最近半年使用:0次
【推荐2】根据有关知识,回答下列问题。
(1)符号 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。
(2)铝原子核外电子云有__________ 种不同的伸展方向,有__________ 种不同运动状态的电子。
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是__________ (填元素符号,下同),电负性最大的元素是__________ 。
(4)Be的第一电离能大于B的第一电离能,这是因为__________ 。
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:__________ 。
(6)锰元素位于第四周期第ⅦB族,请写出基础 的价层电子排布式
的价层电子排布式__________ 。
(1)符号
 所代表的含义是__________(填字母)。
所代表的含义是__________(填字母)。A. 轨道上有3个电子 轨道上有3个电子 |
B.第3个电子层 轨道有三个伸展方向 轨道有三个伸展方向 |
C. 电子云有3个伸展方向 电子云有3个伸展方向 |
| D.第3个电子层沿x轴方向伸展的p轨道 |
(3)短周期的化学元素(0族和放射性元素除外)中,第一电离能最小的元素是
(4)Be的第一电离能大于B的第一电离能,这是因为
(5)短周期元素中符合“对角线规则”的元素有Be和Al、B和Si,它们的性质分别有一定的相似性,写出
 与NaOH溶液反应的离子方程式:
与NaOH溶液反应的离子方程式:(6)锰元素位于第四周期第ⅦB族,请写出基础
 的价层电子排布式
的价层电子排布式
您最近半年使用:0次
【推荐3】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铬是24号元素,画出Cr的价层电子排布图:_______ 。
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铬是24号元素,画出Cr的价层电子排布图:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近半年使用:0次



