铜、银和硝酸银溶液组成原电池,回答下列问题:
(1)负极反应式是_______ 。
(2)正极反应式是_______ 。
(3)当有1.6g铜溶解时,银棒增重_______ g。
(1)负极反应式是
(2)正极反应式是
(3)当有1.6g铜溶解时,银棒增重
更新时间:2021-05-25 08:52:14
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】原电池工作原理:电源是将___________ 能转化为___________ 能的实用装置。发生氧化反应的一极为___________ ,发生还原反应的一极为___________ ;电子流向:___________ →___________ ;电流流向:___________ →___________ ;离子流向:阳离子→___________ ,阴离子→___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是______ (填字母代号),负极Zn发生了_____ 反应(填“氧化”或“还原”)。
(2)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:
①下列说法正确的是_______ (填字母代号)。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲______ 乙(填“>”、“<“或“=”)。
③请写出图中构成原电池的装置负极的电极反应式___________ 。
④当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为_______
(1)现有如下两个反应:A.NaOH+HCl=NaCl+H2O;B.Zn+H2SO4=ZnSO4+H2↑。上述反应中能设计成原电池的是
(2)将纯锌片和纯铜片按如图所示方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的装置负极的电极反应式
④当乙中产生1.12 L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】将锌片和铜片用导线连接后插入稀硫酸中,并在中间串联一个电流表,装置如图所示。
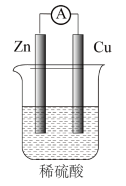
(1)该装置可以将_______ 能转化为_______ 能。
(2)装置中的负极材料是_______ 。
(3)铜片上的电极反应式是_______ ,该电极上发生了_______ (填“氧化”或“还原”)反应。
(4)稀硫酸中的SO 向
向_______ 片移动。导线中电子流向_______ 片。
(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为_______ 。

(1)该装置可以将
(2)装置中的负极材料是
(3)铜片上的电极反应式是
(4)稀硫酸中的SO
 向
向(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为稀硫酸。放电时,该电池总反应式为:Pb+PbO2+2H2SO4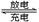 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
(1)该蓄电池的负极材料是_________ ,放电时发生_________ (填“氧化”或“还原”)反应。
(2)该蓄电池放电时,电解质溶液的酸性_________ (填“增大”、“减小”或“不变”),电解质溶液中阴离子移向_________ (填“正”或“负”)极。
(3)已知硫酸铅为不溶于水的白色沉淀,生成时附着在电极上。试写出该电池放电时,正极的电极反应_______________________________________ (用离子方程式表示)。
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为__________________________________ 。该电池工作时,外电路每流过1×103mol e-,消耗标况下氧气_________ m3。
 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:(1)该蓄电池的负极材料是
(2)该蓄电池放电时,电解质溶液的酸性
(3)已知硫酸铅为不溶于水的白色沉淀,生成时附着在电极上。试写出该电池放电时,正极的电极反应
(4)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】铝作为一种应用广泛的金属,在电化学领域发挥着举足轻重的作用。回答下列问题:
(1)某同学根据氧化还原反应: 设计如图所示的原电池:
设计如图所示的原电池:
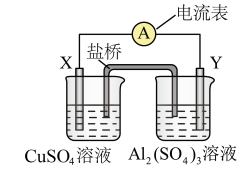
①电极X的化学式为__________ ,电极Y的化学式为________________ 。
②盐桥中的阴离子向_____ (填化学式)溶液中移动。
(2)新型电池中的铝电池类型较多。
① 是一种二次电池,可用于车载电源,其电池总反应为
是一种二次电池,可用于车载电源,其电池总反应为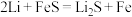 。放电时的正极反应式为
。放电时的正极反应式为______________ ,充电时,阴极的电极反应式为____________________ 。
②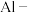 空气燃料电池可用作电动汽车的电源,该电池多使用
空气燃料电池可用作电动汽车的电源,该电池多使用 溶液为电解液。电池工作过程中电解液的
溶液为电解液。电池工作过程中电解液的
_______ (填“增大”“减小”或“不变”)。
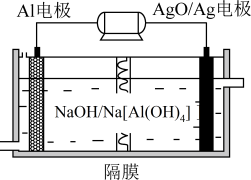
③图为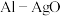 电池的原理结构示意图,这种电池可用作水下动力电源。该电池反应的化学方程式为
电池的原理结构示意图,这种电池可用作水下动力电源。该电池反应的化学方程式为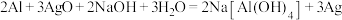 ,当电极上析出
,当电极上析出 时,电路中转移的电子为
时,电路中转移的电子为_____  。
。
(1)某同学根据氧化还原反应:
 设计如图所示的原电池:
设计如图所示的原电池:
①电极X的化学式为
②盐桥中的阴离子向
(2)新型电池中的铝电池类型较多。
①
 是一种二次电池,可用于车载电源,其电池总反应为
是一种二次电池,可用于车载电源,其电池总反应为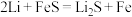 。放电时的正极反应式为
。放电时的正极反应式为②
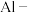 空气燃料电池可用作电动汽车的电源,该电池多使用
空气燃料电池可用作电动汽车的电源,该电池多使用 溶液为电解液。电池工作过程中电解液的
溶液为电解液。电池工作过程中电解液的
③图为
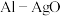 电池的原理结构示意图,这种电池可用作水下动力电源。该电池反应的化学方程式为
电池的原理结构示意图,这种电池可用作水下动力电源。该电池反应的化学方程式为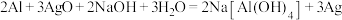 ,当电极上析出
,当电极上析出 时,电路中转移的电子为
时,电路中转移的电子为 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】人们应用原电池原理制作了多种电池,以满足不同的需要。以下各种电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息填空:
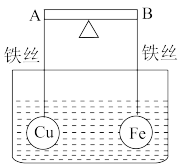
(1)如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央铁丝滴入浓CuSO4溶液,(实验过程中,不考虑铁丝反应及两球的浮力变化)一段时间后,当杠杆为绝缘体时,_______ (填 “A”或“B”,下同)端高;当杠杆为导体时, _______ 端高。
(2)铁、铜、铝是生活中使用广泛的金属,FeCl3溶液常用于腐蚀印刷电路铜板,反应过程的离子方程式为_______ ,若将此反应设计成原电池,则负极所用电极材料为_______ (填元素符号),正极反应式为_______ 。
(3)科学家利用下图所示电池装置可以将CO2转化为气体燃料CO。
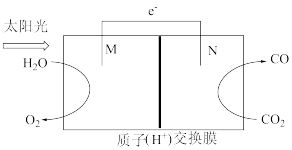
①该装置工作时,N电极为_______ (填“正极”或“负极)。
②外电路中,电子流向为_______ (填“M→N”或“N→M”)。
③理论上生成1mol O2的同时,流经导线的电子有_______ mol。
(1)如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中央铁丝滴入浓CuSO4溶液,(实验过程中,不考虑铁丝反应及两球的浮力变化)一段时间后,当杠杆为绝缘体时,

(2)铁、铜、铝是生活中使用广泛的金属,FeCl3溶液常用于腐蚀印刷电路铜板,反应过程的离子方程式为
(3)科学家利用下图所示电池装置可以将CO2转化为气体燃料CO。

①该装置工作时,N电极为
②外电路中,电子流向为
③理论上生成1mol O2的同时,流经导线的电子有
您最近一年使用:0次



