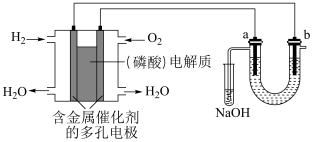
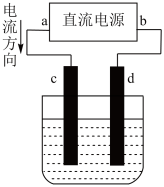
臭氧(O3)是一种强氧化剂,常用于消毒灭菌等,可用下图电解稀硫酸制得O3,下列说法正确的是
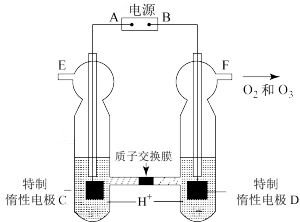

| A.图中特制惰性电极C为阳极 |
| B.电解一段时间后停止电解,溶液的pH显著变大 |
| C.电解开始后电子的移动方向为:A→C→D→B |
D.电解一段时间后E、F处分别收集到xL和yL气体(标准状况),则F处收集的气体中O3所占的体积分数为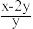 (忽略O3的分解) (忽略O3的分解) |
更新时间:2021-05-31 06:51:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】最近我国科学家设计了一种电化学协同处理氮、硫的氧化物的装置如图所示,实现对烟气的净化处理,并得到合成氨的原料。
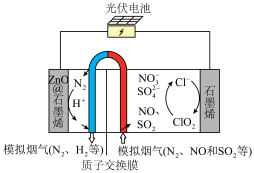
下列叙述错误 的是

下列叙述
| A.采用石墨烯作电极材料,能够提高电池工作效率 |
| B.ZnO@石墨烯极连接光伏电池的负极 |
C.石墨烯电极表面的电极反应为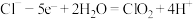 |
| D.协同反应中,NO被还原为氮气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.1 mol N2与4 mol H2混合充分反应,则反应中转移的电子数目为6 mol |
| B.反应2Mg(s)+CO2(g) =C(s)+2MgO(s) 能自发进行,则该反应的ΔH>0 |
| C.在稀溶液中:H+(aq)+OH-(aq) =H2O(l) ΔH= -57.3kJ·mol−1,若将含0.5 mol H2SO4的浓硫酸与1 L 1.0 mol·L−1 的NaOH溶液混合,放出的热量大于57.3 kJ |
| D.电解精炼铜过程中,若阳极质量减少32 g,则电路中转移电子数目为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】甲装置中所含的是物质的量之比为1∶2的CuSO4和NaCl的混合溶液,电解过程中溶液的pH值随时间t变化的示意图如乙示(不考虑电解产物可能与水的反应)。试分析下列叙述中正确的是


A.是该混合溶液中的SO 导致了A点溶液的pH值小于B点 导致了A点溶液的pH值小于B点 |
| B.整个电解过程中,阴极和阳极产生的气体体积之比大于2 |
| C.AB线段与BC线段在阴极上发生的反应是相同的即:Cu2++2e-=Cu |
| D.在整个电解的过程中不会出现少量的Cu(OH)2沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在水中加等物质的量的Ag+,Pb2+,Na+, ,
, ,Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为
,Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为
 ,
, ,Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为
,Cl-,该溶液放在用惰性电极做电极的电解槽中,通电片刻,则氧化产物与还原产物质量比为| A.35.5:108 | B.71:207 | C.108:35.5 | D.8:1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】利用电解原理将含硫污染物SO2资源转化大规模制备高质高值的氢气和硫酸的技术路线,如下图所示,下列说法正确的是


| A.N与电源正极相连 |
| B.生成1 mol的气体,需要消耗11.2 LSO2(标况下) |
| C.H+通过质子交换膜从b室移向c室 |
| D.连接M的电极反应为2HI-2e-=2H++I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】浮选凝聚法处理酸性污水的工作原理如图所示,下列说法不正确的是


| A.通入甲烷的石墨电极的电极反应式为:CH4+10OH--8e-═CO32-+7H2O |
| B.通入空气的石墨电极的电极反应式为O2+2CO2+4e-═2CO32- |
| C.Fe电极的电极反应式为:Fe-2e-═Fe2+ |
| D.为增强污水的导电能力,可向污水中加入适量工业用食盐 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据所学的反应原理知识进行判断,下列结论或推断正确的是
A.用惰性电极电解 溶液,两极均收集到标况下气体11.2L,可得到32克铜 溶液,两极均收集到标况下气体11.2L,可得到32克铜 |
B.恒温密闭容器内发生反应: , , 的体积分数不变时说明反应达到平衡状态 的体积分数不变时说明反应达到平衡状态 |
| C.变黑的银饰品放入盛食盐水的铝碗中恢复如新,利用了原电池原理,铝做正极 |
D.已知酸性: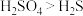 ,则反应 ,则反应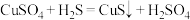 不能发生 不能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】工业上可用惰性电极电解酸性 溶液来制备
溶液来制备 ,电解装置如图所示,隔膜的作用是隔离两极产生的气体,并传递离子,下列说法正确的是
,电解装置如图所示,隔膜的作用是隔离两极产生的气体,并传递离子,下列说法正确的是

 溶液来制备
溶液来制备 ,电解装置如图所示,隔膜的作用是隔离两极产生的气体,并传递离子,下列说法正确的是
,电解装置如图所示,隔膜的作用是隔离两极产生的气体,并传递离子,下列说法正确的是
A.a电极接电源正极,电极产物有 |
B.如果隔膜采用阳离子膜,电解完成后阴极区溶液的 将增大 将增大 |
C.采用阴离子隔膜或阳离子隔膜都能使 达到同样的理论利用率 达到同样的理论利用率 |
| D.阴阳两极产生的气体体积比为:1∶4 |
您最近一年使用:0次