已知氮元素是地球大气中含量最多的元素,请完成下列有关问题:
(1)写出N2的电子式:__ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是__ (填字母)。
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是__ (填字母)。
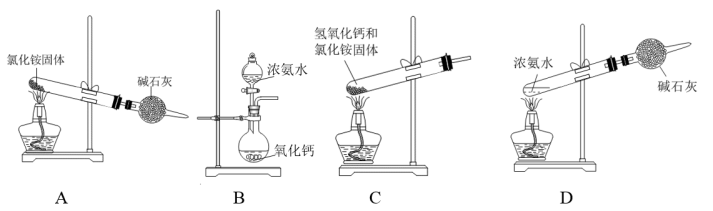
选取了正确的制备装置后,若想收集一试管氨气,可用___ 排空气法。
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓__ 溶液、加热,再用__ 试纸检验产生的气体,若试纸变蓝则表明含有 。
。
(1)写出N2的电子式:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮,则下列属于固氮过程的是
A.NH3经过催化氧化生成NO
B.NH3和HNO3反应生成NH4NO3
C.N2和H2在一定条件下反应生成NH3
D.雷雨闪电时空气中的N2和O2化合生成NO
(3)如图是实验室制取氨气的装置和选用试剂,其中错误的是

选取了正确的制备装置后,若想收集一试管氨气,可用
(4)NH4HCO3是常用的铵态氮肥,在施用时若受热会释放出氨气而降低肥效。检验其中
 的方法是将固体溶于水配制浓溶液,加入浓
的方法是将固体溶于水配制浓溶液,加入浓 。
。
更新时间:2021-06-02 11:02:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】通常情况下,氮气很不活泼,其原因是:N2分子内部具有N≡N结构,键能很大,不容易被破坏。
(1)在一定条件下也可以与其他物质反应,有两种气体,一种能够氧化N2,一种能够还原N2,请分别写出这两个反应的化学方程式:
①氧化N2:_______ ;
②还原N2:_______ 。
(2)Mg可以在N2中燃烧生成氮化镁,写出该反应的化学方程式_______ ,在该反应中N2表现_______ 性。
(3)已知氮化镁可以与水反应生成氢氧化镁和氨气,写出该反应的化学反应方程式_______ 。
(1)在一定条件下也可以与其他物质反应,有两种气体,一种能够氧化N2,一种能够还原N2,请分别写出这两个反应的化学方程式:
①氧化N2:
②还原N2:
(2)Mg可以在N2中燃烧生成氮化镁,写出该反应的化学方程式
(3)已知氮化镁可以与水反应生成氢氧化镁和氨气,写出该反应的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。Ⅰ. 氮在自然界中的转化是一个复杂的过程,如图所示的氮循环是生态系统物质循环的重要组成部分。___________ (填转化序号)。
(2)循环图中转化④的反应之一可表示为NH +2O2
+2O2  X+2H++H2O,其中X为
X+2H++H2O,其中X为___________ 。
(3)下列有关氮循环说法正确的是___________。
Ⅱ.NH3和HNO3是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。___________ 。___________ 性质,氧化炉中反生反应的化学方程式是___________ 。
(6)将吸收塔中制备好的浓硝酸进行储存运输,可以选择___________作为罐体材料。
(7)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体。现有NO2和NO混合的气体(体积比为1∶1),处理3 mol 混合气体需要的NH3 为___________ mol。
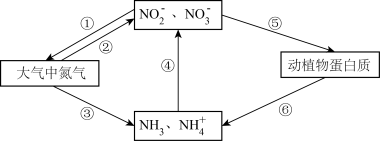
(2)循环图中转化④的反应之一可表示为NH
 +2O2
+2O2  X+2H++H2O,其中X为
X+2H++H2O,其中X为(3)下列有关氮循环说法正确的是___________。
| A.图中转化②③④都属于氮的固定 | B.雷雨天气容易发生转化②的过程 |
| C.只有氮、氧两种元素参加了氮循环 | D.植物吸收的无机氮主要是NH 和NO 和NO |
Ⅱ.NH3和HNO3是重要的工业产品,下图是合成氨和氨氧化制硝酸的工艺流程。


(6)将吸收塔中制备好的浓硝酸进行储存运输,可以选择___________作为罐体材料。
| A.铜 | B.铁 | C.铝 | D.银 |
(7)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体。现有NO2和NO混合的气体(体积比为1∶1),处理3 mol 混合气体需要的NH3 为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氮元素在地球上含量丰富,是构成生命体的基本元素之一、回答下列问题:
(1)N元素在元素周期表中的位置为_______ 。
(2)制备下列物质属于固氮的是 _______。
(3)受到阳光照射浓硝酸会变黄的原因是 _______ ( 用化学方程式表示)。
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是_______ 。
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: _______ 。
(5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是_______ 。
②电解质溶液中OH- 离子向_______ 移动 (填“电极a”或“电极b”)。
③电极b的电极反应式为_______ 。
(1)N元素在元素周期表中的位置为
(2)制备下列物质属于固氮的是 _______。
| A.用氮气和氢气合成氨 |
| B.分离液态空气获得氮气 |
| C.用NH4Cl和熟石灰制备氨气 |
| D.NO2溶于水得到HNO3 |
(4)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
①氮的氧化物是空气的主要污染物,下列环境问题与氮的氧化物排放有关的是
A.酸雨 B.光化学烟雾
C.白色污染 D.水土流失
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式: (5)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH- 离子向
③电极b的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫和氮是两种重要的元素,它们的氧化物又是造成空气污染的主要物质。
(1)汽车尾气含有NO、CO等多种污染物,是城市的污染源。
①用化学方程式表示产生NO的原因___ 。
②治理尾气方法是加装催化转化装置,使NO和CO反应转化为无污染的两种气体,发生反应的化学方程式是___ 。
(2)工业上产生的NO2可用NH3在一定条件下消除污染。
①写出此反应的化学方程式___ 。
②在标准状况下,消耗NO233.6L,则此反应的氧化产物比还原产物多___ g。
(3)工业上为了减少燃煤过程中SO2的排放,向燃煤中加入生石灰,其产物可作建筑材料。写出有关反应的化学方程式___ 。
(1)汽车尾气含有NO、CO等多种污染物,是城市的污染源。
①用化学方程式表示产生NO的原因
②治理尾气方法是加装催化转化装置,使NO和CO反应转化为无污染的两种气体,发生反应的化学方程式是
(2)工业上产生的NO2可用NH3在一定条件下消除污染。
①写出此反应的化学方程式
②在标准状况下,消耗NO233.6L,则此反应的氧化产物比还原产物多
(3)工业上为了减少燃煤过程中SO2的排放,向燃煤中加入生石灰,其产物可作建筑材料。写出有关反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】依据下图中氮元素及其化合物的转化关系,回答下列问题。

(1)过程II是氨的催化氧化,其化学方程式是_______ 。
(2)过程IV的化学方程式为_______ 。
(3)过程V可对NO2进行尾气处理,产物除NaNO2外,还有两种常见物质(其中一种是气体),反应的化学方程式为_______ 。
(4)一定条件下,在2L的密闭容器中,进行N2和H2合成NH3的反应。反应过程中测得各气体的物质的量如下图所示。回答下列问题:

①用H2表示0~2min内该反应的平均速率为_______ 。
②第2min末,N2的转化率为_______ 。
③能说明该反应已经达到平衡状态的是_______ 。
a.气体的密度不随时间而改变
b.体系总物质的量不随时间而改变
c.N2和H2的浓度比为1:3
d.H2的体积百分数保持恒定

(1)过程II是氨的催化氧化,其化学方程式是
(2)过程IV的化学方程式为
(3)过程V可对NO2进行尾气处理,产物除NaNO2外,还有两种常见物质(其中一种是气体),反应的化学方程式为
(4)一定条件下,在2L的密闭容器中,进行N2和H2合成NH3的反应。反应过程中测得各气体的物质的量如下图所示。回答下列问题:

①用H2表示0~2min内该反应的平均速率为
②第2min末,N2的转化率为
③能说明该反应已经达到平衡状态的是
a.气体的密度不随时间而改变
b.体系总物质的量不随时间而改变
c.N2和H2的浓度比为1:3
d.H2的体积百分数保持恒定
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】 、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1) 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为_____________________________________ 。
(2)NO和 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为
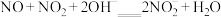
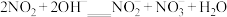
①下列措施能提高尾气中NO和NO2去除率的有___________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是___________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是__________________ (填化学式)。
 、NO和
、NO和 等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。(1)
 的处理。
的处理。 是硝酸生产中氨催化氧化的副产物,用特种催化剂能使
是硝酸生产中氨催化氧化的副产物,用特种催化剂能使 分解。
分解。 与
与 在加热和催化剂作用下生成
在加热和催化剂作用下生成 的化学方程式为
的化学方程式为(2)NO和
 的处理。已除去
的处理。已除去 的硝酸尾气可用NaOH溶液吸收,主要反应为
的硝酸尾气可用NaOH溶液吸收,主要反应为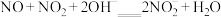
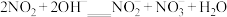
①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到
 晶体,该晶体中的主要杂质是
晶体,该晶体中的主要杂质是
您最近一年使用:0次



