A、B、C、D、E均是短周期元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素。请回答:
(1)E在元素周期表中的位置是_______ 。
(2)AB2的电子式是_______ ;C的最高价氧化物的水化物与D的氧化物反应的化学方程式是_______ 。
(3)A、B、E的简单氢化物的稳定性从强到弱顺序是_______ (用化学式回答)
(4)利用非金属单质的置换反应比较E与硫的氧化性强弱,可采用的方法及预期出现的现象是_______ 。
(5)“84消毒液”的主要成分是CEB,“84消毒液”不可与酸性清洁剂混用的原因是:_______ (用离子方程式表示)。
(1)E在元素周期表中的位置是
(2)AB2的电子式是
(3)A、B、E的简单氢化物的稳定性从强到弱顺序是
(4)利用非金属单质的置换反应比较E与硫的氧化性强弱,可采用的方法及预期出现的现象是
(5)“84消毒液”的主要成分是CEB,“84消毒液”不可与酸性清洁剂混用的原因是:
更新时间:2021-06-15 17:40:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C为短周期元素,在周期表中所处位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数。B原子核内质子数和中子数相等。

(1)写出元素名称:A_________ 、B_________ 、C_________ 。
(2)B位于元素周期表第_________ 周期第_________ 族。
(3)比较B、C的原子半径:B___________ C。写出A的气态氢化物与B的最高价氧化物对应的水化物反应的化学方程式________________________ 。

(1)写出元素名称:A
(2)B位于元素周期表第
(3)比较B、C的原子半径:B
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A原子核内只有1个质子;B原子半径是其所在主族中最小的,B的最高价氧化物对应的水化物的化学式为HBO3;C原子最外层的电子数比次外层的多4;C的简单阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C;C、E同主族。回答下列问题:
(1)B在元素周期表中的位置为______________________ 。
(2)B、C、D、E形成的简单离子半径由大到小的关系是________________ (用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程______________________ 。
(4)由A、B、C三种元素形成的常见的离子化合物的化学式为___________ ,该化合物的水溶液中各离子的浓度由大到小的顺序为______________________ 。
(5)化合物D2EC3在一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为______________________ 。
(1)B在元素周期表中的位置为
(2)B、C、D、E形成的简单离子半径由大到小的关系是
(3)用电子式表示化合物D2C的形成过程
(4)由A、B、C三种元素形成的常见的离子化合物的化学式为
(5)化合物D2EC3在一定条件下可以发生分解反应生成两种盐,其中一种产物为无氧酸盐,则此反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】为了清理路面积雪,人们常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol 电子。
(1)该融雪剂的化学式是________ ,该物质中化学键类型是________ ,电子式是________________ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是____________ ;D与E能形成一种结构类似于CO2的三原子分子,且每个原子都达到了8e-稳定结构,该分子的电子式为____________ ,化学键类型为________________ (填“离子键”、“非极性共价键”或“极性共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成________ ,其化学键类型为________ ;加热时生成________ ,其化学键类型为________________ 。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】前四周期元素X、Y、Z、M的原子序数依次增大。元素X和铝在元素周期表中具有特殊的“对角线”关系,单质及化合物的性质十分相似;Y原子半径在短周期主族元素中最大;Z元素有多种同素异形体,其中一种为正四面体结构,易自燃;M基态原子未成对电子数在同周期元素中最多。
请回答下列问题:
(1)元素Z在周期表中的位置是_______ 。
(2)元素X的氧化物能与Y的氧化物的水化物形成的溶液反应,生成一种四配位化合物,写出该化合物的化学式________ 。
(3)元素Y的氢化物被称作“万能还原剂”,具有强的还原性。其电子式为______ ,遇水可发生反应的化学方程式为________ 。
(4)元素M的名称为_______ ,其+3价氧化物与铝反应的化学方程式为_______ 。
请回答下列问题:
(1)元素Z在周期表中的位置是
(2)元素X的氧化物能与Y的氧化物的水化物形成的溶液反应,生成一种四配位化合物,写出该化合物的化学式
(3)元素Y的氢化物被称作“万能还原剂”,具有强的还原性。其电子式为
(4)元素M的名称为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,回答下列问题。
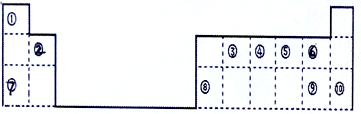
(1)⑨在周期表中的位置是____________________________ ;请写出⑧单质与⑦最高价氧化物对应的水化物反应的离子方程式________________________________ 。
(2)⑥对应的气态氢化物沸点高于同主族元素对应的气态氢化物,原因是_____________________ ;
(3)①③两元素可以形成原子个数比2 :1的化合物X,X的电子式为____________ ,X发生加聚反应的方程式为___________________________________________ 。
(4)实验室制取④的最简单氢化物的化学反应方程式是:___________________________________ ;
(5)由①③⑤三种元素组成的化合物之一Z,是生活中常见的有机化合物,它具有特殊的香味,它能使加热变黑后的铜丝恢复亮红色,并闻到刺激性气味。请用化学方程式解释:____________________ 。

(1)⑨在周期表中的位置是
(2)⑥对应的气态氢化物沸点高于同主族元素对应的气态氢化物,原因是
(3)①③两元素可以形成原子个数比2 :1的化合物X,X的电子式为
(4)实验室制取④的最简单氢化物的化学反应方程式是:
(5)由①③⑤三种元素组成的化合物之一Z,是生活中常见的有机化合物,它具有特殊的香味,它能使加热变黑后的铜丝恢复亮红色,并闻到刺激性气味。请用化学方程式解释:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】X、Y、Z、W、M、N为原子序数依次增大的六种短周期元素,常温下,六种元素的常见单质中三种为气体,三种为固体。X与M,W与N分别同主族,在周期表中X是原子半径最小的元素,且X能与Y、Z、W分别形成电子数相等的三种分子,Z、W的最外层电子数之和与M的核外电子总数相等。试回答下列问题:
(1)N元素在周期表中的位置为____ 。
(2)X、Z形成的含18电子的化合物的化学式为____ 。
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式____ 。
(4)X和W组成的化合物中,俗称绿色氧化剂的是____ (填化学式),此化合物可将碱性工业废水中的CN-氧化,生成碳酸盐和氨气,相应的离子方程式为____ 。
(1)N元素在周期表中的位置为
(2)X、Z形成的含18电子的化合物的化学式为
(3)由X、Z、W、N四种元素组成的一种离子化合物A,已知A既能与盐酸反应,又能与氯水反应,写出A与足量盐酸反应的离子方程式
(4)X和W组成的化合物中,俗称绿色氧化剂的是
您最近一年使用:0次
【推荐1】W、X、Y为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为3s23p4,X的电离能数据如下表所示。
(1)Y在元素周期表中的位置是___________ 。
(2)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
资料:ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为 ,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一,水化物的M—O—H结构中,成键原子电负性差异越大,所形成的化学键越容易断。
①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响M—O—H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈___________ (填“酸”或“碱”)性,依据是___________ 。
②W和X的最高价氧化物对应的水化物中,碱性较强的是___________ (写化学式),结合资料说明理由:___________ 。
| 电离能 |  |  |  |  | … |
 | 738 | 1451 | 7733 | 10540 | … |
(2)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
资料:ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为
 ,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一,水化物的M—O—H结构中,成键原子电负性差异越大,所形成的化学键越容易断。
①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响M—O—H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈
②W和X的最高价氧化物对应的水化物中,碱性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1。请回答下列问题:

(1)四种元素的所有化合价中,最低负化合价为______ 价,最高正化合价为_____ 价。
(2)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有消毒杀菌作用,其化学式为_________ ;化合物乙是一种离子化合物,常用作化肥,其化学式为________ 。
(3)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确,说明理由:____________________ 。
(4)元素Y和W能形成一种化合物YW3。YW3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:________________ 。

(1)四种元素的所有化合价中,最低负化合价为
(2)甲和乙分别是由W、X、Y、Z四种元素中的三种元素组成的常见化合物,化合物甲具有消毒杀菌作用,其化学式为
(3)HYO3的酸性比HWO强,有人据此认为Y的非金属性强于W,你认为这种看法是否正确,说明理由:
(4)元素Y和W能形成一种化合物YW3。YW3能发生水解反应生成一种弱碱和一种弱酸,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E、F、G7种元素,它们的核电荷数依次增大,且A~E都为短周期元素。其中G元素是1826年一位法国青年科学家发现的,他在研究海水制盐时向剩余的副产物(苦卤)中通入氯气后发现溶液的颜色变深,经过一步提取可得红棕色液体,有刺激性气味;A为非金属元素,A和F属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上的电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)写出下列元素的名称:A:_____ ,C:_____ ,E:_____ ,G:_____ 。
(2)G元素在周期表中的位置为:______ ;其价电子排布图为:______ 。
(3)由A、B、C、D、F五种元素组成的一种化合物为______ (写化学式),并写出该物质的一种用途______ 。
(4)已知由D和E形成的一种化合物D2E2是一种橙黄色液体遇水剧烈反应,产生能使品红溶液褪色的气体。
①D2E2中E为_____ 价;且该物质为_____ (填”极性”或“非极性”)分子。
②写出D2E2与水反应的化学方程式______ 。
(1)写出下列元素的名称:A:
(2)G元素在周期表中的位置为:
(3)由A、B、C、D、F五种元素组成的一种化合物为
(4)已知由D和E形成的一种化合物D2E2是一种橙黄色液体遇水剧烈反应,产生能使品红溶液褪色的气体。
①D2E2中E为
②写出D2E2与水反应的化学方程式
您最近一年使用:0次



