已知固体A是常见的金属,可发生以下转化:
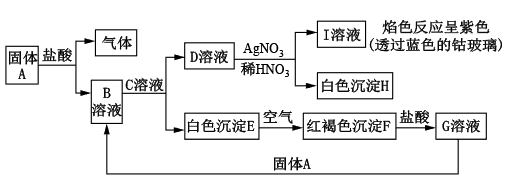
试回答下列问题。
(1)B的化学式为_______ ,D的化学式为_______ 。
(2)写出由E转变成F的化学方程式_______ 。
(3)常用来鉴别G溶液中所含金属阳离子的试剂是_______ ,向G溶液中加入A,发生反应的离子方程式为_______ 。

试回答下列问题。
(1)B的化学式为
(2)写出由E转变成F的化学方程式
(3)常用来鉴别G溶液中所含金属阳离子的试剂是
更新时间:2021-06-05 23:19:48
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碳酸亚铁晶体[ 为白色固体,不溶于水,干燥品在空气中稳定、湿品在空气中缓慢氧化为
为白色固体,不溶于水,干燥品在空气中稳定、湿品在空气中缓慢氧化为 呈茶色]可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色]可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
(1)实验室利用 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:

①方框内为制取 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是_______ (填字母)。
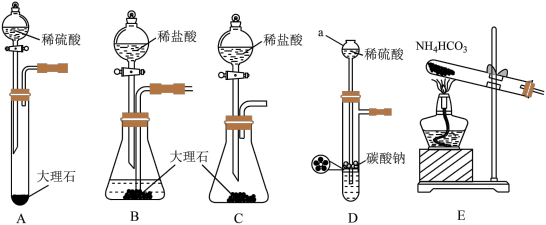
②装置D中仪器a的名称是_______ 。
③根据①的选择,装置甲中试剂a的名称是_______ 。
(2) 的制备,步骤如下:
的制备,步骤如下:
通入一段时间 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。
①生成 的离子方程式为
的离子方程式为_______ 。
②装置丙的作用是_______ 。
(3)某同学查阅资料得知,煅烧 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、
中依次加入试剂:稀硫酸、_______ 和_______ ;然后再_______ (填操作)、灼烧,即可得到 。
。
(4)草酸亚铁和碳酸亚铁晶体均能受热分解。称取3.60 g ,用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。
,用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。
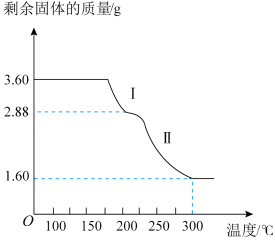
①过程Ⅰ发生反应的化学方程式为_______ 。
②300℃时剩余固体只有一种且是铁的氧化物,则其化学式为_______ 。
 为白色固体,不溶于水,干燥品在空气中稳定、湿品在空气中缓慢氧化为
为白色固体,不溶于水,干燥品在空气中稳定、湿品在空气中缓慢氧化为 呈茶色]可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:
呈茶色]可用作阻燃剂、动物饲料铁添加剂、补血剂等。回答下列问题:(1)实验室利用
 溶液和
溶液和 溶液制备
溶液制备 ,实验装置(夹持仪器已省略)如图所示:
,实验装置(夹持仪器已省略)如图所示:
①方框内为制取
 的装置,下列装置和药品较为适宜的是
的装置,下列装置和药品较为适宜的是
②装置D中仪器a的名称是
③根据①的选择,装置甲中试剂a的名称是
(2)
 的制备,步骤如下:
的制备,步骤如下:通入一段时间
 后,向
后,向 溶液中加入过量
溶液中加入过量 溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到
溶液,搅拌,反应后过滤,将沉淀洗涤、干燥,得到 。
。①生成
 的离子方程式为
的离子方程式为②装置丙的作用是
(3)某同学查阅资料得知,煅烧
 的产物中含有+2价铁元素,于是他设计了由
的产物中含有+2价铁元素,于是他设计了由 制备
制备 的方案。先向
的方案。先向 中依次加入试剂:稀硫酸、
中依次加入试剂:稀硫酸、 。
。(4)草酸亚铁和碳酸亚铁晶体均能受热分解。称取3.60 g
 ,用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。
,用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。
①过程Ⅰ发生反应的化学方程式为
②300℃时剩余固体只有一种且是铁的氧化物,则其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
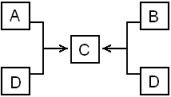
【推荐2】在下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A.D为金属单质,其他为化合物。试推断:

(1)写出下列物质的化学式:A:________ B:________ G:________
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式________________________________________
C→E的化学方程式________________________________________
H→I的化学方程式________________________________________

(1)写出下列物质的化学式:A:
(2)写出下列反应的化学方程式或离子方程式:
C→F的离子方程式
C→E的化学方程式
H→I的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E是中学化学阶段学过的常见物质。根据如下转化图填空。
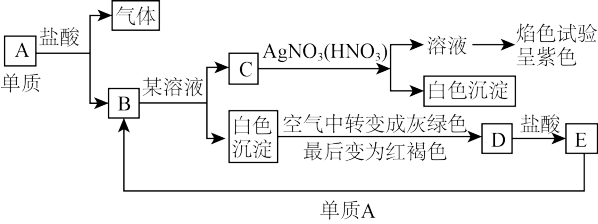
(1)写出C溶液溶质的化学式:______ 。
(2)溶液E中含有的金属离子检验原理为______ (用离子方程式表示)。
(3)写出生成D的化学方程式______ 。
(4)写出B→C的化学方程式______ ;
(5)写出E→B的离子方程式______ 。
(6)写出E溶液腐蚀覆铜板的离子方程式______ 。

(1)写出C溶液溶质的化学式:
(2)溶液E中含有的金属离子检验原理为
(3)写出生成D的化学方程式
(4)写出B→C的化学方程式
(5)写出E→B的离子方程式
(6)写出E溶液腐蚀覆铜板的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】在下图所示的物质转化关系中。 C、G、I、M为常见单质,G和M化合可生成最常见液体A,E为黑色粉末,F的焰色反应为黄色,K为白色沉淀,N为红褐色沉淀,I为黄绿色气体,化合物B的摩尔质量为24 g ·mol-1。(部分生成物和反应条件未列出)
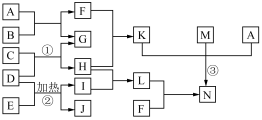
(1) M的化学式为______________ 。
(2) A的电子式为______________ 。
(3) 反应②的离子方程式为____________________________________ 。
(4) 反应③的化学方程式为____________________________________ 。

(1) M的化学式为
(2) A的电子式为
(3) 反应②的离子方程式为
(4) 反应③的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。

请回答下列问题:
(1)A在B中燃烧的现象是_______________ 。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是___________ 。
(3)G+J→M的离子方程式是_________________________ 。
(4)Y受热分解的化学方程式是_________________________ 。

请回答下列问题:
(1)A在B中燃烧的现象是
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是
(3)G+J→M的离子方程式是
(4)Y受热分解的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
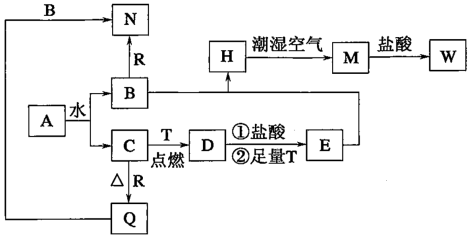
(1)写出下列物质的化学式:A:_______ ,D:_______ ,R:_______ 。
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:_______ ;
B和R反应生成N的离子方程式:_______ ;
D与盐酸反应的离子方程式:_______ 。
(3)向W溶液中加入一定量T后,为检验所得溶液中金属阳离子,甲、乙两位同学做了如下实验:甲同学取出少量反应后溶液,加入少量H2O2,再滴加几滴KSCN溶液,发现溶液显血红色,由此得出结论有Fe2+;乙同学取出少量反应后溶液,加入少量酸性KMnO4溶液,发现酸性KMnO4溶液褪色,由此得出结论有Fe2+。丙同学看了实验过程后认为甲、乙同学的结论都有问题,你觉得丙同学判断甲、乙同学结论的依据是:
甲同学:_______ ;
乙同学:_______ 。

(1)写出下列物质的化学式:A:
(2)按要求写下列反应方程式:
H在潮湿空气中变成M的过程中的化学方程式:
B和R反应生成N的离子方程式:
D与盐酸反应的离子方程式:
(3)向W溶液中加入一定量T后,为检验所得溶液中金属阳离子,甲、乙两位同学做了如下实验:甲同学取出少量反应后溶液,加入少量H2O2,再滴加几滴KSCN溶液,发现溶液显血红色,由此得出结论有Fe2+;乙同学取出少量反应后溶液,加入少量酸性KMnO4溶液,发现酸性KMnO4溶液褪色,由此得出结论有Fe2+。丙同学看了实验过程后认为甲、乙同学的结论都有问题,你觉得丙同学判断甲、乙同学结论的依据是:
甲同学:
乙同学:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】金属A能够被磁铁所吸引.A及其A的化合物之间有如下的转化关系:

(1)写出A、C的化学式:A_____ ;C_____ .
(2)检验B中阳离子的试剂是_____ .
(3)写出下列反应的化学方程式或离子方程式:
A→D 的离子方程式_____
E→C 的化学方程式_____

(1)写出A、C的化学式:A
(2)检验B中阳离子的试剂是
(3)写出下列反应的化学方程式或离子方程式:
A→D 的离子方程式
E→C 的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】氧化锌在工业和生活中的运用非常广泛,以闪锌矿(主要成分为ZnS,含有少量FeS和SiO2)为原料制备活性氧化锌的工艺流程如下,请回答下列问题:

(1)浸取前,将闪锌矿粉碎的目的是_______________ 。
(2)矿渣中除了有淡黄色的物质,还有_________ (填化学式);浸取时FeS发生反应的离子方程式为_______________ 。
(3)加入铁粉的目的是__________ ,能循环利用的无机物是______________ (填化学式)。
(4)生成ZnCO3·2Zn(OH)2的离子方程式为_________________ 。
(5)有机萃取利TBP能将氯化亚铁和氯化锌分离的原因是___________________ 。
(6)工业上常采用Femton氧化法去除度水中的有机物,即向废水中加入H2O2以FeCl2作催化剂,产生具有强氧化性的羟基自由基(·OH)来氧化降解水中的有机物(TOC)。
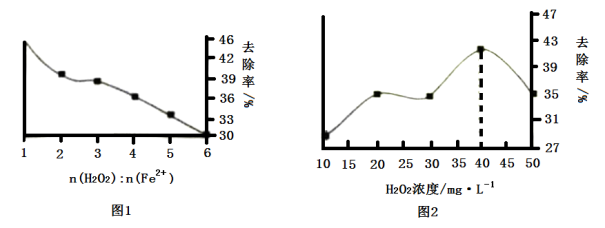
①其他条件一定时,n(H2O2):n(Fe2+ )的值对TOC去除效果的影响如图1所示,当废水中TOC的去除率最大时,n(H2O2): n(Fe2+)=_________ 。
②在酸性条件下,H2O2的加入量对TOC的去除效果如图2所示,当TOC的去除效果最好时,H2O2的物质的量浓度c(H2O2)=_______ (保留三位有效数字)。

(1)浸取前,将闪锌矿粉碎的目的是
(2)矿渣中除了有淡黄色的物质,还有
(3)加入铁粉的目的是
(4)生成ZnCO3·2Zn(OH)2的离子方程式为
(5)有机萃取利TBP能将氯化亚铁和氯化锌分离的原因是
(6)工业上常采用Femton氧化法去除度水中的有机物,即向废水中加入H2O2以FeCl2作催化剂,产生具有强氧化性的羟基自由基(·OH)来氧化降解水中的有机物(TOC)。

①其他条件一定时,n(H2O2):n(Fe2+ )的值对TOC去除效果的影响如图1所示,当废水中TOC的去除率最大时,n(H2O2): n(Fe2+)=
②在酸性条件下,H2O2的加入量对TOC的去除效果如图2所示,当TOC的去除效果最好时,H2O2的物质的量浓度c(H2O2)=
您最近一年使用:0次