含氮化合物对环境、生产和人类活动有很大影响。
(1)氨气具有还原性。将氨气通入灼热的氧化铜固体中,现象是_______ ;化学方程式是_______ 。
(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3。该反应中氧化剂与还原剂的物质的量之比为_______ ,NF3在空气中泄漏时很容易被观察到,原因是(用化学方程式表示)_______ 。
(3)火箭燃料偏二甲肼C2H8N2与N2O4反应放出大量的热,生成无毒、无污染的气体和水。1 mol C2H8N2完全反应转移的电子数是_______ 。
(1)氨气具有还原性。将氨气通入灼热的氧化铜固体中,现象是
(2)NF3为无色、无味的气体,在潮湿的环境中易变质生成HF、NO、HNO3。该反应中氧化剂与还原剂的物质的量之比为
(3)火箭燃料偏二甲肼C2H8N2与N2O4反应放出大量的热,生成无毒、无污染的气体和水。1 mol C2H8N2完全反应转移的电子数是
更新时间:2021-06-19 16:17:31
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有下列9种物质:①CuSO4·5H2O、②铜、③Na2O、④CO2、⑤NH3、⑥CaCO3、⑦稀硫酸、⑧淀粉溶液、⑨NaHSO4固体,根据要求填空(填序号)
(1)写出⑤的催化氧化的化学方程式___________ 。
(2)属于电解质的是___________ ;属于非电解质的是___________ 。
(3)在标准状况下,相同体积的④和⑤,其原子个数之比为___________ 。
(4)写出⑨在水中的电离方程式___________ 。
(5)写出②与浓硝酸反应的化学方程式___________ 。
(1)写出⑤的催化氧化的化学方程式
(2)属于电解质的是
(3)在标准状况下,相同体积的④和⑤,其原子个数之比为
(4)写出⑨在水中的电离方程式
(5)写出②与浓硝酸反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应(夹持仪器略去)。
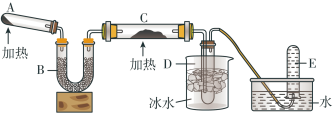
(1)A中装有氯化铵和氢氧化钙的混合物,发生反应的化学方程式是___________ ;
(2)B中加入的是碱石灰,其作用是___________ ;
(3)实验时C中观察到的现象是___________ ,发生反应的化学方程式是_____________ ;
(4)试管D中收集到的物质是___________ ,向其中滴加酚酞试液,溶液变_____ 色,原因是___________________ (用电离方程式表示)。

(1)A中装有氯化铵和氢氧化钙的混合物,发生反应的化学方程式是
(2)B中加入的是碱石灰,其作用是
(3)实验时C中观察到的现象是
(4)试管D中收集到的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
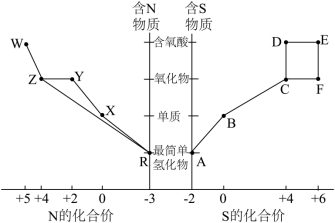
【推荐3】I.元素的“价—类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式___________ 。
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是___________ 。
(3)写出物质E的浓溶液与碳单质反应的化学方程式:___________ 。
(4)写出物质Z与水反应的离子方程式:___________ ,当反应消耗0.3mol物质Z时,转移电子数为___________ 。
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
II.粗盐中含有泥沙及 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:
(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为___________ 。
(7)加盐酸调溶液pH的目的是___________ 。
(1)写出实验室利用两种固体物质加热制备物质R的化学方程式
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是
(3)写出物质E的浓溶液与碳单质反应的化学方程式:
(4)写出物质Z与水反应的离子方程式:
(5)下列有关图中所示含N、S物质的叙述,正确的是___________(填标号)。
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.图中所示的物质中,只有W、D、E属于电解质 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
| D.Z、C、F均能与NaOH溶液反应,都是酸性氧化物 |
II.粗盐中含有泥沙及
 、
、 、
、 等杂质,其提纯过程一般经过以下流程:
等杂质,其提纯过程一般经过以下流程: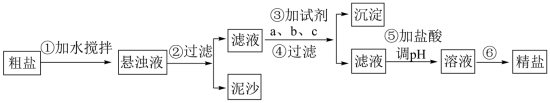
 溶液、
溶液、 溶液等药品以及必备的实验仪器若干。请回答下列问题:
溶液等药品以及必备的实验仪器若干。请回答下列问题:(6)操作③按a、b、c顺序依次加入过量的试剂。若a为NaOH溶液,则c为
(7)加盐酸调溶液pH的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列问题:
(1)下列物质属于化合物但不属于电解质的是____ (填标号)。
(2)工业上制取金刚砂的反应为SiO2+3C SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为____ 。
(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是____ (填元素符号)。
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式____ 。
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为_____ 。
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为____ 。
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为____ 。
(1)下列物质属于化合物但不属于电解质的是
| A.石墨 | B.CO2 | C.NH3·H2O | D.CaCO3 |
 SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】天然固氮的方式有生物固氮和大气固氮。大气固氮是在放电或高温下,空气中的N2转化为HNO3的过程。
(1)将下列N2转化为HNO3的过程补充完整。
N2 ①
① NO2
NO2 HNO3
HNO3
①为_______ ,②为_______ 。
A.NH3 B.NO C.N2O5 D.H2O
(2)NH4HCO3是常用的氮肥,在施用时若受热会释放出氨气而降低肥效。检验 的方法是将待检物加入到试管中,然后_______。
的方法是将待检物加入到试管中,然后_______。
(3)中国科学院科研团队研究发现,在常温常压和可见光下,基于LDH(一种固体催化剂)合成NH3的原理示意图如图。该过程实现了太阳能转化为化学能,该过程_______ (填“属于”或“不属于”)氮的固定。
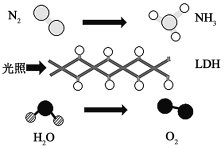
(4)上述反应中氧化剂是_______ ,被氧化的元素是_______ 。反应的化学方程式为_______ 。
(1)将下列N2转化为HNO3的过程补充完整。
N2
 ①
① NO2
NO2 HNO3
HNO3①为
A.NH3 B.NO C.N2O5 D.H2O
(2)NH4HCO3是常用的氮肥,在施用时若受热会释放出氨气而降低肥效。检验
 的方法是将待检物加入到试管中,然后_______。
的方法是将待检物加入到试管中,然后_______。| A.加热,用湿润的红色石蕊试纸放入试管口检验 |
| B.加水溶解,用红色石蕊检验其酸碱性 |
| C.加入碱溶液,加热,再滴入酚酞试液 |
| D.加入苛性钠溶液,加热,用湿润的红色石蕊试纸在试管口检验 |

(4)上述反应中氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯,硫,氯元素广泛存在于自然界中,对人类生命和生活具有重要意义。
(1)氯气的颜色:______ ; 在
在 中燃烧火焰颜色:
中燃烧火焰颜色:__________ 。
(2)浓硫酸具有:①酸性②强氧化性③吸水性④脱水性,下列现象硫酸所表现出的性质为(填编号)
干燥氯气______ ,使蔗糖变黑________ ,吸收氨气_________ ,与铜反应________ 。
(3)为了提高农作物的产量,德国化学家哈伯、波施等成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理:________ ;实验室制取氨气的化学方程式____________ 。
(4)自然界形成NO的化学方程式:_____________ 。氮氧化物( )污染环境,若用
)污染环境,若用 ,溶液吸收
,溶液吸收 可生成
可生成 ,9.2g
,9.2g 和
和 溶液完全反应时转移电子0.1mol,则反应的离子方程式为
溶液完全反应时转移电子0.1mol,则反应的离子方程式为_____________ 。
(1)氯气的颜色:
 在
在 中燃烧火焰颜色:
中燃烧火焰颜色:(2)浓硫酸具有:①酸性②强氧化性③吸水性④脱水性,下列现象硫酸所表现出的性质为(填编号)
干燥氯气
(3)为了提高农作物的产量,德国化学家哈伯、波施等成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理:
(4)自然界形成NO的化学方程式:
 )污染环境,若用
)污染环境,若用 ,溶液吸收
,溶液吸收 可生成
可生成 ,9.2g
,9.2g 和
和 溶液完全反应时转移电子0.1mol,则反应的离子方程式为
溶液完全反应时转移电子0.1mol,则反应的离子方程式为
您最近一年使用:0次



