(1)写出下图中序号①、③仪器的名称:
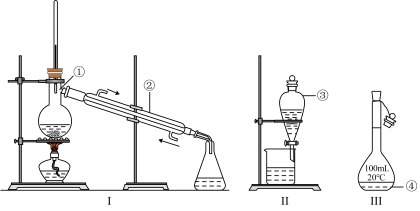
①_______ ;
③_______ ;
(2)仪器①~④中,使用时必须检查是否漏水的有_______ (填仪器序号)。
(3)如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480mL1mol·L-l的稀硫酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平⑦玻璃棒。请回答下列问题:
①配制稀硫酸时,还缺少的仪器有_______ (写仪器名称)。
②经计算,配制480 mL l mol·L-l的稀硫酸需要用量筒量取上述浓硫酸的体积为_______ mL。
③在转入容量瓶前烧杯中液体应_______ ,否则会使结果浓度_______ (填“偏高、偏低、无影响”)。
④定容时必须使溶液的凹液面与刻度线相平,若俯视会使浓度_______ 。(填“偏高、偏低、无影响”)。

①
③
(2)仪器①~④中,使用时必须检查是否漏水的有
(3)如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。现用该浓硫酸配制480mL1mol·L-l的稀硫酸。

可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平⑦玻璃棒。请回答下列问题:
①配制稀硫酸时,还缺少的仪器有
②经计算,配制480 mL l mol·L-l的稀硫酸需要用量筒量取上述浓硫酸的体积为
③在转入容量瓶前烧杯中液体应
④定容时必须使溶液的凹液面与刻度线相平,若俯视会使浓度
更新时间:2021-06-21 20:40:27
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】根据如图所示实验装置,回答下列问题。

(1)写出下列仪器的名称:①___ ,④___ 。
(2)仪器①~④中,使用时必须检查是否漏水的是___ (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是___ ,②的进水口是__ (填“f”或“g”)。
(4)配制溶液时,下列操作会导致所配溶液的浓度偏低的是__ (填标号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线

(1)写出下列仪器的名称:①
(2)仪器①~④中,使用时必须检查是否漏水的是
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器是
(4)配制溶液时,下列操作会导致所配溶液的浓度偏低的是
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室需要 溶液,现用NaOH固体配制该溶液。回答下列问题:
溶液,现用NaOH固体配制该溶液。回答下列问题:
(1)配制过程中除用到了玻璃棒、烧杯、量筒、胶头滴管外,还需要的玻璃仪器为_______ ,该仪器使用前必须进行的操作为_______ 。
(2)经计算需要用托盘天平称量NaOH固体的质量为_______ 。
(3)配制前,若容量瓶内含少量水,则所配溶液浓度_______ (填“偏大”“偏小”或“无影响”,下同),若定容过程中仰视刻度线,则所配溶液浓度_______ 。
(4)取出480mL所配溶液,溶液中所含 数目为
数目为_______ (用 表示阿伏加德罗常数的值)。若要将该溶液转化为
表示阿伏加德罗常数的值)。若要将该溶液转化为 溶液,则反应消耗
溶液,则反应消耗 的体积为
的体积为_______ L(标准状况下测得,结果保留3位有效数字)。
 溶液,现用NaOH固体配制该溶液。回答下列问题:
溶液,现用NaOH固体配制该溶液。回答下列问题:(1)配制过程中除用到了玻璃棒、烧杯、量筒、胶头滴管外,还需要的玻璃仪器为
(2)经计算需要用托盘天平称量NaOH固体的质量为
(3)配制前,若容量瓶内含少量水,则所配溶液浓度
(4)取出480mL所配溶液,溶液中所含
 数目为
数目为 表示阿伏加德罗常数的值)。若要将该溶液转化为
表示阿伏加德罗常数的值)。若要将该溶液转化为 溶液,则反应消耗
溶液,则反应消耗 的体积为
的体积为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】实验室需要配制1mol/L的氢氧化钠溶液250mL。完成下列各题。
(1)应选择规格为___ mL的容量瓶。该容量瓶上除注明规格外,还标有___ (选填编号)
a.温度b.浓度c.压强d.刻度线
(2)用电子天平秤取___ gNaOH。
(3)将称好的氢氧化钠固体加适量蒸馏水将其溶解,待___ 后将溶液移入容量瓶中。
(4)用少量蒸馏水冲洗____ 2~3次,将洗液移入容量瓶中。
(5)向容量瓶内加水至接近刻度1~2cm处,改用_____ 小心地加入至溶液凹液面与刻度线相切。
(6)最后塞好瓶塞,摇匀,将配好的溶液移入___ 中并贴好标签。
(7)分析下列操作可能会对氢氧化钠溶液浓度造成的影响(填“偏高”、“偏低”或“无影响”)
①转移时容量瓶中有残留的蒸馏水___ ②定容时俯视___
(1)应选择规格为
a.温度b.浓度c.压强d.刻度线
(2)用电子天平秤取
(3)将称好的氢氧化钠固体加适量蒸馏水将其溶解,待
(4)用少量蒸馏水冲洗
(5)向容量瓶内加水至接近刻度1~2cm处,改用
(6)最后塞好瓶塞,摇匀,将配好的溶液移入
(7)分析下列操作可能会对氢氧化钠溶液浓度造成的影响(填“偏高”、“偏低”或“无影响”)
①转移时容量瓶中有残留的蒸馏水
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】用18.4 mol/L的浓H2SO4来配制500 mL 0.2 mol/L的稀H2SO4.可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平 ⑦药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时不需要使用的有___________ (填代号),还缺少的仪器是___________ 。
(2)经计算,需浓H2SO4的体积为___________ ,量取浓硫酸时应选用___________ (填序号)(选填①10 mL、②50 mL、③100 mL三种规格)的量筒。
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。可能引起这种结果的操作是___________ 。
①定容时俯视刻度线;
②未冷却到室温就定容;
③用量筒量取浓硫酸时仰视读数;
④洗涤量取浓硫酸的量筒并将洗涤液转移到容量瓶;
⑤摇匀后,发现液面在刻线以下,未采取其它任何补救操作;
⑥洗涤完烧杯的洗液直接倒掉,未转移到容量瓶里;
⑦把烧杯中的溶液转移到容量瓶前,容量瓶中含有少量的水;
⑧定容时水加多了,用滴管吸出少量水至刻度线。
(1)上述仪器中,在配制稀H2SO4时不需要使用的有
(2)经计算,需浓H2SO4的体积为
(3)将所配制的稀H2SO4进行测定,发现浓度大于0.2 mol/L。可能引起这种结果的操作是
①定容时俯视刻度线;
②未冷却到室温就定容;
③用量筒量取浓硫酸时仰视读数;
④洗涤量取浓硫酸的量筒并将洗涤液转移到容量瓶;
⑤摇匀后,发现液面在刻线以下,未采取其它任何补救操作;
⑥洗涤完烧杯的洗液直接倒掉,未转移到容量瓶里;
⑦把烧杯中的溶液转移到容量瓶前,容量瓶中含有少量的水;
⑧定容时水加多了,用滴管吸出少量水至刻度线。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某同学用MnO2与浓盐酸反应制备氯气,并探究氯气的性质。

试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是______ (填字母),盛放MnO2的仪器名称是______ ,写出反应的化学方程式_______ 。
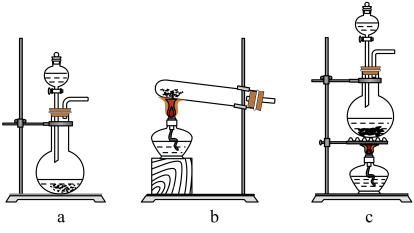
(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色了。其原因可能是______ ,合理的改进方法是______ 。
(3)家庭中常用消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)清洁卫生。但若两者混合使用会产生有毒的气体,写出反应的离子方程式:______ 。
(4)用氢氧化钠固体配制480mL1mol/LNaOH溶液用于尾气的吸收。配制时用到的玻璃仪器除了烧杯、量筒、玻璃棒、胶头滴管外,还需要_______ 。若所用的氢氧化钠固体受潮,则会导致配得的溶液浓度_____ (填“偏大”或“偏小”)。

试回答下列问题:
(1)在该实验中,以下可用于制取氯气的装置是

(2)装置B、C中依次放入的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色了。其原因可能是
(3)家庭中常用消毒液(主要成分是NaClO)与洁厕灵(主要成分是盐酸)清洁卫生。但若两者混合使用会产生有毒的气体,写出反应的离子方程式:
(4)用氢氧化钠固体配制480mL1mol/LNaOH溶液用于尾气的吸收。配制时用到的玻璃仪器除了烧杯、量筒、玻璃棒、胶头滴管外,还需要
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.实验室要配制500 mL 0.2 mol/L NaOH溶液,请回答下列问题:
(1)下列玻璃仪器中,不需使用的是________________________ (填名称)。
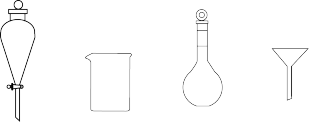
(2)用托盘天平称取氢氧化钠固体,其质量为___________ g。
(3)下列主要操作步骤的正确顺序是①________________ ④(填余下步骤的序号)。
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度_______ (填“偏高、偏低”或“不变”)。
Ⅱ.如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
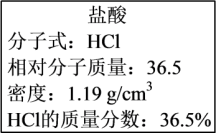
(5)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(6)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(1)下列玻璃仪器中,不需使用的是

(2)用托盘天平称取氢氧化钠固体,其质量为
(3)下列主要操作步骤的正确顺序是①
①称取一定质量的氢氧化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶瓶颈刻度线下1~2 cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③待冷却至室温后,将溶液转移到500 mL容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会使配制出的NaOH溶液浓度
Ⅱ.如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
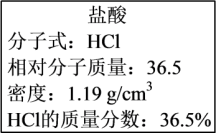
(5)该浓盐酸中HCl的物质的量浓度为
(6)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验室用63%的浓HNO3(其密度为1.4g/mL)配制240mL0.50mol/L稀HNO3,此浓硝酸的物质的量浓度为___ ,配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号)___ 。
①量取浓硝酸的量筒用蒸馏水洗涤2〜3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(2)现有下列仪器:
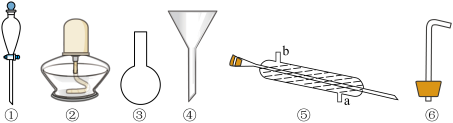
①海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,按照实验仪器从下到上、从左到右的顺序,依次是____ (填序号);仪器⑤的冷凝水应从___ 口进入(填“a”或“b”)。
②海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的___ (填序号),该仪器名称为___ ,向该碘水中加入四氯化碳以提取碘单质的实验操作叫做___ 。
①量取浓硝酸的量筒用蒸馏水洗涤2〜3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线。
(2)现有下列仪器:

①海水蒸馏是由海水获得淡水的常用方法之一,在实验室里组成一套蒸馏装置肯定需要上述仪器中的一部分,按照实验仪器从下到上、从左到右的顺序,依次是
②海带等藻类物质经过处理后,可以得到碘水,欲从碘水中提取碘,需要上述仪器中的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室需要配制480 mL 0.5 mol/L的氢氧化钠溶液,有如下操作步骤:
(1)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、______ 、_____ 。需要称量NaOH固体的质量为_______ g。
(2)若出现如下情况,对所配溶液浓度将有何影响? (填“偏高”“偏低”或“无影响" )
A.容量瓶中原有少量蒸馏水_______ 。
B.转移溶液时,没有洗涤玻璃棒和溶解用的烧杯_______ 。
C.定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线_______ 。
D.定容时,俯视观察液面_______ 。
(1)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、
(2)若出现如下情况,对所配溶液浓度将有何影响? (填“偏高”“偏低”或“无影响" )
A.容量瓶中原有少量蒸馏水
B.转移溶液时,没有洗涤玻璃棒和溶解用的烧杯
C.定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线
D.定容时,俯视观察液面
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】邻苯二甲酸氢钾常用作pH测定的缓冲剂,现需要用0.1mol/L邻苯二甲酸氢钾溶液和0.1mol/L盐酸配成pH=3.3的缓冲液。回答下列问题:
(1)用邻苯二甲酸氢钾固体配制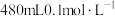 邻苯二甲酸氢钾溶液,除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有
邻苯二甲酸氢钾溶液,除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有___________ 。
(2)在配制邻苯二甲酸氢钾溶液时,下列说法正确的是___________ 。
a.溶解邻苯二甲酸氢钾后直接转移到容量瓶中
b.容量瓶用蒸馏水洗净烘干后才能用于溶液配制
c.定容时仰视会导致浓度偏低
(3)用密度 、质量分数为
、质量分数为 的盐酸配制
的盐酸配制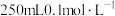 的稀盐酸,需要用量筒量取
的稀盐酸,需要用量筒量取___________  浓盐酸。
浓盐酸。
(4)若量取浓盐酸的量筒未干燥,则所配盐酸的浓度___________ (填“偏高”“偏低”或“无影响”,下同);若用量筒量取浓盐酸时俯视,所配盐酸的浓度___________ 。
(1)用邻苯二甲酸氢钾固体配制
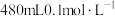 邻苯二甲酸氢钾溶液,除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有
邻苯二甲酸氢钾溶液,除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有(2)在配制邻苯二甲酸氢钾溶液时,下列说法正确的是
a.溶解邻苯二甲酸氢钾后直接转移到容量瓶中
b.容量瓶用蒸馏水洗净烘干后才能用于溶液配制
c.定容时仰视会导致浓度偏低
(3)用密度
 、质量分数为
、质量分数为 的盐酸配制
的盐酸配制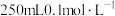 的稀盐酸,需要用量筒量取
的稀盐酸,需要用量筒量取 浓盐酸。
浓盐酸。(4)若量取浓盐酸的量筒未干燥,则所配盐酸的浓度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】欲用36.5%(密度为1.18g/cm3)的浓盐酸配制浓度为1.00mol/L的稀盐酸500mL。
 (1)选用的主要玻璃仪器有:①
(1)选用的主要玻璃仪器有:①____ ②____ ③___ ④___ ⑤___ 。
(2)现有下列配制操作,正确的操作顺序为:_________ (填字母)
A.用量筒量取浓盐酸;B.反复颠倒摇匀;C.用胶头滴管加水至刻度线;D.洗净所用仪器,洗涤液也转入容量瓶;E.稀释浓盐酸;F.溶液冷却后转入容量瓶
(3)简要回答下列问题:
如果实验室有10mL、50mL、100mL的量筒,应选用______ mL的量筒。量取时发现量筒不干净,用水洗净后直接量取,将使配制的溶液浓度______ (填“偏高”、“偏低”或“无影响”)。

 (1)选用的主要玻璃仪器有:①
(1)选用的主要玻璃仪器有:①
(2)现有下列配制操作,正确的操作顺序为:

A.用量筒量取浓盐酸;B.反复颠倒摇匀;C.用胶头滴管加水至刻度线;D.洗净所用仪器,洗涤液也转入容量瓶;E.稀释浓盐酸;F.溶液冷却后转入容量瓶
(3)简要回答下列问题:
如果实验室有10mL、50mL、100mL的量筒,应选用
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】某实验小组用0.50 mol∙L−1的NaOH溶液和0.50 mol∙L−1的硫酸溶液进行中和热测定实验。
Ⅰ.配制0.50 mol∙L−1NaOH溶液
(1)若实验中大约要使用230mLNaOH溶液,需要称量NaOH固体_______ g。
(2)用NaOH固体配制NaOH溶液用到的带刻度的玻璃仪器有烧杯、_______ 。
Ⅱ.测定中和热实验,其装置如图所示。

(3)从实验装置上看,图中尚缺少一种玻璃仪器是_______ 。
(4)写出该反应的热化学方程式(中和热的数值为57.3):_______ 。
(5)取50mLNaOH溶液和30mL硫酸溶液进行实验,测得的实验数据如表。
①请填写下表中的空白:
②0.50 mol∙L−1NaOH溶液和0.50 mol∙L−1硫酸溶液的密度均近似为1 ,中和后生成的溶液比热容
,中和后生成的溶液比热容 。则测得中和热
。则测得中和热
_______  (取小数点后一位)。
(取小数点后一位)。
③上述实验数值结果与57.3 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
Ⅰ.配制0.50 mol∙L−1NaOH溶液
(1)若实验中大约要使用230mLNaOH溶液,需要称量NaOH固体
(2)用NaOH固体配制NaOH溶液用到的带刻度的玻璃仪器有烧杯、
Ⅱ.测定中和热实验,其装置如图所示。

(3)从实验装置上看,图中尚缺少一种玻璃仪器是
(4)写出该反应的热化学方程式(中和热的数值为57.3):
(5)取50mLNaOH溶液和30mL硫酸溶液进行实验,测得的实验数据如表。
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值 (t2−t1)/℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 ,中和后生成的溶液比热容
,中和后生成的溶液比热容 。则测得中和热
。则测得中和热
 (取小数点后一位)。
(取小数点后一位)。③上述实验数值结果与57.3
 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次



