有A、B、C、D四种金属,用稀硫酸作电解质溶液,当A、B组成原电池时,电子流动方向A→B;当A、D组成原电池时,A为正极;B与C构成原电池时,C极发生还原反应,B极发生氧化反应。则A、B、C、D金属性由强到弱的顺序为
| A.A>B>C>D | B.A>B>D>C |
| C.D>C>A>B | D.D>A>B>C |
更新时间:2021-06-22 13:05:27
|
【知识点】 利用原电池原理比较金属活动性强弱解读
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C三种金属,分别进行如下实验:
①A、B用导线相连后,同时浸入稀硫酸中,B极为负极;
②B、C用导线相连后,同时浸入稀硫酸中,B极产生大量气泡;
据此判断三种金属的活泼性顺序为
①A、B用导线相连后,同时浸入稀硫酸中,B极为负极;
②B、C用导线相连后,同时浸入稀硫酸中,B极产生大量气泡;
据此判断三种金属的活泼性顺序为
| A.A>B>C | B.C>B>A | C.A>C>B | D.B>C>A |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】有a、b、c、d四种金属,将a与b用导线连接起来,浸入稀硫酸中,导线中电子从a流向b;将a、d分别投入等浓度的盐酸中,d比a反应剧烈;又知一定条件下能发生如下离子反应: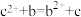 ,则四种金属的活动性出强到弱的顺序是
,则四种金属的活动性出强到弱的顺序是
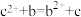 ,则四种金属的活动性出强到弱的顺序是
,则四种金属的活动性出强到弱的顺序是| A.dcab | B.dabc | C.dbac | D.badc |
您最近一年使用:0次



