肼(H2N—NH2)是一种高能燃料,共价键的键能与热化学方程式信息如表:
则关于反应N2H4(g)+O2(g)=N2(g)+2H2O(g)说法正确的是
| 共价键 | N—H | N—N | O=O | N≡N | O—H |
| 键能/(kJ•mol-1) | 391 | 161 | 498 | 946 | 463 |
| A.该反应是吸热反应 | B.N2H4(l)比N2H4(g)能量高 |
| C.反应物总键能小于生成物总键能 | D.H2O空间结构是直线型 |
20-21高一下·浙江绍兴·期末 查看更多[8]
浙江省绍兴市诸暨市2020-2021学年高一下学期期末考试化学试题(已下线)2022年1月浙江省普通高中学业水平考试化学仿真模拟试卷A(已下线)2022年浙江省6月高考真题变式题11-20四川省成都市新都区2021-2022学年高一下学期期末测试化学试题(已下线)专题15 反应热计算的几种类型-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题14 化学反应与热量计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)浙江省金华市东阳中学2022-2023学年高二下学期7月月考化学试题浙江省湖州市吴兴高级中学2023-2024学年高二上学期10月阶段性测试化学试题
更新时间:2021-06-28 08:15:37
|
相似题推荐
【推荐1】某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程如图所示(图中只画出了HAP的部分结构,用18O标记羟基磷灰石中的羟基氧原子)。下列说法正确的是
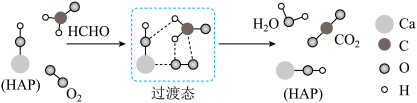

| A.反应物的键能之和大于生成物的键能之和 |
| B.经过该催化氧化过程后18O仍然在HAP中 |
| C.HAP改变了该反应的历程和焓变,加快了反应速率 |
| D.HAP降低了反应的活化能,提高活化分子百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】科学家提出一种大气中 在
在 和
和 作用下转变为
作用下转变为 的机理(图1),其能量变化如图2所示。
的机理(图1),其能量变化如图2所示。不正确 的是
 在
在 和
和 作用下转变为
作用下转变为 的机理(图1),其能量变化如图2所示。
的机理(图1),其能量变化如图2所示。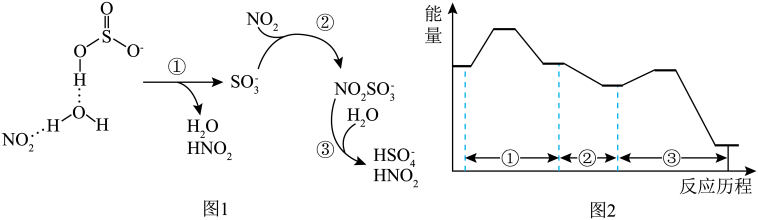
已知: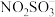 的结构式为
的结构式为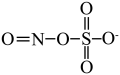
A.①中涉及 键的断裂与生成 键的断裂与生成 | B.②③均发生了氧化还原反应 |
| C.由图2可知,该过程的决速步是① | D.总反应中还原剂与氧化剂的物质的量之比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知H―H的键能为 I―I的键能为
I―I的键能为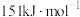 反应
反应 经历了如下反应历程:①
经历了如下反应历程:①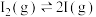 ,②
,② ,反应过程的能量变化如图所示。下列说法正确的是
,反应过程的能量变化如图所示。下列说法正确的是
 I―I的键能为
I―I的键能为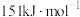 反应
反应 经历了如下反应历程:①
经历了如下反应历程:①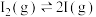 ,②
,② ,反应过程的能量变化如图所示。下列说法正确的是
,反应过程的能量变化如图所示。下列说法正确的是
A.H―I的键能为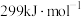 |
| B.升高温度,反应①速率增大,反应②速率减小 |
C.升高温度,反应②的限度和速率均增大,有利于提高 的转化率 的转化率 |
D.为防止反应过程中有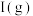 大量累积,应选择合适的催化剂降低反应②的焓变 大量累积,应选择合适的催化剂降低反应②的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
| B.由C(s,石墨)═C(s,金刚石)△H=+1.9kJ•mol-1可知金刚石比石墨稳定 |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
D.已知Ⅰ.反应H2(g)+Cl2(g)=2HCl(g)△H=-akJ·mol-1;Ⅱ. 。且a、b、c均大于零,则断开1mol H-Cl键所需的能量为 。且a、b、c均大于零,则断开1mol H-Cl键所需的能量为 kJ kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】研究表明,化学反应的能量变化与反应物和生成物的键能有关,键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的 键能数据:已知白磷燃烧的化学方程式为P4(s)+5O2(g)=P4O10(s)该反应放出热量2 378 kJ,且白磷分子为正四面体,4个磷原子分别位于正四面体的四个顶点,白磷及其完全燃烧的产物结构如图所示,则下表中x为

| 化学键 | P—P | P—O | O=O | P=O |
| 键能(kJ·mol-1) | 197 | x | 499 | 434 |

| A.410 | B.335 | C.360 | D.188 |
您最近一年使用:0次




