已知H―H的键能为 I―I的键能为
I―I的键能为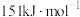 反应
反应 经历了如下反应历程:①
经历了如下反应历程:①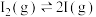 ,②
,② ,反应过程的能量变化如图所示。下列说法正确的是
,反应过程的能量变化如图所示。下列说法正确的是
 I―I的键能为
I―I的键能为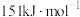 反应
反应 经历了如下反应历程:①
经历了如下反应历程:①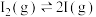 ,②
,② ,反应过程的能量变化如图所示。下列说法正确的是
,反应过程的能量变化如图所示。下列说法正确的是
A.H―I的键能为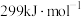 |
| B.升高温度,反应①速率增大,反应②速率减小 |
C.升高温度,反应②的限度和速率均增大,有利于提高 的转化率 的转化率 |
D.为防止反应过程中有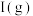 大量累积,应选择合适的催化剂降低反应②的焓变 大量累积,应选择合适的催化剂降低反应②的焓变 |
更新时间:2024-03-02 18:00:55
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在反应CH4(g)=C(s)+2H2(g) △H中,1molC(s)成键释放的热量为709.6kJ,C-H的键能为414kJ•mol-1,则H-H的键能为
已知:反应①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ•mol-1;
反应②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205.9kJ•mol-1。
已知:反应①C(s)+H2O(g)=CO(g)+H2(g) △H1=+131.5kJ•mol-1;
反应②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2=+205.9kJ•mol-1。
| A.872kJ | B.436kJ | C.872kJ•mol-1 | D.436kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关反应热的说法不正确的是
A.在稀溶液中: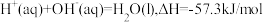 ,若将含0.5 mol H2SO4的稀硫酸与含 ,若将含0.5 mol H2SO4的稀硫酸与含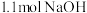 的稀溶液混合,放出的热量等于57.3 kJ 的稀溶液混合,放出的热量等于57.3 kJ |
B.甲烷的燃烧热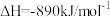 ,则甲烷燃烧的热化学方程式为: ,则甲烷燃烧的热化学方程式为: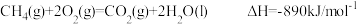 |
C. 键、 键、 键和 键和 键的键能分别为 键的键能分别为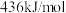 , ,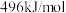 和 和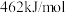 ,则反应 ,则反应 的 的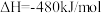 |
D. ,石墨比金刚石稳定 ,石墨比金刚石稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】臭氧分解过程如图所示,下列说法正确的是
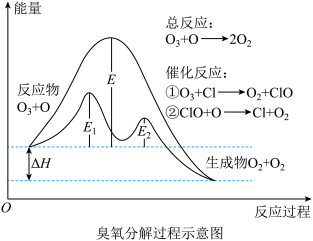

| A.催化反应①②均为放热反应 |
B.决定 分解反应速率的是催化反应② 分解反应速率的是催化反应② |
C. 是催化反应①对应的正反应的活化能, 是催化反应①对应的正反应的活化能,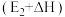 是催化反应②对应的逆反应的活化能 是催化反应②对应的逆反应的活化能 |
| D.温度升高,总反应的正反应速率增加,逆反应速率减小。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在浓硫酸作用下,苯与浓硝酸发生反应的反应历程如图。下列说法错误的是
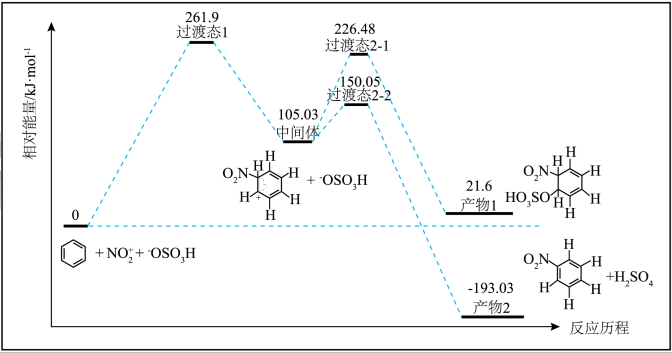
| A.生成中间体时碳的杂化方式未发生改变 |
| B.生成中间体的反应为决速步骤 |
| C.产物1为加成反应的产物 |
| D.动力学和热力学优势产物均为产物2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在锌与某浓度的盐酸反应的实验中,得到如下结果:
下列说法中,正确的是
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| 实验序号 | 锌的质量/g | 锌的形状 | 温度/℃ | 锌完全溶解于酸的时间/s |
1 | 2 | 薄片 | 15 | 150 |
2 | 2 | 薄片 | 35 | t1 |
3 | 2 | 粉末 | 35 | t2 |
①t1<t2 ②t1>150 ③实验1和实验2比较,单位时间内消耗的锌的质量前者小于后者
| A.只有① | B.①② | C.只有③ | D.②③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知:3Z(s) X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法
X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法不正确 的是( )
 X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法
X(g)+2Y(g) ΔH=akJ·molˉ1(a>0)。下列说法| A.增大压强,平衡逆向移动,化学平衡常数不变 |
| B.达到化学平衡状态时,气体平均摩尔质量不变 |
| C.投入3mol Z,达到化学平衡状态时,反应放出的总热量可达akJ |
| D.升高反应温度,逆反应速率增大,正反应速率也增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验操作(或实验操作和现象)能得到的结论正确的是
选项 | 实验操作(或实验操作和现象) | 结论 |
A | 向两支盛有5mL不同浓度的 | 反应物浓度越大,反应速率越大 |
B |
|
|
C |
| 验证AgC1的溶解度大于 |
D |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】CO(g)+Cl2(g) COCl2(g) △H<0,当反应达到平衡时,下列措施:①加压、②升温、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体,能提高CO转化率的是
COCl2(g) △H<0,当反应达到平衡时,下列措施:①加压、②升温、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体,能提高CO转化率的是
 COCl2(g) △H<0,当反应达到平衡时,下列措施:①加压、②升温、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体,能提高CO转化率的是
COCl2(g) △H<0,当反应达到平衡时,下列措施:①加压、②升温、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体,能提高CO转化率的是| A.②③ | B.③⑤ | C.①③ | D.③⑥ |
您最近一年使用:0次

 )
)
 )
)
 )
)
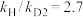
 和
和 都是有害物质,有人提出通过以下反应来处理尾气:
都是有害物质,有人提出通过以下反应来处理尾气: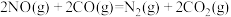 。对上述反应,下列说法正确的是
。对上述反应,下列说法正确的是 溶液的试管中同时加入
溶液的试管中同时加入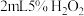 溶液,观察实验现象
溶液,观察实验现象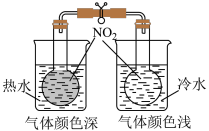
 为放热反应
为放热反应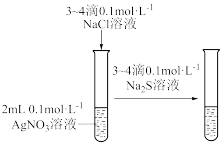


 的水解程度比
的水解程度比 强
强