下列离子方程式书写正确的是
A.铜与浓硫酸加热条件下反应:Cu+SO +4H+ +4H+ SO2↑+Cu2++2H2O SO2↑+Cu2++2H2O |
B.NaClO溶液中通入足量SO2:SO2+ClO-+H2O=SO +Cl-+2H+ +Cl-+2H+ |
C.碳酸氢钠溶液和过量澄清石灰水混合:2HCO +Ca2++2OH-=CaCO3+CO +Ca2++2OH-=CaCO3+CO +H2O +H2O |
D.NH4HSO4溶液中滴入少量Ba(OH)2溶液:NH +H++SO +H++SO +Ba2++2OH-=NH3•H2O+BaSO4↓+H2O +Ba2++2OH-=NH3•H2O+BaSO4↓+H2O |
更新时间:2021/06/28 16:23:57
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列反应的离子方程式中正确的是
A.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH-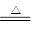 NH3↑+H2O NH3↑+H2O |
| B.Ca(HCO3)2溶液中滴加少量NaOH溶液 Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.向Fe(OH)2中加入稀硝酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列各溶液中加入试剂后,发生反应的离子方程式书写正确的是
A.向Mg(HCO3)2溶液中滴加足量NaOH溶液:Mg2++ +OH-=MgCO3↓+H2O +OH-=MgCO3↓+H2O |
B.水杨酸与过量碳酸钠溶液反应: + + → →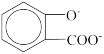 +CO2↑+H2O +CO2↑+H2O |
| C.Na2O2与H218O反应:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
D.Na2S2O3溶液中通入足量氯气: +4Cl2+5H2O=2 +4Cl2+5H2O=2 +8Cl-+10H+ +8Cl-+10H+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列离子方程式的书写及评价均合理的是( )
| 选项 | 离子方程式 | 评价 |
| A | 将2 molCl2通入到含1 mol FeI2的溶液中:2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | 正确;Cl2过量,Fe2+、I-均被氧化 |
| B | 将Na2O2固体溶于水:2Na2O2+2H2O=4Na++4OH-+O2↑ | 正确;Na2O2是碱性氧化物 |
| C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO-=HClO+HSO3- | 正确;H2SO3的酸性强于HClO |
| D | Mg(HCO3)2溶液与足量的NaOH溶液反应:Mg2++2HCO3-+4OH-=Mg(OH)2 ↓+2CO32-+2H2O | 正确;Mg(OH)2比MgCO3更难溶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列对应离子方程式正确的是
| A | 向饱和 溶液中通入过量 溶液中通入过量 | 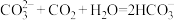 |
| B |  溶液中加入过量的 溶液中加入过量的 溶液 溶液 | 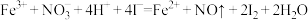 |
| C |  溶液与过量石灰水反应 溶液与过量石灰水反应 |  |
| D |  溶液中通入少量 溶液中通入少量 气体 气体 | 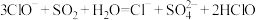 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列探究卤族元素单质及其化合物性质的实验方案能达到目的的是
| 选项 | 探究目的 | 实验方案 |
| A | 溴乙烷发生消去反应 | 将溴乙烷和NaOH的乙醇溶液混合后加热,产生的气体经水洗后,再通入酸性 溶液中,观察酸性 溶液中,观察酸性 溶液的颜色变化 溶液的颜色变化 |
| B | Ksp(AgI)<Ksp(AgCl) | 向 溶液中先滴加4滴 溶液中先滴加4滴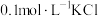 溶液,再滴加4滴 溶液,再滴加4滴 溶液,观察生成沉淀的颜色 溶液,观察生成沉淀的颜色 |
| C | 氯气与水的反应存在限度 | 取两份新制氯水,分别滴加 溶液和淀粉KI溶液,观察生成物的颜色 溶液和淀粉KI溶液,观察生成物的颜色 |
| D | NaClO溶液的酸碱性 | 用玻璃棒蘸取NaClO溶液点滴在pH试纸上,再与标准比色卡对照 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题-单题
|
较难
(0.4)
【推荐2】依据下列实验方案设计和现象所得结论正确的是
| 选项 | 方案设计 | 现象 | 结论 |
| A | 用红色激光笔照射某液体 | 有一条光亮的“通路” | 该液体一定是 胶体 胶体 |
| B | 向盛有 和 和 的试管中分别滴加浓盐酸 的试管中分别滴加浓盐酸 | 盛有 的试管中产生黄绿色气体 的试管中产生黄绿色气体 | 氧化性: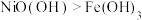 |
| C | 向某溶液中滴加几滴 稀溶液,用湿润的红色石蕊试纸靠近试管口 稀溶液,用湿润的红色石蕊试纸靠近试管口 | 红色石蕊试纸 无明显现象 | 该溶液中一定无 |
| D | 将氯气通入紫色石蕊试液中 | 紫色石蕊试液 先变红后褪色 | 氯气既有酸性又有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】已知某些酸的电离常数数据如下,下列离子方程式正确的是
| H2SO3 | K1=1.5×10-2;K2=1.1×10-7 |
| H2CO3 | K1=4.3×10-7;K2=5.6×10-11 |
| HClO | K=3.0×10-8 |
A.NaClO溶液中通少量SO2:2ClO-+SO2+H2O=2HClO+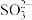 |
B.Na2CO3溶液中通足量SO2: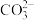 +2SO2+H2O=CO2↑+2 +2SO2+H2O=CO2↑+2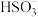 |
C.NaClO溶液中通少量CO2:2ClO-+CO2+H2O=2HClO+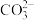 |
D.Na2CO3溶液中加少量氯水: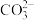 +H+= +H+=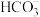 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列实验操作及现象与结论一致的是
| 选项 | 实验操作及现象 | 结论 |
| A | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 氧化性:稀硝酸大于浓硝酸 |
| B | 将浓硫酸滴入蔗糖中并搅拌,得到黑色蓬松的固体并产生有刺激性气味的气体 | 该过程中浓硫酸仅体现了脱水性 |
| C | 向滴有酚酞的氨水中滴加氯水,溶液的红色褪去 | 氯水具有漂白性 |
| D | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入少量稀硝酸,再滴加几滴KSCN溶液,溶液变为红色 | 菠菜中含有铁元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列对实验装置图、实验操作及结论描述正确的是
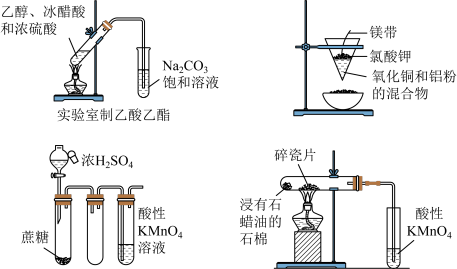

| A.制取乙酸乙酯 |
| B.制取金属铜 |
| C.滴入浓硫酸后一段时间,高锰酸钾溶液褪色,说明蔗糖发生了水解反应 |
| D.加热片刻后高锰酸钾溶液褪色,说明石蜡油分解产生了乙烯 |
您最近一年使用:0次

 溶液中滴入
溶液中滴入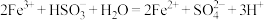
 溶液中通入
溶液中通入 ,溶液变为黄绿色:
,溶液变为黄绿色: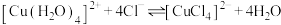
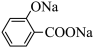 溶液中加入少量盐酸:
溶液中加入少量盐酸: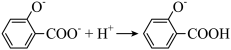

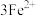 +NO
+NO =NO↑+
=NO↑+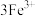 +2H2O
+2H2O +
+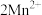 +2H2O
+2H2O +HCO
+HCO =MgCO3↓+H2O
=MgCO3↓+H2O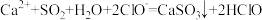
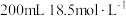 浓硫酸充分反应后,固体完全溶解,同时生成气体
浓硫酸充分反应后,固体完全溶解,同时生成气体 (生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到
(生成气体全部逸出,测定条件为标准状况)。将反应后的溶液稀释到 ,测得稀释后溶液中的
,测得稀释后溶液中的 浓度为
浓度为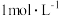 。向反应后的溶液中加入
。向反应后的溶液中加入 时,所得沉淀质量最大,其质量为
时,所得沉淀质量最大,其质量为 。下列叙述中不正确的是
。下列叙述中不正确的是