A、B、C、D、E为原子序数依次增大的短周期元素,A是周期表中原子半径最小的元素,B是形成有机物的必备元素,C的最外层电子数是次外层的3倍,D与水能剧烈反应产生一种化合物X和 ,E的最高价氧化物的水化物是二元强酸。
,E的最高价氧化物的水化物是二元强酸。
(1)B在元素周期表中的位置_______
(2)B、E两元素形成的各原子均达 稳定结构的化合物的结构式为
稳定结构的化合物的结构式为_______
(3)A和C两元素形成的一种化合物Y具有强氧化性,用电子式表示Y的形成过程_______
(4)元素的非金属性:E_______ C(填强于”或“弱于”),其实验依据是_______ (用化学方程式表示)
(5)元素的金属性:Al_______ D(填“>”或“<”),其理由是_______ (从结构观点说明)
(6)A、B、C三种元素可形成多种化合物,其中Z、W是生活中常见的有机物,Z是食醋的成分,Z可由酸性高锰酸钾氧化W制得。Z、W在加热和浓硫酸条件下发生反应的化学方程式为_______
 ,E的最高价氧化物的水化物是二元强酸。
,E的最高价氧化物的水化物是二元强酸。(1)B在元素周期表中的位置
(2)B、E两元素形成的各原子均达
 稳定结构的化合物的结构式为
稳定结构的化合物的结构式为(3)A和C两元素形成的一种化合物Y具有强氧化性,用电子式表示Y的形成过程
(4)元素的非金属性:E
(5)元素的金属性:Al
(6)A、B、C三种元素可形成多种化合物,其中Z、W是生活中常见的有机物,Z是食醋的成分,Z可由酸性高锰酸钾氧化W制得。Z、W在加热和浓硫酸条件下发生反应的化学方程式为
更新时间:2021-07-02 08:43:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】如表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
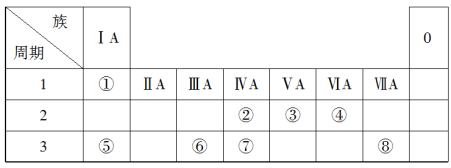
(1)地壳中含量居于第二位的元素在周期表中的位置是___ 。除稀有气体外,原子半径最大的元素是__ ,它的原子结构示意图是___ 。
(2)②的最高价氧化物的分子式为___ ;电子式为___ 。
⑦的最高价氧化物对应水化物的分子式为___ 。表中最高价氧化物对应的水化物中酸性最强的是___ (填化学式)。
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的化学式:____ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___ 。
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为___ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
⑦的最高价氧化物对应水化物的分子式为
(3)①④⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的化学式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是
A.最高正化合价为+6
B.气态氢化物比H2S稳定
C.最高价氧化物对应水化物的酸性比硫酸弱
D.单质在常温下可与氢气化合
(5)已知X为第ⅡA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第ⅢA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表列出了部分前20号元素的一些性质:
下列问题用元素符号及化学式回答:
(1)②在周期表中的位置是___________ 。
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为___________ 。由①⑨组成的分子中,共含有18e-的化合物结构式为___________ 。
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为___________ 。
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为___________ 。
元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径(10-10m) | 0.37 | 2.27 | 0.74 | 1.52 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 0.71 |
| 最高价态 | +1 | +1 | - | +1 | +4 | +5 | +7 | +1 | - | |
| 最低价态 | -1 | - | -2 | - | -4 | -3 | -1 | - | -1 |
(1)②在周期表中的位置是
(2)①与③以原子个数比1:1形成的化合物中含有
A.离子键 B.非极性键 C.极性键
(3)①②③组成的化合物电子式为
(4)⑥、⑦、⑩元素非金属性由强至弱顺序为
(5)某元素X,原子半径为1.02×10-l0m,X的一种氧化物与⑦单质的水溶液反应生成两种强酸的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为五种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素在周期表中的位置是_______ 。
(2)请写出X与Z元素按1:1组成的常见物质的电子式_______ ,
(3)由X、Y两种元素组成的8电子微粒的结构简式为_______ 。
(4)Z、Q两种元素分别形成的简单离子中半径较大的是_______ ,原因是_______ 。
(5)Z、R两种元素分别形成的简单氢化物的稳定性由大到小顺序是_______ 。
(6)废印刷电路板上含有铜,用X2Z2和稀硫酸浸泡废印刷电路板既能溶解铜,又对环境无污染,试写出反应的离子方程式_______ 。
| 元素 | 元素的相关信息 |
| X | 周期表中原子半径最小的元素 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素在周期表中的位置是
(2)请写出X与Z元素按1:1组成的常见物质的电子式
(3)由X、Y两种元素组成的8电子微粒的结构简式为
(4)Z、Q两种元素分别形成的简单离子中半径较大的是
(5)Z、R两种元素分别形成的简单氢化物的稳定性由大到小顺序是
(6)废印刷电路板上含有铜,用X2Z2和稀硫酸浸泡废印刷电路板既能溶解铜,又对环境无污染,试写出反应的离子方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】石油通过裂化和裂解可以得到乙烯,乙烯的产量可以用来衡量一个国家石油化工发展水平。图是由乙烯为原料生产某些化工产品的转化关系图。

据此回答下列问题。
(1)写出乙烯的一种用途__________ ,指出乙烯→B的反应类型 __________________ 。
(2)写出A的结构简式_________ 。
(3)写出X和新制的氢氧化铜悬浊液反应的化学方程式____________ 。
(4)写出B+C→D的化学反应方程式____________ 。

据此回答下列问题。
(1)写出乙烯的一种用途
(2)写出A的结构简式
(3)写出X和新制的氢氧化铜悬浊液反应的化学方程式
(4)写出B+C→D的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知:A是石油裂解气的主要成分,其产量通常用来衡量一个国家的石油化工水平,E物质有浓郁香味,H是高分子化合物。现以A为主要原料有如图所示的转化关系:
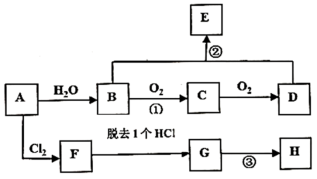
(1)B的官能团名称是___ ,D的官能团结构简式是___ 。
(2)反应①的化学方程式为___ ;反应类型___ 。
(3)反应③的化学方程式为___ ;反应类型__ 。
(4)如图为实验室制取E的装置图:
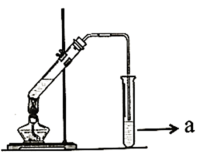
①试剂a作用为___ 。
②导管的作用为___ 。
③分离出E物质的方法是___ 。

(1)B的官能团名称是
(2)反应①的化学方程式为
(3)反应③的化学方程式为
(4)如图为实验室制取E的装置图:

①试剂a作用为
②导管的作用为
③分离出E物质的方法是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】已知: A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;由A通过聚合反应生成高分子化合物F,F可用于工业合成塑料,现以A为主要原料合成G, 以A为原料的合成路线如下图所示。
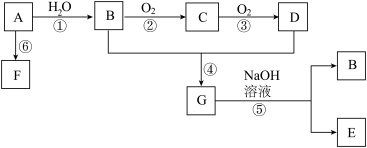
回答下列问题:
①D、G分子中的官能团名称分别__________ 、___________ 。
②在反应①~⑥中,属于加成反应的是________ ,属于取代反应的是________ 。(填序号)
③写出与G分子式相同的所有羧酸类的同分异构体:___________________________________________________________ 。

回答下列问题:
①D、G分子中的官能团名称分别
②在反应①~⑥中,属于加成反应的是
③写出与G分子式相同的所有羧酸类的同分异构体:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】与碳氢化合物类似,N、H两元素也可以形成氮烷、氮烯。联氨(又称肼,N2H4,无色液体)是一种氮烷,可用作火箭燃料。回答下列问题:
(1)氮和氢形成的无环氮烷,若分子中含n个氮原子,其分子式为___________
(2)火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
I.N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=akJ·mol-1
Ⅱ.H2O(g)=H2O(l) ΔH2=bkJ·mol-1
Ⅲ.2H2O2(l)=2H2O(l)+O2(g) ΔH3=ckJ·mol-1
则N2H4(l)与H2O2(l)反应生成N2(g)和H2O(g)的热化学方程式为___________ 。
(3)肼—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注。(Ci~Cs均为石墨电极,假设各装置在工作过程中溶液体积不变):
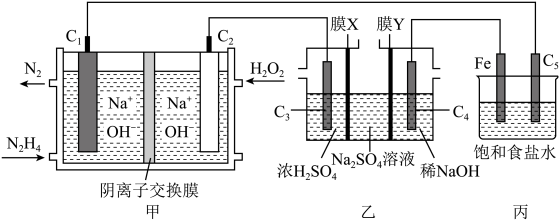
①甲装置Cl电极反应式为___________ ,该装置工作过程中,右侧溶液的pH___________ (填“变大”、“变小”、“不变”)。
②乙装置用于处理含高浓度硫酸钠的废水,膜X为___________ 交换膜(填“阳离子”"阴离子"或“质子”),通电一段时间后,废水中硫酸钠浓度由4.5mol/L降至0.5mol/L,若处理废水1m3,理论上消耗H2O2的物质的量为___________ (假定水分子不能通过膜X和膜Y)。
③工作时,利用丙装置对Fe电极进行防护,如果能有效防护,写出防护名称___________ ,如果不能有效防护,在上空中写出改进措施。
(1)氮和氢形成的无环氮烷,若分子中含n个氮原子,其分子式为
(2)火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
I.N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH=akJ·mol-1
Ⅱ.H2O(g)=H2O(l) ΔH2=bkJ·mol-1
Ⅲ.2H2O2(l)=2H2O(l)+O2(g) ΔH3=ckJ·mol-1
则N2H4(l)与H2O2(l)反应生成N2(g)和H2O(g)的热化学方程式为
(3)肼—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注。(Ci~Cs均为石墨电极,假设各装置在工作过程中溶液体积不变):

①甲装置Cl电极反应式为
②乙装置用于处理含高浓度硫酸钠的废水,膜X为
③工作时,利用丙装置对Fe电极进行防护,如果能有效防护,写出防护名称
您最近一年使用:0次
【推荐2】Ⅰ.下表标出的是元素周期表的一部分元素,回答下列问题:

①表中用字母标出的14种元素中,化学性质最不活泼的是____________ (用元素符号表示,下同),金属性最强的是____________ ,常温下单质为液态的非金属元素是____________ 。
②B、F、C气态氢化物中以________ (填分子式)最不稳定。
Ⅱ. 有短周期的A、B、C、D、E 五种元素,它们在周期表的位置如图所示。已知A原子最外层电子数是次外层电子数的2倍。试回答下列问题:
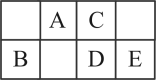
(1) 元素E在周期表中位于第_______ 周期_______ 族。
(2) 元素A的最高价氧化物的电子式为________ ,元素D的原子结构示意图为________ ;
(3) 比较C、D两种元素最高价氧化物对应水化物的酸性强弱:______ > ______ 。(用分子式表示)
(4)元素C的气态氢化物与元素E的最高价氧化物对应水化物化合生成的正盐的化学式为___________ ,该盐的晶体类型为________ 。
(5) ①元素B所在周期的简单离子半径最小的是______ 。(用离子符号表示)
②元素C、D的简单氢化物沸点较高的是______ 。(用分子式表示)
(6)请用电子式表示Na2S的形成过程____________________________________ 。

①表中用字母标出的14种元素中,化学性质最不活泼的是
②B、F、C气态氢化物中以
Ⅱ. 有短周期的A、B、C、D、E 五种元素,它们在周期表的位置如图所示。已知A原子最外层电子数是次外层电子数的2倍。试回答下列问题:

(1) 元素E在周期表中位于第
(2) 元素A的最高价氧化物的电子式为
(3) 比较C、D两种元素最高价氧化物对应水化物的酸性强弱:
(4)元素C的气态氢化物与元素E的最高价氧化物对应水化物化合生成的正盐的化学式为
(5) ①元素B所在周期的简单离子半径最小的是
②元素C、D的简单氢化物沸点较高的是
(6)请用电子式表示Na2S的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】X、Y、L、M为核电荷数依次增大的前20号主族元素。X2是密度最小的气体,Y、L与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与L组成的最简单化合物的电子式为_______ 。
(2)X与M组成的物质为_______ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为_______ 。该反应中每生成1molH2转移的电子数为_______ 。
(3)Y元素在周期表中的位置是_______ ,其含氧酸的化学式为_______ 。
(4)L与M形成的化合物中L的化合价是_______ 。
(1)X与L组成的最简单化合物的电子式为
(2)X与M组成的物质为
(3)Y元素在周期表中的位置是
(4)L与M形成的化合物中L的化合价是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的核外电子排布式为___________ 。
(2)B元素在周期表中的位置是___________ ;离子半径:B___________ A(填“大于”或“小于”)。
(3)C原子的电子排布图是___________ ,其原子核外有___________ 个未成对电子,能量最高的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(4)D原子的电子排布式为___________ ,D-的结构示意图是___________ 。
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为___________ ;B的最高价氧化物对应的水化物与D的氢化物的水溶液反应的化学方程式为___________ 。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物的水化物呈两性 |
| C | 在空气中含量第二,在地壳中含量第一 |
| D | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的核外电子排布式为
(2)B元素在周期表中的位置是
(3)C原子的电子排布图是
(4)D原子的电子排布式为
(5)B的最高价氧化物对应的水化物与A的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】随原子序数的递增,八种短周期元素(用字母表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
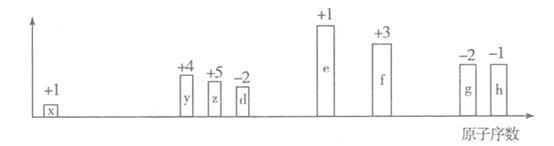
根据判断出的元素回答问题:
(1)y在元素周期表中的位置是____________________ 。z、d、e、f四种元素的简单离子中,半径最大的是_____________ (填离子符号)
(2)e的氢氧化物是一种重要的基本化工原料,写出工业上制备该氢氧化物的离子方程式___________________ 。
(3)z的氢化物和h的氢化物反应形成化合物A,A中含有的化学键类型为____________ ;
(4)含f的某化合物可用作净水剂的原理是_________________ (用离子方程式表示)
(5)25℃,f的最高价氧化物的水化物的Ksp=1.0 10-34,使含0.1 mol·L-1 f离子的溶液开始产生沉淀的pH为
10-34,使含0.1 mol·L-1 f离子的溶液开始产生沉淀的pH为________________ 。
(6)元素e和g组成的化合物B的水溶液中离子浓度由大到小的顺序为____________ 。

根据判断出的元素回答问题:
(1)y在元素周期表中的位置是
(2)e的氢氧化物是一种重要的基本化工原料,写出工业上制备该氢氧化物的离子方程式
(3)z的氢化物和h的氢化物反应形成化合物A,A中含有的化学键类型为
(4)含f的某化合物可用作净水剂的原理是
(5)25℃,f的最高价氧化物的水化物的Ksp=1.0
 10-34,使含0.1 mol·L-1 f离子的溶液开始产生沉淀的pH为
10-34,使含0.1 mol·L-1 f离子的溶液开始产生沉淀的pH为(6)元素e和g组成的化合物B的水溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知六种短周期元素A、B、C、D、E、F的原子序数依次增大,A的原子核内没有中子,A、D同主族,C、F同主族,A和B可形成5核10电子的阳离子,C与D形成的离子化合物D2C中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应,试回答下列问题:
(1)E在元素周期表中的位置是___________ 。
(2)写出A和B形成4核10电子分子的化学式是___________ 。
(3)C、D、F的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(4)写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式___________ 。
(5)已知周期表中存在对角相似规则,如Li与Mg在周期表中处于对角线位置则化学性质相似。根据“对角线规则”,铍(Be)的性质与上述六种元素中的___________ (填名称)相似,能溶于氢氧化钠溶液生成[Be(OH)4]2- ,请写出氢氧化铍与氢氧化钠溶液反应的化学方程式___________ 。
(6)A、C、D可形成多种二元化合物,下列说法不正确的___________(填字母)。
(7)能说明F的非金属性比氯弱的事实是___________ (填序号)。
①F的最高价氧化物的水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl-易被氧化
④HCl比F的氢化物稳定
⑤铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
(1)E在元素周期表中的位置是
(2)写出A和B形成4核10电子分子的化学式是
(3)C、D、F的简单离子半径由大到小的顺序为
(4)写出E的最高价氧化物的水化物与D的最高价氧化物的水化物反应的离子方程式
(5)已知周期表中存在对角相似规则,如Li与Mg在周期表中处于对角线位置则化学性质相似。根据“对角线规则”,铍(Be)的性质与上述六种元素中的
(6)A、C、D可形成多种二元化合物,下列说法不正确的___________(填字母)。
| A.C和A、D都可形式两种化合物 |
| B.A、D可形成的化合物中A显-1价 |
| C.D2C、D2C2中阴阳离子个数比均为1:2 |
| D.D2C和D2C2均能溶于A2C,并发生化合反应 |
①F的最高价氧化物的水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl-易被氧化
④HCl比F的氢化物稳定
⑤铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
您最近一年使用:0次



