X、Y、L、M为核电荷数依次增大的前20号主族元素。X2是密度最小的气体,Y、L与M三种元素的质子数均为5的倍数。回答下列问题:
(1)X与L组成的最简单化合物的电子式为_______ 。
(2)X与M组成的物质为_______ (填“共价”或“离子”)化合物,该物质可作为野外工作的应急燃料,其与水反应的化学方程式为_______ 。该反应中每生成1molH2转移的电子数为_______ 。
(3)Y元素在周期表中的位置是_______ ,其含氧酸的化学式为_______ 。
(4)L与M形成的化合物中L的化合价是_______ 。
(1)X与L组成的最简单化合物的电子式为
(2)X与M组成的物质为
(3)Y元素在周期表中的位置是
(4)L与M形成的化合物中L的化合价是
更新时间:2022-09-13 09:37:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素周期表的一部分如图,回答下列问题:
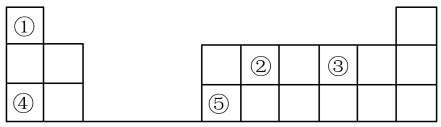
(1)表中五种元素中,最高价氧化物对应水化物的碱性最强的物质为__________ (填化学式);
②的一种核素常用于文物考古,该核素的符号为__________ .
(2)③与④可形成一种碱性氧化物W,用电子式表示W的形成过程:__________ .
(3)③④⑤的原子半径由大到小的顺序是__________ (填元素符号).
(4)少量的②的最高价氧化物和④的最高价氧化物对应的水化物反应的离子方程式为__________ .
(5)汽车电源蓄电池的正极材料是二氧化铅.已知 元素与②同主族且位于第六周期,下列关于
元素与②同主族且位于第六周期,下列关于 的说法中正确的是__________(填标号).
的说法中正确的是__________(填标号).
(6)①与②能形成18电子的分子M,M的分子式为__________ ,M的摩尔质量为__________ .

(1)表中五种元素中,最高价氧化物对应水化物的碱性最强的物质为
②的一种核素常用于文物考古,该核素的符号为
(2)③与④可形成一种碱性氧化物W,用电子式表示W的形成过程:
(3)③④⑤的原子半径由大到小的顺序是
(4)少量的②的最高价氧化物和④的最高价氧化物对应的水化物反应的离子方程式为
(5)汽车电源蓄电池的正极材料是二氧化铅.已知
 元素与②同主族且位于第六周期,下列关于
元素与②同主族且位于第六周期,下列关于 的说法中正确的是__________(填标号).
的说法中正确的是__________(填标号).| A.最外层有4个电子 | B.原子序数为82 | C.失电子能力比②弱 | D.可制作半导体材料 |
(6)①与②能形成18电子的分子M,M的分子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如下图所示,分别是前三周期主族元素原子半径与第一电离能的关系曲线。回答下列问题:
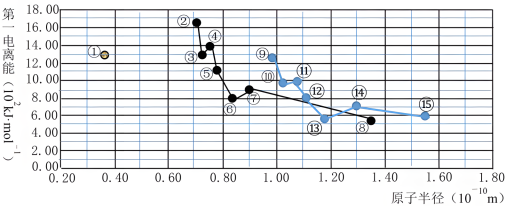
(1)图中编号为①⑥⑨的元素的元素符号分别是________ 、________ 、________ 。
(2)编号为⑮的元素原子的基态核外电子排布式为________ 。编号为⑬的元素原子的价层电子轨道表示式为________ 。元素②③⑭⑮对应的最简单离子半径由大到小的顺序为________ (用离子符号表示)。
(3)编号为⑨的元素在元素周期表中的位置为________ ,由它的原子和编号为⑮的元素的原子形成化合物的过程,用电子式可表示为________ 。
(4)由编号为①④⑤三种元素组成的一种结构式为 的物质,其中Y元素的化合价为
的物质,其中Y元素的化合价为________ 。该物质的电子式是________ 。

(1)图中编号为①⑥⑨的元素的元素符号分别是
(2)编号为⑮的元素原子的基态核外电子排布式为
(3)编号为⑨的元素在元素周期表中的位置为
(4)由编号为①④⑤三种元素组成的一种结构式为
 的物质,其中Y元素的化合价为
的物质,其中Y元素的化合价为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】有A、B、C、D四种元素,已知A元素原子的K层和M层电子数相同;B元素原子的L层比K层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的最外层电子数是次外层电子数的3倍。
(1)写出元素符号:A_______ ,D_______ 。
(2)A的原子结构示意图_______ ,B的离子结构示意图_______ ,C的离子结构示意图_______ 。
(3)C原子的电子式_______ 。
(4)A和B元素组成的物质的化学式为_______ ,它是由_______ (选填“原子”、“离子”或“分子”)构成的物质。
(5)由C和D可组成CD 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为_______ 。
(1)写出元素符号:A
(2)A的原子结构示意图
(3)C原子的电子式
(4)A和B元素组成的物质的化学式为
(5)由C和D可组成CD
 离子,一个CD
离子,一个CD 离子所带电子数为
离子所带电子数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】随着原子序数的递增,8种短周期元素原子半径的相对大小、最高正化合价或最低负化合价如图所示。请用相应的化学用语回答下列问题:
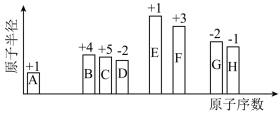
(1)元素G在元素周期表中的位置是_______ ,元素C的简单气态氢化物的电子式是_______ 。
(2)分子式为 的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是
的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是_______ 。
(3)元素 中,非金属性较强的是
中,非金属性较强的是_______ ,元素E、F的最高价氧化物的水化物反应的离子方程式为_______ 。
(4)化合物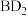 由固态变为气态需克服的微粒间作用力是
由固态变为气态需克服的微粒间作用力是_______ ,由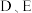 元素按照原子个数比为
元素按照原子个数比为 组成的化合物中所含的化学键是
组成的化合物中所含的化学键是_______ 。
(5)写出由 四种元素形成的一种离子化合物的化学式
四种元素形成的一种离子化合物的化学式_______ 。
(6)化合物 遇水反应生成一种气体和一种强碱,反应的化学方程式为
遇水反应生成一种气体和一种强碱,反应的化学方程式为_______ 。

(1)元素G在元素周期表中的位置是
(2)分子式为
 的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是
的物质可能是乙醇,也可能是二甲醚,这两种有机物的相互关系是(3)元素
 中,非金属性较强的是
中,非金属性较强的是(4)化合物
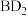 由固态变为气态需克服的微粒间作用力是
由固态变为气态需克服的微粒间作用力是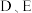 元素按照原子个数比为
元素按照原子个数比为 组成的化合物中所含的化学键是
组成的化合物中所含的化学键是(5)写出由
 四种元素形成的一种离子化合物的化学式
四种元素形成的一种离子化合物的化学式(6)化合物
 遇水反应生成一种气体和一种强碱,反应的化学方程式为
遇水反应生成一种气体和一种强碱,反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出这五种元素的名称。A___ ,B__ ,C__ ,D___ ,E__ 。
(2)写出D元素单质的结构式:___ 。
(3)写出下列物质的电子式:
E与B形成的化合物:__ ;A、B、E形成的化合物:__ ;D、E形成的化合物:___ 。
(4)A、B两元素组成的化合物A2B2属于___ (填“离子”或“共价”)化合物,存在的化学键是___ 。写出A2B2与水反应的化学方程式:__ 。
(1)写出这五种元素的名称。A
(2)写出D元素单质的结构式:
(3)写出下列物质的电子式:
E与B形成的化合物:
(4)A、B两元素组成的化合物A2B2属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】阅读下列信息:
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
A、B、C均为上表中的元素;
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙。
请回答:
⑴该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式_______________________ (有多组符合,写出任意一个即可)。
⑵元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是___________ 。
⑶甲、乙分别与氨反应生成丙、丁、戊三种盐。0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)_________________ 。
⑷很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5∶2时,还原产物可能为(填写化学式)__________ 、___________ 。
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
元素性质 | 元素编号 | |||||
① | ② | ③ | ④ | ⑤ | ⑥ | |
氢化物沸点(℃) | -33.4 | 100 | 19.54 | -87.7 | -60.7 | -84.9 |
主要化合价 | +5-3 | -2 | -1 | +5-3 | +6-2 | +7-1 |
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙。
请回答:
⑴该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式
⑵元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是
⑶甲、乙分别与氨反应生成丙、丁、戊三种盐。0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)
⑷很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5∶2时,还原产物可能为(填写化学式)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有四种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填写:
(1)A原子的外围电子排布式__________________________________ 。
(2)B元素在周期表中的位置________ ;离子半径:B________ A(填“大于”或“小于”)。
(3)C元素原子核外有________ 个未成对电子,能量最高的电子为________ 轨道上的电子,其轨道呈________ 形。
(4)D元素原子的价电子排布式为________ ,D-的结构示意图是________ 。
(5)B的最高价氧化物对应的水化物的化学式___________________ ,与A的最高价氧化物对应的水化物相比,碱性较强的是:_______________ (填化学式)。
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)A原子的外围电子排布式
(2)B元素在周期表中的位置
(3)C元素原子核外有
(4)D元素原子的价电子排布式为
(5)B的最高价氧化物对应的水化物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有部分短周期元素的性质或原子结构如下表:
(1)四种元素原子半径由大到小的顺序是(写元素符号)_________________________ 。
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式________ (用元素符号表示)。
(3)T元素的简单阴离子的结构示意图是______________________ ,
(4)证明该粒子的还原性比Z-强的离子方程式是____________________ .
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为_______________________ 。
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为____________ g。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 最外层电子数是电子层数的2倍 |
| Z | 元素最高正价是+7价 |
(1)四种元素原子半径由大到小的顺序是(写元素符号)
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式
(3)T元素的简单阴离子的结构示意图是
(4)证明该粒子的还原性比Z-强的离子方程式是
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.按要求完成下列方程式:
(1)单质铁与氯气在加热条件下反应的方程式是:___________ 。
(2)0.2mol 通入100mL 3mol/L的NaOH溶液,该总反应的离子方程式为:
通入100mL 3mol/L的NaOH溶液,该总反应的离子方程式为:______ 。
Ⅱ.科研人员最新研制了一种利用废钒催化剂(含有 、
、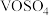 及不溶性残渣)制备
及不溶性残渣)制备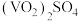 的方法如下图。
的方法如下图。
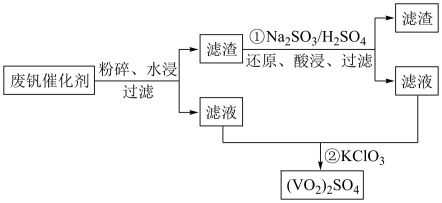
回答下列问题:
(3)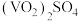 中钒的化合价
中钒的化合价___________ 。
(4)为了提高钒的浸出率,反应①用 和硫酸酸浸使催化剂中的
和硫酸酸浸使催化剂中的 转变成可溶于水的
转变成可溶于水的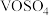 ,与水浸液合并,通过反应②用
,与水浸液合并,通过反应②用 氧化,使滤液中的
氧化,使滤液中的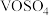 氧化成易溶于水的
氧化成易溶于水的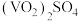 。则反应①的离子方程式为
。则反应①的离子方程式为___________ ;完善并配平反应②:___________ ___________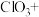 ___________
___________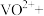 ___________=___________
___________=___________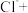 ___________
___________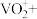 ___________。
___________。
(5) 能与盐酸反应产生
能与盐酸反应产生 和一种黄绿色气体,该气体能与
和一种黄绿色气体,该气体能与 溶液反应被吸收,则
溶液反应被吸收,则 、
、 、
、 还原性由强到弱的顺序是
还原性由强到弱的顺序是___________ 。
(6)在20.00 mL含0.1mol/L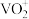 的溶液中加入0.195 g锌粉,恰好完全反应,则还原产物可能是___________(填序号)。
的溶液中加入0.195 g锌粉,恰好完全反应,则还原产物可能是___________(填序号)。
(1)单质铁与氯气在加热条件下反应的方程式是:
(2)0.2mol
 通入100mL 3mol/L的NaOH溶液,该总反应的离子方程式为:
通入100mL 3mol/L的NaOH溶液,该总反应的离子方程式为:Ⅱ.科研人员最新研制了一种利用废钒催化剂(含有
 、
、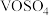 及不溶性残渣)制备
及不溶性残渣)制备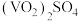 的方法如下图。
的方法如下图。
回答下列问题:
(3)
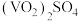 中钒的化合价
中钒的化合价(4)为了提高钒的浸出率,反应①用
 和硫酸酸浸使催化剂中的
和硫酸酸浸使催化剂中的 转变成可溶于水的
转变成可溶于水的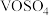 ,与水浸液合并,通过反应②用
,与水浸液合并,通过反应②用 氧化,使滤液中的
氧化,使滤液中的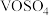 氧化成易溶于水的
氧化成易溶于水的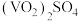 。则反应①的离子方程式为
。则反应①的离子方程式为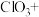 ___________
___________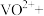 ___________=___________
___________=___________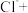 ___________
___________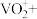 ___________。
___________。(5)
 能与盐酸反应产生
能与盐酸反应产生 和一种黄绿色气体,该气体能与
和一种黄绿色气体,该气体能与 溶液反应被吸收,则
溶液反应被吸收,则 、
、 、
、 还原性由强到弱的顺序是
还原性由强到弱的顺序是(6)在20.00 mL含0.1mol/L
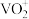 的溶液中加入0.195 g锌粉,恰好完全反应,则还原产物可能是___________(填序号)。
的溶液中加入0.195 g锌粉,恰好完全反应,则还原产物可能是___________(填序号)。A. | B.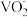 | C. | D.V |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】用铅蓄电池连接惰性电极电解一定量的CuSO4溶液,请回答下列问题:
(1)铅蓄电池放电时正极的电极反应式为___ 。
(2)用铅蓄电池给另一个铅蓄电池充电时,应将该铅蓄电池的正极与另一个铅蓄电池的___ 极相连接。
(3)用惰性电极电解熔融NaOH的化学方程式为___ 。
(4)若电解一段时间后向电解池溶液中加入1molCu2(OH)2CO3,可以使该溶液恢复至原来的浓度和体积,则在该电解过程中转移电子的数目为___ ,产生的气体在标准状况下的体积为___ 。
(5)已知PbSO4的Ksp=3×10‒7(25℃),将0.1mol/L的CuSO4溶液与0.05mol/L的Pb(NO3)2溶液等体积混合,充分反应后,c(Pb2+)=___ 。
(1)铅蓄电池放电时正极的电极反应式为
(2)用铅蓄电池给另一个铅蓄电池充电时,应将该铅蓄电池的正极与另一个铅蓄电池的
(3)用惰性电极电解熔融NaOH的化学方程式为
(4)若电解一段时间后向电解池溶液中加入1molCu2(OH)2CO3,可以使该溶液恢复至原来的浓度和体积,则在该电解过程中转移电子的数目为
(5)已知PbSO4的Ksp=3×10‒7(25℃),将0.1mol/L的CuSO4溶液与0.05mol/L的Pb(NO3)2溶液等体积混合,充分反应后,c(Pb2+)=
您最近一年使用:0次
【推荐3】工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下。回答下列问题:
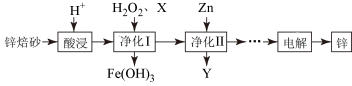
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是________ 。
②工业上利用反应ZnFe2(C2O4)3·6H2O ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是________ 。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是________________________ (任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有____________________________________________ 。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_________ ;试剂X的作用是_______ 。

(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
①ZnFe2O4中Fe的化合价是
②工业上利用反应ZnFe2(C2O4)3·6H2O
 ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中每生成1 mol ZnFe2O4转移电子的物质的量是(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是
(3)净化Ⅰ中H2O2参与反应的离子方程式为
您最近一年使用:0次



