乙烯和苯是来自石油和煤的两种重要化工原料。
(1)下列物质中,不能通过乙烯发生加成反应得到的是_______ (填字母)。
A.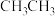 B.
B. C.
C.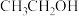
(2)将苯加入到盛有少量酸性高锰酸钾溶液的试管中,振荡,酸性高锰酸钾溶液不褪色,说明苯分子中_______ (填“有”或“没有”)碳碳双键。苯分子的空间构型为_______ 。
(3)一定条件下,乙烯和苯都能与溴发生反应。乙烯与溴发生反应的化学方程式为_______ ;苯与液溴在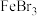 催化作用下发生的反应属于
催化作用下发生的反应属于_______ (填反应类型)。
(4)实验室制硝基苯的反应原理为_______ (用化学方程式表示),在制备和纯化硝基苯的实验中,下列操作未涉及的是_______ (填字母)。
A. B.
B.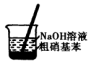 C.
C.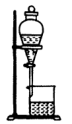 D.
D.
(1)下列物质中,不能通过乙烯发生加成反应得到的是
A.
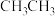 B.
B. C.
C.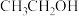
(2)将苯加入到盛有少量酸性高锰酸钾溶液的试管中,振荡,酸性高锰酸钾溶液不褪色,说明苯分子中
(3)一定条件下,乙烯和苯都能与溴发生反应。乙烯与溴发生反应的化学方程式为
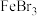 催化作用下发生的反应属于
催化作用下发生的反应属于(4)实验室制硝基苯的反应原理为
A.
 B.
B. C.
C. D.
D.
更新时间:2021-07-08 18:17:05
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】1,2-二溴乙烷可作汽油抗爆剂的添加剂,在实验室中可以用下图所示装置制备1,2二溴乙烷。其中A和F中装有乙醇和浓硫酸的混合液,D中的试管里装有液溴。可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。(夹持装置已略去)
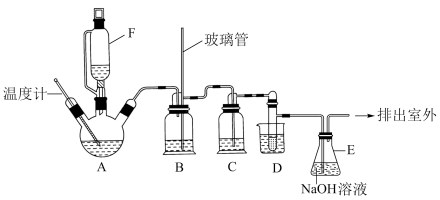
有关数据列表如下:
填写下列空白:
(1)A的仪器名称是____ 。
(2)安全瓶B可以防止倒吸,还可以检查实验进行时导管是否发生堵塞。请写出发生堵塞时瓶B中的现象____ 。
(3)A中发生反应的化学方程式为:____ ;D中发生反应的化学方程式为:____ 。
(4)在装置C中应加入____ (填字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)若产物中有少量副产物乙醚,可用___ (填操作名称)的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是____ 。

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g∙cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)A的仪器名称是
(2)安全瓶B可以防止倒吸,还可以检查实验进行时导管是否发生堵塞。请写出发生堵塞时瓶B中的现象
(3)A中发生反应的化学方程式为:
(4)在装置C中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)若产物中有少量副产物乙醚,可用
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发;但又不能过度冷却(如用冰水),其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】1,2-二溴乙烷在常温下是无色液体,密度是2.18g/cm3,沸点是131.4°C,熔点是9.79°C,不溶于水,易溶于醇、丙酮等有机溶剂。在实验室可用如图所示装置来制备1, 2-二溴乙烷,其中试管C中装有浓溴水。

(1)写出实验室制备乙烯的化学方程式:_______ ; 该反应属于_______ 反应(填反应类型);
(2)写出制备1, 2-二溴乙烷的化学方程式_______ ;该反应属于_______ 反应(填反应类型);
(3)安全瓶a可以防止倒吸,并可以检查实验进行时试管c是否发生堵塞,如果发生堵塞,a中的现象是:_______ ;
(4)容器b中NaOH溶液的作用是_______ ;
(5)将试管c置于冷水中的目的是_______ ;
(6)容器d中NaOH溶液的作用是_______ , 所发生反应的离子方程式为_______ 。

(1)写出实验室制备乙烯的化学方程式:
(2)写出制备1, 2-二溴乙烷的化学方程式
(3)安全瓶a可以防止倒吸,并可以检查实验进行时试管c是否发生堵塞,如果发生堵塞,a中的现象是:
(4)容器b中NaOH溶液的作用是
(5)将试管c置于冷水中的目的是
(6)容器d中NaOH溶液的作用是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】如图为由乙烯合成乙酸乙酯的流程图,回答下列问题:
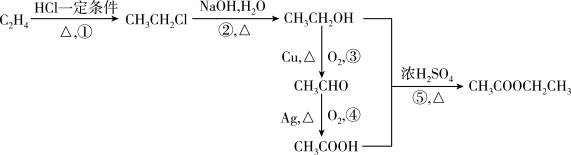
(1)反应①的反应类型是________________ ;反应②的反应类型是__________ 。
(2) 所含的官能团是
所含的官能团是________ ; 所含的官能团是
所含的官能团是_______ 。
(3)写出反应①的化学方程式:_____________________________ ;写出反应⑤的化学方程式:_____________________ 。
(4)物质A是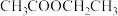 的同分异构体,A能与
的同分异构体,A能与 反应,放出
反应,放出 气体,则A的结构简式可能是
气体,则A的结构简式可能是_______ 。

(1)反应①的反应类型是
(2)
 所含的官能团是
所含的官能团是 所含的官能团是
所含的官能团是(3)写出反应①的化学方程式:
(4)物质A是
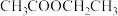 的同分异构体,A能与
的同分异构体,A能与 反应,放出
反应,放出 气体,则A的结构简式可能是
气体,则A的结构简式可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】德国化学家凯库勒认为,苯分子的结构中碳碳间以单、双键交替排列结合成环状。为了验证凯库勒的观点,某同学设计了以下实验方案:

①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量FeBr3,塞上橡皮塞,打开止水夹K1、K2、K3;
④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象。
(1)A中所发生反应的反应类型为________ ,能证明凯库勒观点错误的实验现象是________________________________________________________________ 。
(2)装置B的作用是___________________________________ 。
(3)装置A中发生反应的化学方程式:________________________________________ 。

①按如图所示的装置连接好仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量FeBr3,塞上橡皮塞,打开止水夹K1、K2、K3;
④待烧瓶a中收集满气体后,将导管b的下端插入烧杯D里的水中,挤压预先盛有水的胶头滴管,观察实验现象。
(1)A中所发生反应的反应类型为
(2)装置B的作用是
(3)装置A中发生反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】根据下列实验,总结苯的某些性质。
(1)向试管中加入 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是________________________ 。
(2)向试管中加入 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是_________________________________________________________________________________________ 。
(3)实验结论:苯________ (填“能”或“不能”)与溴水和酸性高锰酸钾溶液发生反应。
(4)根据上述实验结论可知:苯分子中________ (填“存在”或“不存在”)碳碳双键。
(1)向试管中加入
 苯,再加入
苯,再加入 溴水,振荡后静置。观察到的现象是
溴水,振荡后静置。观察到的现象是(2)向试管中加入
 苯,再加入
苯,再加入 酸性高锰酸钾溶液,振荡后静置。观察到的现象是
酸性高锰酸钾溶液,振荡后静置。观察到的现象是(3)实验结论:苯
(4)根据上述实验结论可知:苯分子中
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
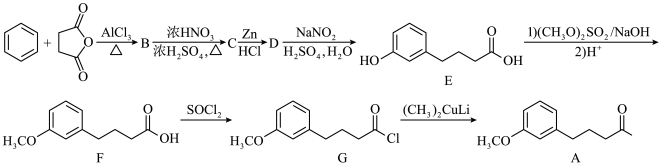
【推荐1】化合物A是合成雌酮激素的中间体,合成路线如下:
(1)若C的结构简式是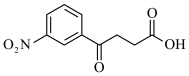 ,则B的结构简式是
,则B的结构简式是_______ 。化合物A中的含氧官能团的名称是_______ 。
(2)若D中只有两种含氧官能团,D的结构简式是_______ 。D的同分异构体W符合下列条件,则W的结构有_______ 种。
①苯环上只有三个取代基,其中一个是氨基
②1molW能与2molNaHCO3反应
③不能发生银镜反应,也不和FeCl3溶液发生反应
(3)B转化为C的化学方程式是_______ 。C转化为D的反应类型是_______ 。
(4)E与足量的氢氧化钠溶液反应的化学方程式为_______ 。
(5)设计由乙酸酐[(CH3CO)2O]和苯制备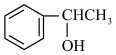 的合成路线:
的合成路线:_______ (无机试剂任选)。
(1)若C的结构简式是
 ,则B的结构简式是
,则B的结构简式是(2)若D中只有两种含氧官能团,D的结构简式是
①苯环上只有三个取代基,其中一个是氨基
②1molW能与2molNaHCO3反应
③不能发生银镜反应,也不和FeCl3溶液发生反应
(3)B转化为C的化学方程式是
(4)E与足量的氢氧化钠溶液反应的化学方程式为
(5)设计由乙酸酐[(CH3CO)2O]和苯制备
 的合成路线:
的合成路线:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硝基苯是重要的化工原料,用途广泛。制备反应如下:
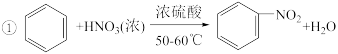
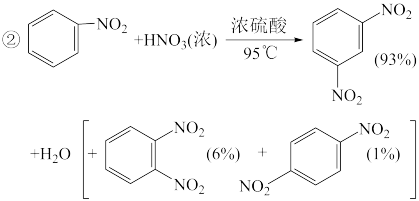
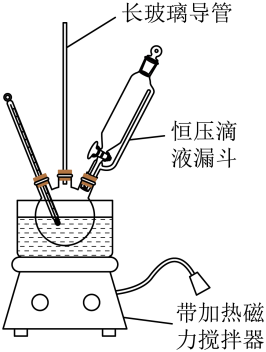
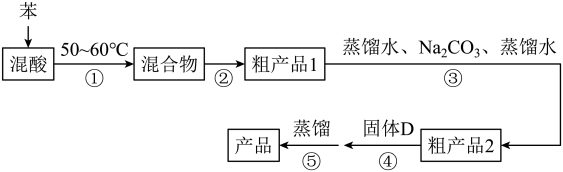
组装如右上图反应装置。 制备、提纯硝基苯流程如下:
可能用到的有关数据列表如下:
请回答下列问题:
(1)配制混酸应在烧杯中先加入__ ;实验装置中长玻璃管最好用________ 代替(填仪器名称);恒压滴液漏斗的优点是__________________ 。
(2)反应温度控制在50~60 ℃的原因是______________ ;反应结束后产物在___ 层(填“上”或者“下”),步骤②分离混酸和产品的操作名称是_____ 。
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?_____________ 。
(4)固体D的名称为_____ 。
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为______________________________________ 。
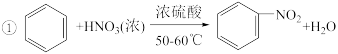


组装如右上图反应装置。 制备、提纯硝基苯流程如下:

可能用到的有关数据列表如下:
| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20 ℃)/g · cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | — | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | — | 338 | 1.84 | 易溶于水 |
(1)配制混酸应在烧杯中先加入
(2)反应温度控制在50~60 ℃的原因是
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?
(4)固体D的名称为
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
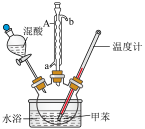
【推荐3】一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(含对硝基甲苯和邻硝基甲苯)。
实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15mL甲苯(密度为0.866g•cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度30℃,大约反应10分钟至三颈烧瓶底有大量淡黄色油状液体出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15g。
根据上述实验,回答下列问题:
(1)简述配制混酸的方法:___________ 。
(2)A仪器名称是___________ ,进水口是___________ (填"a"或"b")。
(3)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:___________ 。
(4)分离产品方案如下:___________ ,经测定,产品2的核磁共振氢谱中有5个峰,它的名称为___________ 。
(5)本实验中一硝基甲苯的产率为___________ (结果保留三位有效数字)。

| 有机物 | 密度(g•cm-3) | 沸点(℃) | 溶解性 |
| 甲苯 | 0.866 | 110.6 | 不溶于水 |
| 对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
| 邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
①配制浓硫酸和浓硝酸的混合物(混酸);
②在三颈烧瓶里装15mL甲苯(密度为0.866g•cm-3);
③装好其他药品,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度30℃,大约反应10分钟至三颈烧瓶底有大量淡黄色油状液体出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯共15g。
根据上述实验,回答下列问题:
(1)简述配制混酸的方法:
(2)A仪器名称是
(3)写出甲苯与混酸反应生成对硝基甲苯的化学方程式:
(4)分离产品方案如下:

(5)本实验中一硝基甲苯的产率为
您最近一年使用:0次



