名校
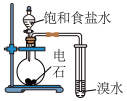
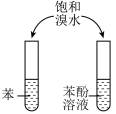
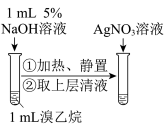
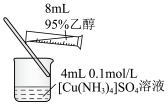
1 . 下列实验能达到 实验目的的是
|
|
|
|
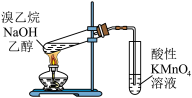
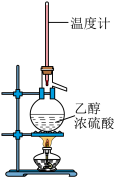
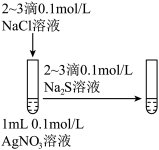
| A.验证乙炔可使溴水褪色 | B.验证生成物是乙烯 | C.证明羟基使苯环活化 | D.检验溴乙烷的水解产物Br− |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
2 . 如图所示是实验室利用乙醇消去反应制取乙烯并检验产物的实验装置图。回答以下问题。___________ 。
(2)为避免发生副反应,烧瓶 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为___________ 。
(3)反应中,观察到烧瓶 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。
①装置 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整___________ 。
②实验过程中,装置 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因___________ 。
(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为___________ ;反应一段时间后,装置C中溶液分层,有机物位于___________ (填“上”或“下”)层。
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择___________ (填序号)。
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓

(2)为避免发生副反应,烧瓶
 中的温度需要迅速升至170C∘,副反应的化学方程式为
中的温度需要迅速升至170C∘,副反应的化学方程式为(3)反应中,观察到烧瓶
 中混合液变为黑色,有气态副产物生成。
中混合液变为黑色,有气态副产物生成。①装置
 中所用试剂为滴加酚酞的
中所用试剂为滴加酚酞的 溶液,用于除去气体中的杂质,在虚线方框内将装置
溶液,用于除去气体中的杂质,在虚线方框内将装置 补充完整
补充完整②实验过程中,装置
 中溶液颜色变浅,用化学方程式说明原因
中溶液颜色变浅,用化学方程式说明原因(4)装置C中所用试剂为溴水,用于检验乙烯的生成,实验中在该装置处观察到的实验现象为
(5)有同学认为在装置C后应添加一个尾气处理装置,该装置中的试剂应选择
 酸性
酸性 溶液
溶液  碱石灰
碱石灰  浓
浓
您最近半年使用:0次
名校
解题方法
3 . 化学是以实验为基础的学科,下列实验操作、现象、结论均合理的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将 样品溶于稀 样品溶于稀 ,滴加KSCN溶液 ,滴加KSCN溶液 | 观察到溶液变红 |  样品已氧化变质 样品已氧化变质 |
| B | 将乙醇和浓硫酸混合溶液加热至170℃,将产生的气体通入溴水中 | 溴水褪色 | 有乙烯生成 |
| C | 取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化钠溶液中和酸,再加少量碘水 | 溶液未变蓝 | 淀粉已经完全水解 |
| D | 向盛有 溶液的试管中滴加碳酸氢钠溶液 溶液的试管中滴加碳酸氢钠溶液 | 产生白色沉淀 |  结合氢离子的能力比 结合氢离子的能力比 强 强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
455次组卷
|
2卷引用:2024届辽宁省协作校高三下学期一模大联考化学试题
名校
4 . 用下列实验装置进行相应实验,能达到实验目的是(夹持装置未画出)
| A制备晶体[Cu(NH3)4]SO4∙H2O | B检验溴乙烷消去产物 |
|
|
| C实验室制备乙烯 | D探究溶解度大小Ag2S<AgCl |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 溴乙烷是一种重要的有机合成中间体,沸点为38.4℃,密度为1.44g/cm3。实验室制备少量溴乙烷主要步骤如下:
步骤Ⅱ:向仪器A中依次加入搅拌磁子、9.2 g乙醇及18 mL水,冰水冷却下缓慢加入28 mL 18 mol/L H2SO4,冷却至室温,搅拌下加入24g NaBr。缓慢加热至无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得溴乙烷13.5 g。
已知: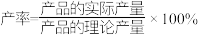
(1)仪器A的名称是________ ,冷凝管中冷却水进水口为________ (填“m”或“n”)。
(2)反应生成的主要副产物有乙烯,写出生成乙烯的化学反应方程式________ 。
(3)步骤2中需向锥形瓶内加入少量冰水并置于冰水浴中的目的是________ 。
(4)溴乙烷在水中的溶解性_______ (填“大于”、“小于”或“等于”)乙醇在水中的溶解性,其原因是________ 。
(5)为进一步制得纯净的溴乙烷,将粗品溴乙烷________ 。(写出实验步骤,实验中须使用的试剂:蒸馏水、无水CaCl2固体)
(6)计算本实验中溴乙烷的产率________ 。(保留三位有效数字)
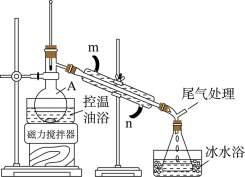
步骤Ⅱ:向仪器A中依次加入搅拌磁子、9.2 g乙醇及18 mL水,冰水冷却下缓慢加入28 mL 18 mol/L H2SO4,冷却至室温,搅拌下加入24g NaBr。缓慢加热至无油状物馏出为止。
步骤3:将馏出液转入分液漏斗,分出有机相。
步骤4:将分出的有机相转入分液漏斗,依次用12 mL H2O、12 mL Na2CO3溶液和12 mL H2O洗涤,分液,得粗产品,进一步提纯得溴乙烷13.5 g。
已知:
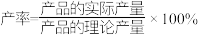
(1)仪器A的名称是
(2)反应生成的主要副产物有乙烯,写出生成乙烯的化学反应方程式
(3)步骤2中需向锥形瓶内加入少量冰水并置于冰水浴中的目的是
(4)溴乙烷在水中的溶解性
(5)为进一步制得纯净的溴乙烷,将粗品溴乙烷
(6)计算本实验中溴乙烷的产率
您最近半年使用:0次
6 . 利用如图装置验证制备乙烯时产生的杂质气体(加热、夹持及尾气处理装置已省略)。下列说法正确的是
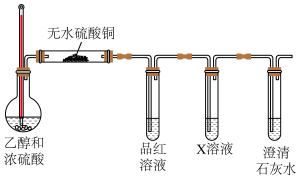
| A.无水硫酸铜的作用是干燥气体 |
B.品红溶液褪色说明有 产生 产生 |
C.X溶液为酸性 溶液 溶液 |
D.澄清石灰水变浑浊说明一定有 产生 产生 |
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
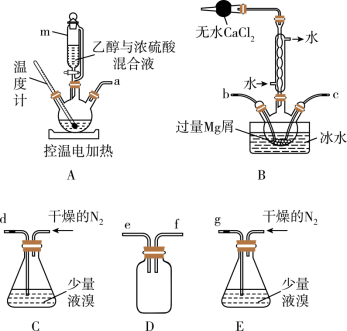
7 . 无水溴化镁常常做催化剂。选用如图所示装置(夹持装置略)采用镁屑与液溴为原料制备无水MgBr2。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是_______ 。
(2)装置A中使用仪器m的优点是_______ 。
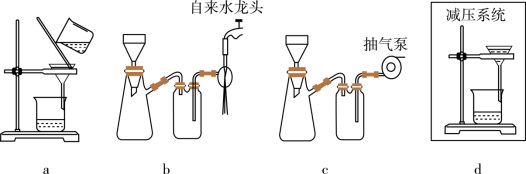
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是_______ (填序号)。_______ 。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是
(2)装置A中使用仪器m的优点是
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是
您最近半年使用:0次
解题方法
8 . 下列实验装置及药品能达到相应实验目的的是
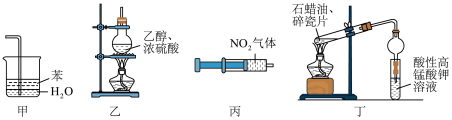
| A.利用甲装置在实验室中吸收尾气氨气 |
| B.利用乙装置在实验室中制备乙烯 |
| C.利用丙装置可验证压强对化学平衡的影响 |
| D.利用丁装置验证石蜡油受热分解产生乙烯 |
您最近半年使用:0次
解题方法
9 . 下列实验能够达到目的的是
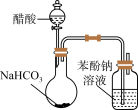
| A.用如图所示的装置比较醋酸、碳酸、苯酚的酸性强弱 |
| B.用金属钠检验乙醇中是否含有少量水 |
| C.向稀硝酸银溶液中逐滴滴加稀氨水,边滴边振荡,至生成的沉淀恰好溶解可以得到银氨溶液 |
| D.乙醇与浓硫酸170℃共热,将产生的气体通入溴水中,溴水褪色以证明产生的气体为乙烯 |
您最近半年使用:0次
名校
10 . 下列有关实验装置及用途叙述完全正确的是
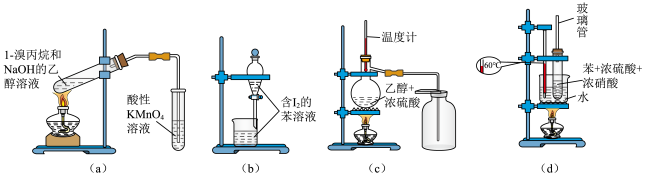
| A.a装置检验消去产物 | B.b装置苯萃取碘水中的I2,分出水层的操作 |
| C.c装置用于实验室制取并收集乙烯 | D.d装置用于实验室制硝基苯 |
您最近半年使用:0次