以CH4 (g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,其负极电极反应方程式为
| A.2H++ 2e- = H2 | B.CH4-8e-+2H2O=CO2+8H+ |
| C.2OH--2e-=O2+ H+ | D.CH4+4e-=C+ H+ |
2016高二·广东·竞赛 查看更多[1]
更新时间:2021-08-01 10:48:40
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列关于原电池的叙述中正确的是
| A.正极和负极必须是两种不同的金属 |
| B.原电池是把化学能转化成电能的装置 |
| C.原电池工作时,正极和负极上发生的都是氧化还原反应 |
| D.锌、铜和盐酸构成的原电池工作时,锌片上有6.5g锌溶解,正极就有0.1g氢气生成 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】关于图中原电池的说法不正确的是( )
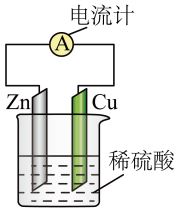

| A.Zn是负极 |
B.正极反应:2H++2e- H2↑ H2↑ |
C.负极反应:Zn-2e- Zn2+ Zn2+ |
| D.电流通过导线从锌片流向铜片 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】关于图中原电池的说法不正确的是( )


| A.Zn是负极 |
B.正极反应:2H++2e- H2↑ H2↑ |
C.负极反应:Zn-2e- Zn2+ Zn2+ |
| D.电流通过导线从锌片流向铜片 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】如果把2FeCl3+Cu→2FeCl2+CuCl2设计成原电池,则在正极上生成的离子是( )
| A.Cl- | B.Fe2+ | C.Cu2+ | D.Fe3+ |
您最近一年使用:0次
【推荐3】在《科学》(Science)中的一篇论文中,圣安德鲁斯的化学家描绘出了一种使用DMSO(二甲亚砜)作为电解液,并用多孔的黄金作为电极的锂—空气电池的实验模型,这种实验电池在充放电100次以后,其电池容量仍能保持最初的95%。该电池放电时在多孔的黄金上氧分子与锂离子反应,形成过氧化锂,其装置图如图所示。下列有关叙述正确的是


| A.多孔的黄金作为正极,负极的电极反应式为Li+-e-=Li |
| B.DMSO电解液能传递Li+,但不能换成水溶液 |
| C.该电池放电时每消耗2mol空气,转移4mol电子 |
| D.给该锂—空气电池充电时,金属锂接直流电源正极 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】我国新一代电动汽车因其“技术含量高”“节能环保”而备受关注。液态锂离子电池是一种被采用的车载电池,充电时该电池的电极反应分别为:6C+xLi+ +xe- =LixC6、LiNiO2-xe- = Li1-xNiO2+xLi+。下列有关该电池的说法中正确的是
| A.放电时,电子从正极流向电池的负极 |
| B.放电时,Li+向负极移动 |
C.该电池的总反应为6C+ LiNiO2 LixC6 + Li1-xNiO2 LixC6 + Li1-xNiO2 |
| D.充电时,阳极发生的电极反应为Li1-xNiO2 +xLi+ +xe- = LiNiO2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】一种微型锂电池以锂与石墨作电极材料、以四氯化铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成的溶液为电解质,具有容量大、电压稳定、工作温度范围宽(-56.7~71.1°C)等特点。下列有关说法中,不正确的是
| A.电池工作时,Li+向正极方向移动 |
| B.电池工作时,正极反应为2SOCl2+4e-=SO2+S+4Cl- |
| C.电池工作时,锂失去的电子与正极区析出硫的物质的量之比理论上为4:1 |
| D.电解质溶液要严禁混入水,因为锂会与水反应、SOCl2遇水会发生水解反应 |
您最近一年使用:0次