物质类别与元素化合价是研究物质性质的两个视角,下列是硫元素及其化合物的“价类二维图”。
I.根据要求回答下列问题:
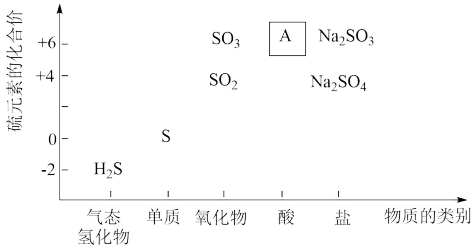
(1)写出图中A的化学式_______ 。
(2)SO2属于_______ (填“酸性”或“碱性”)氧化物,因此可与CaO、_______ (写出与CaO不同类别的一个具体物质)等反应。请写出CaO除去燃煤产生的SO2的化学方程式_______ (两个方程式)。
(3)重庆八中小王同学预测SO2具有还原性,其理论依据是_______ ,将SO2通入酸性高锰酸钾溶液中,下列实验事实能够证实SO2具有还原性的是_______ (填序号)。
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
II.硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生Cu(NO3)2以外,还产生了NO与NO2两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):
(4)反应产生的混合气体中,产生NO气体的体积为_______ L(标准状况下测定)。
(5)反应后, 的物质的量浓度为
的物质的量浓度为_______ mol/L。
I.根据要求回答下列问题:

(1)写出图中A的化学式
(2)SO2属于
(3)重庆八中小王同学预测SO2具有还原性,其理论依据是
①反应后溶液由紫色变为无色
②取反应后的溶液少许,加入BaCl2溶液,产生白色沉淀
③取反应后的溶液少许,加入Ba(NO3)2溶液,产生白色沉淀。
II.硝酸是一种具有强氧化性、腐蚀性的强酸。已知25.6gCu与过量的300mL、6mol/L硝酸充分反应,反应结束后,除了产生Cu(NO3)2以外,还产生了NO与NO2两种气体共13.44L(标况下测定),请计算(忽略反应前后溶液体积的变化):
(4)反应产生的混合气体中,产生NO气体的体积为
(5)反应后,
 的物质的量浓度为
的物质的量浓度为
更新时间:2021-08-02 11:37:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请按要求写出下列方程式。
(1)Al与NaOH溶液反应的离子方程式_______ 。
(2)工业生产漂白粉的化学方程式_______ 。
(3)Fe3O4与稀HNO3(具有强氧化性)溶液反应的离子方程式_______ 。
(4)氯化铝溶液与过量氨水反应的离子方程式_______ 。
(1)Al与NaOH溶液反应的离子方程式
(2)工业生产漂白粉的化学方程式
(3)Fe3O4与稀HNO3(具有强氧化性)溶液反应的离子方程式
(4)氯化铝溶液与过量氨水反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
(1)上述反应的离子方程式为___________ 。
(2)用单线桥表示该反应的电子转移___________ 。
(3)反应中HNO3的作用___________ 。
(1)上述反应的离子方程式为
(2)用单线桥表示该反应的电子转移
(3)反应中HNO3的作用
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
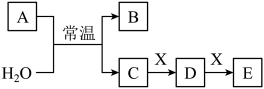
【推荐3】已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为___________ ;若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___________ 。(填字母)
a. 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液
(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入 溶液变红。
溶液变红。
①写出加热条件下C的浓溶液与X反应生成D的化学方程式___________ 。
②检验溶液D中还可能存在 的方法是
的方法是___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则
 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为a.
 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入
 溶液变红。
溶液变红。①写出加热条件下C的浓溶液与X反应生成D的化学方程式
②检验溶液D中还可能存在
 的方法是
的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10 mL)中通入Cl2,当B中溶液变黄时,停止通气
Ⅱ.打开活塞b,使约2 mL的溶液流入D试管中,检验取出溶液中的离子
Ⅲ.接着再向B中通入一定量的SO2气体
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子
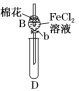
棉花中浸润的溶液为_______ ,目的是_______
Ⅰ.先向B中的FeCl2溶液(约10 mL)中通入Cl2,当B中溶液变黄时,停止通气
Ⅱ.打开活塞b,使约2 mL的溶液流入D试管中,检验取出溶液中的离子
Ⅲ.接着再向B中通入一定量的SO2气体
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子

棉花中浸润的溶液为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面根据海水资源综合利用,请回答下列问题:
(1)淡化海水的方法有________________ (写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________ (填化学式),之后________ (填操作名称),再加入适量________ (填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)由无水MgCl2制取金属镁的常用工业方法是__________________ 。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是__________ 。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式____________ 。再H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为_______________ 。
(1)淡化海水的方法有
(2)由无水MgCl2制取金属镁的常用工业方法是
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性 B.还原性 C.漂白性 D.酸性氧化物的性质
(1)SO2+Br2+2H2O=2HBr+H2SO4______
(2)SO2+2H2S=3S↓+2H2O______
(3)SO2+2NaOH=Na2SO3+H2O______
(4)SO2+Ca(OH)2=CaSO3↓+H2O______
A.氧化性 B.还原性 C.漂白性 D.酸性氧化物的性质
(1)SO2+Br2+2H2O=2HBr+H2SO4
(2)SO2+2H2S=3S↓+2H2O
(3)SO2+2NaOH=Na2SO3+H2O
(4)SO2+Ca(OH)2=CaSO3↓+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】我国农业因遭受酸雨而造成的损失每年高达15亿多元,为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
分析数据,回答以下问题:
①雨水样品呈酸性的原因是________________________________ (用化学方程式表示)。
②如果将刚取样的上述雨水和自来水(含有氯气)混合,pH将________ (填“变大”“变小”或“不变”)。
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,其原因可能是_______ (用化学方程式表示)。
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响________________ 。
(1)现有雨水样品1份,每隔一段时间测定该雨水样品的pH所得数据如下:
测试时间/h | 0 | 1 | 2 | 3 | 4 |
雨水的pH | 4.75 | 4.62 | 4.56 | 4.55 | 4.54 |
分析数据,回答以下问题:
①雨水样品呈酸性的原因是
②如果将刚取样的上述雨水和自来水(含有氯气)混合,pH将
(2)测定雨水样品时,每隔一定时间测定一次pH,发现pH逐渐变小,其原因可能是
(3)举一例说明这种雨水将给环境中的生物或非生物造成的影响
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业及汽车尾气已成为城市空气的主要污染源,研究其反应机理对于环境治理有重要意义。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=___________ kJ/mol。
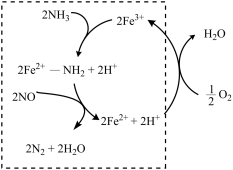
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。___________ 。
②反应过程图中,虚线方框里的过程可描述为___________ 。
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是___________ 。
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和___________ 。(填化学式)
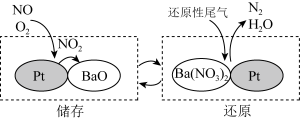
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。___________ 。
(1)硝酸厂尾气可以回收制备硝酸。已知:
①2NO(g)+O2(g)=2NO2(g) △H1=-113.0 kJ/mol
②3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ/mol
4NO2(g)+O2(g)+2H2O(g)=4HNO3(g) △H=
(2)液氨催化还原NO是重要的烟气脱硝技术。使用Fe2O3为催化剂,可能的反应过程如图所示。
②反应过程图中,虚线方框里的过程可描述为
③氨氮比会直接影响该方法的脱硝率。350℃时只改变氨气的投放量,NO的百分含量与氨氮比的关系如图所示。当
 >1.0时,烟气中NO含量反而增大,主要原因是
>1.0时,烟气中NO含量反而增大,主要原因是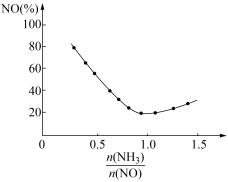
NO2被Na2CO3溶液吸收生成的三种盐分别是NaNO2、NaNO3和
(4)NSR (NOX储存还原)可有效减少氮氧化物排放。工作原理:通过BaO和Ba(NO3)2的相互转化实现NOX的储存和还原,如图所示。
您最近一年使用:0次



