元素的相对原子质量是该元素的天然同位素相对原子质量的加权平均值。例如:氯元素在自然界存在两种稳定的同位素,35Cl 的相对原子质量34.0968852,丰度75.77%,37Cl的相对原子质量36.965903, 丰度24.23%, 则氯元素的相对原子质量等于35.4527(36.965903 ×24.23%+34.0968852 ×75.77%)。《元素周期表》中,每种元素均只标注一个相对原子质量确定数值的情况即将改变。在新表中,氢、锂、硼、碳、氮、氧、硫、硅、氯、铊等十种元素的相对原子质量将采用新的区间方式给予标注,即有上限和下限,例如:硫元素目前标注的相对原子质量为32.065, 今后要依据其所处实际位置的不同而标注,在32.059和32.076的区间内。请回答下列问题:
(1)不同地区的元素相对原子质量有不同的数值,反映了什么事实_______________ ?
(2)举例说明,采用新的标注方法后,有什么重要的应用__________ ?
(1)不同地区的元素相对原子质量有不同的数值,反映了什么事实
(2)举例说明,采用新的标注方法后,有什么重要的应用
更新时间:2021-08-12 23:39:07
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年日本将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的不满。

(1)卡通形象中标+号的小球表示_______ (填微粒名称)。
(2)11g氚水(T216O)所含中子数为________ 个。
(3)氚和其同位素的物理性质________ (填“相同”或“不同”),化学性质________ (填“相同”或“不同”)。

(1)卡通形象中标+号的小球表示
(2)11g氚水(T216O)所含中子数为
(3)氚和其同位素的物理性质
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)①HClO的结构式为___________ ;
②水分子的空间构型___________ ;
③铁红的化学式___________ ;
(2)相同条件下,冰的密度比水小的原因是___________ ;
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为___________ ;
(4)用氯气制备“84”消毒液的离子方程式为___________ ,消毒液消毒衣服时要先用温水稀释后再浸泡一段时间,但温度不能高于50℃。则温度不宜过高的原因是___________ ;
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目___________ 。
(6) 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式___________ 。
(1)①HClO的结构式为
②水分子的空间构型
③铁红的化学式
(2)相同条件下,冰的密度比水小的原因是
(3)氧元素的一种核素,核内有10个中子,该核素的符号可表示为
(4)用氯气制备“84”消毒液的离子方程式为
(5)写出铝粉与氢氧化钠溶液的反应的化学方程式,并用单线桥表示电子转移的方向和数目
(6)
 遇水产生氢气,该反应的化学方程式
遇水产生氢气,该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铋(Bi)与磷(P)同主族且比P核外多三个电子层,铋及其化合物用途非常广泛。回答下列问题:
(1)Bi的天然同位素为 ,该核素的中子数为
,该核素的中子数为___________ 。
(2)Bi的原子结构示意图为______________ 。
(3)最近我国科研人员发现一种由[Bi2O2]2+和[BiS2Cl]2-层交替堆叠构成新型超导体Bi3O2S2Cl,该化合物中Bi的化合价为_______________ 。
(4)次碳酸铋晶体[(BiO)2CO3·0.5H2O,难溶于水]和枸橼酸铋钾均是常见铋剂类胃药。
①Bi(NO3)3溶液与Na2CO3溶液反应可制备次碳酸铋晶体,该反应的离子方程式为________ 。
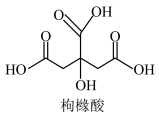
②制备1 mol枸橼酸铋(+3价)钾时,需消耗1 mol Bi(NO3)3溶液、2 mol枸橼酸(如图)和6 mol KOH溶液,同时生成3 mol KNO3。试写出枸橼酸铋钾的化学式:__________
(1)Bi的天然同位素为
 ,该核素的中子数为
,该核素的中子数为(2)Bi的原子结构示意图为
(3)最近我国科研人员发现一种由[Bi2O2]2+和[BiS2Cl]2-层交替堆叠构成新型超导体Bi3O2S2Cl,该化合物中Bi的化合价为
(4)次碳酸铋晶体[(BiO)2CO3·0.5H2O,难溶于水]和枸橼酸铋钾均是常见铋剂类胃药。
①Bi(NO3)3溶液与Na2CO3溶液反应可制备次碳酸铋晶体,该反应的离子方程式为
②制备1 mol枸橼酸铋(+3价)钾时,需消耗1 mol Bi(NO3)3溶液、2 mol枸橼酸(如图)和6 mol KOH溶液,同时生成3 mol KNO3。试写出枸橼酸铋钾的化学式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知下列八种化学符号:
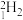






(1)其中,表示核素的符号共___________ 种。
(2)所表示的核素中,互为同位素的是________ 和___________ 。
(3)所表示的核素中,质量数相等但不能互称同位素的是________ 和________ 。

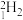






(1)其中,表示核素的符号共
(2)所表示的核素中,互为同位素的是
(3)所表示的核素中,质量数相等但不能互称同位素的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】1956年,美籍华人科学家吴健雄用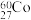 放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。
放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。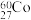 的衰变方程为:
的衰变方程为: ,其中,
,其中,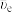 是反中微子,它的电荷数为0,静止质量可认为是0。
是反中微子,它的电荷数为0,静止质量可认为是0。
(1)下列关于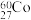 的说法中,错误的是______.
的说法中,错误的是______.
(2)在上述衰变方程中,衰变产物Ni的质量数A为________ ,核电荷数Z为________ 。
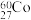 放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。
放射源进行实验验证了杨振宁和李政道的重要发现(此发现于1957年获得诺贝尔物理学奖)。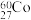 的衰变方程为:
的衰变方程为: ,其中,
,其中,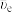 是反中微子,它的电荷数为0,静止质量可认为是0。
是反中微子,它的电荷数为0,静止质量可认为是0。(1)下列关于
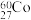 的说法中,错误的是______.
的说法中,错误的是______.| A.质子数是27 | B.电子数是27 | C.质量数是27 | D.中子数是60 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请回答下列问题:
(1) 轰击
轰击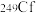 ,生成第118号元素并放出三个中子。写出配平的核反应方程式
,生成第118号元素并放出三个中子。写出配平的核反应方程式__________ 。
(2)推出二元氧化物(稳定物质)中含氧量最高的化合物__________ 。
(3)9.413g未知二元气体化合物中含有0.003227g电子。推出该未知物,写出化学式__________ 。
(1)
 轰击
轰击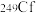 ,生成第118号元素并放出三个中子。写出配平的核反应方程式
,生成第118号元素并放出三个中子。写出配平的核反应方程式(2)推出二元氧化物(稳定物质)中含氧量最高的化合物
(3)9.413g未知二元气体化合物中含有0.003227g电子。推出该未知物,写出化学式
您最近一年使用:0次
【推荐2】环辛四烯及其双负离子
环辛四烯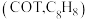 最稳定的结构为船型,与钾作用还原可得平面结构的环辛四烯双负离子
最稳定的结构为船型,与钾作用还原可得平面结构的环辛四烯双负离子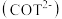 。
。
(1)简要解释环辛四烯与其双负离子具有不同稳定构型的原因_______ 。
(2)封闭的圆环中粒子的能级为: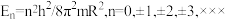 。式中n为描述能级的量子数,R是圆环的半径。m、h分别为电子的质量和Planck常数。若环辛四烯双负离子
。式中n为描述能级的量子数,R是圆环的半径。m、h分别为电子的质量和Planck常数。若环辛四烯双负离子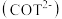 的离域
的离域 电子可近似描述为圆环中粒子,取
电子可近似描述为圆环中粒子,取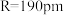 ,试求其电子基态跃起到第一激发态所吸收光的波长
,试求其电子基态跃起到第一激发态所吸收光的波长_______ 。
环辛四烯
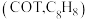 最稳定的结构为船型,与钾作用还原可得平面结构的环辛四烯双负离子
最稳定的结构为船型,与钾作用还原可得平面结构的环辛四烯双负离子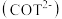 。
。(1)简要解释环辛四烯与其双负离子具有不同稳定构型的原因
(2)封闭的圆环中粒子的能级为:
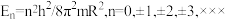 。式中n为描述能级的量子数,R是圆环的半径。m、h分别为电子的质量和Planck常数。若环辛四烯双负离子
。式中n为描述能级的量子数,R是圆环的半径。m、h分别为电子的质量和Planck常数。若环辛四烯双负离子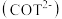 的离域
的离域 电子可近似描述为圆环中粒子,取
电子可近似描述为圆环中粒子,取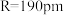 ,试求其电子基态跃起到第一激发态所吸收光的波长
,试求其电子基态跃起到第一激发态所吸收光的波长
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】元素同位素的类型及其天然丰度不仅决定原子量的数值,也是矿物年龄分析、反应机理研究等的重要依据。
(1)已知Cl 有两种同位素35C1和37Cl,二者丰度比为0.75:0.25; Rb 有85Rb和87Rb,二者丰度比为0.72 :0.28①写出气态中同位素组成不同的RbCl分子_____ 。
②这些分子有几种质量数_____ ?写出质量数,并给出其比例_____ 。
(2)年代测定是地质学的一 项重要工作。Lu-Hf法是上世纪80年代随着等离子发射光谱、质谱等技术发展而建立的一种新断代法。Lu有两种天然同位素: 176Lu 和177Lu; Hf 有六种天然同位素: 176Hf, 177Hf, 178Hf, 179Hf, 180Hf 和181Hf。176Lu 发生β衰变生成176Hf,半衰期为3.716 ×1010年。177Hf为稳定同位素且无放射性来源。地质工作者获得一块岩石样品,从该样品的不同部位取得多个样本进行分析。其中的两组有效数据如下:样本1, 175Hf 与177Hf的比值为0.28630 (原子比,记为176Hf/177Hf),177Lu/177Hf为0.42850;样本176Hf/177Hf为0.28239,177Lu/177Hf为0.01470
(一级反应,物种含量c随时间t变化的关系式: c=c0e-kt或1n =-kt,其中c0为起始含量)
=-kt,其中c0为起始含量)
①写出176Lu发生β衰变的核反应方程式(标出核电荷数和质量数)_____ 。
②计算176Lu衰变反应速率常数k_____ 。
③计算该岩石的年龄_____ 。
④计算该岩石生成时176Hf/177Hf的比值_____ 。。
(1)已知Cl 有两种同位素35C1和37Cl,二者丰度比为0.75:0.25; Rb 有85Rb和87Rb,二者丰度比为0.72 :0.28①写出气态中同位素组成不同的RbCl分子
②这些分子有几种质量数
(2)年代测定是地质学的一 项重要工作。Lu-Hf法是上世纪80年代随着等离子发射光谱、质谱等技术发展而建立的一种新断代法。Lu有两种天然同位素: 176Lu 和177Lu; Hf 有六种天然同位素: 176Hf, 177Hf, 178Hf, 179Hf, 180Hf 和181Hf。176Lu 发生β衰变生成176Hf,半衰期为3.716 ×1010年。177Hf为稳定同位素且无放射性来源。地质工作者获得一块岩石样品,从该样品的不同部位取得多个样本进行分析。其中的两组有效数据如下:样本1, 175Hf 与177Hf的比值为0.28630 (原子比,记为176Hf/177Hf),177Lu/177Hf为0.42850;样本176Hf/177Hf为0.28239,177Lu/177Hf为0.01470
(一级反应,物种含量c随时间t变化的关系式: c=c0e-kt或1n
 =-kt,其中c0为起始含量)
=-kt,其中c0为起始含量)①写出176Lu发生β衰变的核反应方程式(标出核电荷数和质量数)
②计算176Lu衰变反应速率常数k
③计算该岩石的年龄
④计算该岩石生成时176Hf/177Hf的比值
您最近一年使用:0次



