I.以下物质:①NaCl晶体②SO2③冰醋酸④铜⑤固体BaSO4⑥蔗糖(C12H22O11)⑦酒精(C2H5OH)⑧熔化的KHSO4⑨氨水⑩液氯。请回答下列问题(填相应序号):
(1)以上物质能导电的是_______ ;
(2)以上物质属于非电解质的是_______ ;
(3)以上物质属于强电解质的是_______ 。
II.室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。
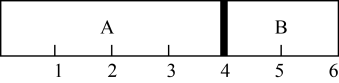
(4)A室混合气体所含分子总数为_______ (用NA表示阿伏加德罗常数)。
(5)实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氢气密度的_ 倍。
(6)若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在_____ 刻度处。
(1)以上物质能导电的是
(2)以上物质属于非电解质的是
(3)以上物质属于强电解质的是
II.室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1mol空气,此时活塞的位置如图所示。

(4)A室混合气体所含分子总数为
(5)实验测得A室混合气体的质量为34g,则该混合气体的密度是同温同压下氢气密度的
(6)若将A室H2、O2的混合气体点燃,恢复原温度后,最终活塞停留的位置在
更新时间:2021-08-24 20:31:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)现有12.8gCO和CO2混合气体,在标准状况下的体积为8.96L,该混合气体的平均摩尔质量为_______ ;
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为_______ ,密度之比为_______ 。
(3)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是_______ (填化学式),质量最大的是_______ (填化学式)。
(4)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、MgSO4三种溶液中的SO 都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为_______ 。
(5)同温同压下的氧气和氢气,若体积相同时,两种气体的质量比为_______ ,若质量相等时,两种气体的体积比为_______ 。
(6)Cl‒浓度为0.4mol·L‒1的MgCl2溶液的物质的量浓度为_______ mol·L-1,200mL该MgCl2溶液中含Mg2+的数目为_______ 。
(1)现有12.8gCO和CO2混合气体,在标准状况下的体积为8.96L,该混合气体的平均摩尔质量为
(2)同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为
(3)在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,所含分子数最多的是
(4)用等体积的0.1 mol·L-1的BaCl2溶液,可使相同体积的Fe2(SO4)3、Na2SO4、MgSO4三种溶液中的SO
 都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为
都恰好完全沉淀,则三种硫酸盐的物质的量浓度之比为(5)同温同压下的氧气和氢气,若体积相同时,两种气体的质量比为
(6)Cl‒浓度为0.4mol·L‒1的MgCl2溶液的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列填空。
(1)49gH2SO4中氧原子数为___________ 。
(2)标准状况下,氮气的密度为___________ 。
(3)同温同压下,0.4gH2与1.6gCH4的体积之比为______ ;二者混合后,所含H原子总数为_______ 。
(4)某金属氯化物MCl240.5g,含有0.6molCl-,则金属M的相对原子质量为_______ 。
(5)有下列物质:①熔融氯化钠②铜③氯化氢气体④稀硫酸⑤二氧化碳⑥碳酸氢钠粉末⑦蔗糖晶体⑧硫酸钡固体,请用序号填空:
i.属于电解质的是___________ (填序号,下同)。
ii.属于非电解质的是___________ 。
iii.写出碳酸氢钠的电离方程式___________ 。
(1)49gH2SO4中氧原子数为
(2)标准状况下,氮气的密度为
(3)同温同压下,0.4gH2与1.6gCH4的体积之比为
(4)某金属氯化物MCl240.5g,含有0.6molCl-,则金属M的相对原子质量为
(5)有下列物质:①熔融氯化钠②铜③氯化氢气体④稀硫酸⑤二氧化碳⑥碳酸氢钠粉末⑦蔗糖晶体⑧硫酸钡固体,请用序号填空:
i.属于电解质的是
ii.属于非电解质的是
iii.写出碳酸氢钠的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.(1)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为___________ 。
(2)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是___________ 。
II.按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:___________ ;
(2)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O 还原为Cr3+,该过程的离子反应方程式为:
还原为Cr3+,该过程的离子反应方程式为:______
(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为:______
(2)在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是
II.按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:
(2)在酸性条件下,向含铬废水中加入FeSO4,可将Cr2O
 还原为Cr3+,该过程的离子反应方程式为:
还原为Cr3+,该过程的离子反应方程式为:(3)在淀粉碘化钾溶液中,滴加少量次氯酸钠碱性溶液,立即会看到溶液变蓝色,离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】I.根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化。
现有下列九种物质:
①HCl气体 ②固体Cu ③乙醇 ④三氧化硫 ⑤熔融NaCl ⑥Al2O3固体 ⑦硫酸溶液 ⑧NaHCO3固体 ⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是___________ (填序号)。
(2)属于酸式盐的物质为___________ (填序号),其电离方程式为___________ 。
(3)属于两性氧化物的是___________ (填序号)。
II.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)在同温同压下,等质量的CO和CO2.其体积之比为___________ ,质子数之比为___________ 。
现有下列九种物质:
①HCl气体 ②固体Cu ③乙醇 ④三氧化硫 ⑤熔融NaCl ⑥Al2O3固体 ⑦硫酸溶液 ⑧NaHCO3固体 ⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是
(2)属于酸式盐的物质为
(3)属于两性氧化物的是
II.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氯化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)在同温同压下,等质量的CO和CO2.其体积之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)同温同压下,同体积的NH3和H2O(水蒸气)质量比是____________ 。
(2)0.3 mol NH3 分子中所含质子数与________ 个H2O分子中所含质子数相等。
(3)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是________ 。
(4)2molSO3和3molSO2其分子数之比为_______ ;相同状况下(均为气体)体积之比为_______ 。
(5)欲用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL。所需量取浓硫酸的体积为_______ mL。
(2)0.3 mol NH3 分子中所含质子数与
(3)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是
(4)2molSO3和3molSO2其分子数之比为
(5)欲用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL。所需量取浓硫酸的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现有下列物质:
①稀硫酸②蔗糖③熔融的 ④
④ 固体⑤
固体⑤ ⑥
⑥ ⑦
⑦
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ ,能导电的是___________ 。
(2)写出 和
和 按物质的量
按物质的量 在水溶液中发生的离子方程式:
在水溶液中发生的离子方程式:___________ 。
(3)分别写出①④在水溶液中的电离方程式:①___________ ;④___________ 。
(4)在两份相同的 溶液中,分别滴入一定浓度的
溶液中,分别滴入一定浓度的 、
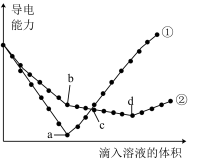
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。滴加
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。滴加 溶液的变化曲线为
溶液的变化曲线为___________ (填①或②),滴加 溶液至呈中性时的离子方程式为:
溶液至呈中性时的离子方程式为:___________ ,对应的点为___________ (填a或b或c或d)。
①稀硫酸②蔗糖③熔融的
 ④
④ 固体⑤
固体⑤ ⑥
⑥ ⑦
⑦
(1)属于电解质的是
(2)写出
 和
和 按物质的量
按物质的量 在水溶液中发生的离子方程式:
在水溶液中发生的离子方程式:(3)分别写出①④在水溶液中的电离方程式:①
(4)在两份相同的
 溶液中,分别滴入一定浓度的
溶液中,分别滴入一定浓度的 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。滴加
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。滴加 溶液的变化曲线为
溶液的变化曲线为 溶液至呈中性时的离子方程式为:
溶液至呈中性时的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)下列物质能导电是_______________ ,属于电解质是_______________ ,属于非电解质的是__________________ 。(填序号,多选或错选扣分)
①水银 ②烧碱 ③硫酸钡 ④氯化钠晶体 ⑤盐酸 ⑥ 蔗糖
(2)按要求完成下列各题:
①Na2SO4在水溶液中的电离方程式:____________________________________________ ;
②NaHCO3在水溶液中的电离方程式:____________________________________________ ;
③硫酸和氢氧化钡溶液反应的离子方程式:______________________________________ ;
④锌粒与稀硫酸反应的离子方程式:____________________________________________
①水银 ②烧碱 ③硫酸钡 ④氯化钠晶体 ⑤盐酸 ⑥ 蔗糖
(2)按要求完成下列各题:
①Na2SO4在水溶液中的电离方程式:
②NaHCO3在水溶液中的电离方程式:
③硫酸和氢氧化钡溶液反应的离子方程式:
④锌粒与稀硫酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质:①NaOH溶液;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩冰水混合物
;⑨蔗糖;⑩冰水混合物
(1)以上物质中属于混合物的是___________ (填序号),以上物质中属于电解质的是___________ (填序号)。
(2)写出制备物质⑤的离子方程式___________ ,在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈___________ 色,即制得 胶体。设计简单的方法判断胶体已制备成功
胶体。设计简单的方法判断胶体已制备成功___________ 。
(3)在足量④的水溶液中加入少量③,发生反应的离子方程式为___________ 。
(4)在含40g溶质的①溶液中缓缓通入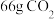 ,则反应后溶液的溶质
,则反应后溶液的溶质___________ (填化学式),该过程的离子反应方程式为___________ 。
 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧
;⑧ ;⑨蔗糖;⑩冰水混合物
;⑨蔗糖;⑩冰水混合物(1)以上物质中属于混合物的是
(2)写出制备物质⑤的离子方程式
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。设计简单的方法判断胶体已制备成功
胶体。设计简单的方法判断胶体已制备成功(3)在足量④的水溶液中加入少量③,发生反应的离子方程式为
(4)在含40g溶质的①溶液中缓缓通入
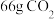 ,则反应后溶液的溶质
,则反应后溶液的溶质
您最近一年使用:0次



