根据如下两个反应,选用上述两种方法,计算出C(s)+ O2(g)=CO(g)的反应热ΔH。
O2(g)=CO(g)的反应热ΔH。
I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+ O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
①“虚拟路径”法
反应C(s)+O2(g)=CO2(g)的途径可设计如下:
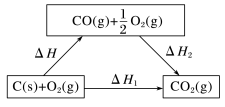
则ΔH=_______ =_______ kJ·mol-1。
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=___ =___ kJ·mol-1。
 O2(g)=CO(g)的反应热ΔH。
O2(g)=CO(g)的反应热ΔH。I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
II.CO(g)+
 O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH2=-283.0kJ·mol-1①“虚拟路径”法
反应C(s)+O2(g)=CO2(g)的途径可设计如下:

则ΔH=
②加合法
分析:找唯一:C、CO分别在I、II中出现一次
同侧加:C是I中反应物,为同侧,则“+I”
异侧减:CO是II中反应物,为异侧,则“-II”
调计量数:化学计量数相同,不用调整,则I-II即为运算式。所以ΔH=
更新时间:2021-09-03 19:21:34
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】(1)在101 kPa时,H2(g)在 1.00 mol O2(g)中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,H2的燃烧热为________ ,表示H2燃烧热的热化学方程式为________________________________ 。
(2)1.00 L 1.00 mol·L−1 H2SO4溶液与2.00 L 1.00 mol·L−1 NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热为________ ,表示其中和热的热化学方程式为____________________________ 。
(2)1.00 L 1.00 mol·L−1 H2SO4溶液与2.00 L 1.00 mol·L−1 NaOH溶液完全反应,放出114.6 kJ热量,该反应的中和热为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据已有内容的规律进行增补
(1)填化学方程式:
①2Na+2H2O=2NaOH+H2↑
②2HBr+Cl2=2HCl+Br2[
③2H2S+O2=2S+2H2O
④____________________________。
(2)已知
回答下列问题:
①比较熔点SiCl4 SiO2(填“>”或“<” ),理由
②工业制纯硅反应如下:
1/2 SiCl4(g)+H2(g)="=" 1/2Si(s)+2HCl(g)△H= +118KJ·mol-1
则H-H键能为 KJ·mol-1
(1)填化学方程式:
①2Na+2H2O=2NaOH+H2↑
②2HBr+Cl2=2HCl+Br2[
③2H2S+O2=2S+2H2O
④____________________________。
(2)已知
| 化学键 | Si-O | Si-Cl | H-Cl | Si-Si |
| 键能/KJ·mol-1 | 460 | 360 | 431 | 176 |
回答下列问题:
①比较熔点SiCl4 SiO2(填“>”或“<” ),理由
②工业制纯硅反应如下:
1/2 SiCl4(g)+H2(g)="=" 1/2Si(s)+2HCl(g)△H= +118KJ·mol-1
则H-H键能为 KJ·mol-1
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】煤燃烧后的主要产物是CO、CO2。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
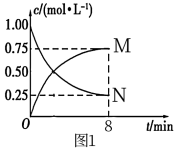

①图1中N表示的是______ (填化学式);0~8min内,以氢气表示的平均反应速率v(H2)=_______ mol • L-1 • min-1。
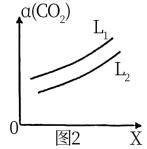
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是____________ (填“温度”或“压强”),L1________ (填“>”或“<”)L2。
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g) 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K_____________ 。
(1)以CO2为原料可制备甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1,向1L的恒容密闭容器中充入1mol CO2(g)和3mol H2(g),测得CO2(g)和CH3OH(g)浓度随时间的变化如图所示。


①图1中N表示的是
②在一定条件下,体系中CO2的平衡转化率(ɑ)与L和X的关系如图2所示,L和X分别表示温度和压强。X表示的物理量是
(2)向一体积为20L的恒容密闭容器中通入1molCO2发生反应:2CO2(g)
 2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
2CO(g)+O2(g),在不同温度下各物质的体积分数变化如图3所示。1600℃时反应达到平衡,则此时反应的平衡常数K
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】I.通过实验测定反应热
(1)经实验测定在一定温度下,0.2mol CH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量。该反应的热化学方程式为______ ;
Ⅱ.通过化学计算间接获得
(2)已知:拆开1mol的H-H、I-I、H-I共价键分别需要吸收的能量为436kJ、153kJ、299kJ,则反应H2(g)+I2(g)=2HI(g)的反应热△H =______ -9
kJ·mol-1。
(3)工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH(g)△H=-90.8kJ·mol-1 =
已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ·mol-1
H2(g)+ O2(g)═H2O(g)△H=-241.8kJ·mol-1
O2(g)═H2O(g)△H=-241.8kJ·mol-1
①H2燃烧热为______ kJ·mol-1
②CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=______ kJ·mol-1。
(1)经实验测定在一定温度下,0.2mol CH4(g)与足量H2O(g)完全反应生成CO2(g)和H2(g)吸收33kJ的热量。该反应的热化学方程式为
Ⅱ.通过化学计算间接获得
(2)已知:拆开1mol的H-H、I-I、H-I共价键分别需要吸收的能量为436kJ、153kJ、299kJ,则反应H2(g)+I2(g)=2HI(g)的反应热△H =
kJ·mol-1。
(3)工业生产甲醇的常用方法是:CO(g)+2H2(g)=CH3OH(g)△H=-90.8kJ·mol-1 =
已知:2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ·mol-1
H2(g)+
 O2(g)═H2O(g)△H=-241.8kJ·mol-1
O2(g)═H2O(g)△H=-241.8kJ·mol-1①H2燃烧热为
②CH3OH(g)+O2(g)=CO(g)+2H2O(g) △H=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】把煤作为燃料可通过下列两种途径。
途径I:C(s)+O2(g)= CO2(g)(放热Q1kJ)
途径II先制水煤气: C(s)+ H2O(g)= CO(g)+H2(g)(吸热Q2 kJ)
再燃烧X煤气:2CO(g)+O2(g)==2CO2(g) 2H2(g)+O2(g)=2H2O(g)(共放热Q3kJ)
试回答:
(1)途径I放出的热量-___________ (填“>”、“=”、“<”)途径II放出的热量。
(2)Q1、Q2、Q3的数学关系式是_________ 。
途径I:C(s)+O2(g)= CO2(g)(放热Q1kJ)
途径II先制水煤气: C(s)+ H2O(g)= CO(g)+H2(g)(吸热Q2 kJ)
再燃烧X煤气:2CO(g)+O2(g)==2CO2(g) 2H2(g)+O2(g)=2H2O(g)(共放热Q3kJ)
试回答:
(1)途径I放出的热量-
(2)Q1、Q2、Q3的数学关系式是
您最近一年使用:0次
【推荐1】I、在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量 N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
(1)写出该反应的热化学方程式_________________ .
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol﹣1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是________ kJ.
(3)丙烷燃烧可以通过以下两种途径:途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣a kJ·mol﹣1;途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol﹣1;2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=﹣c kJ·mol﹣1;2H2(g)+O2(g)═2H2O(l)△H=﹣d kJ·mol﹣1(abcd均为正值)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量_______ (填“大于”、“等于”或“小于”)途径II放出的热量.
II、利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol·L−1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L−1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)为什么所用NaOH溶液要稍过量?__________________________ 。
(2)假设盐酸和氢氧化钠溶液的密度都是1 g·cm−3,又知中和反应后生成溶液的比热容c=4.18 J·g−1·℃−1。为了计算中和热,某学生实验记录数据如下:
依据该学生的实验数据计算,该实验测得的中和热ΔH=____ kJ·mol−1_(结果保留一位小数)。
(3)不能用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是_________________ 。
 N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.
N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256kJ的热量.(1)写出该反应的热化学方程式
(2)已知H2O(l)═H2O(g);△H=+44kJ·mol﹣1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是
(3)丙烷燃烧可以通过以下两种途径:途径I:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣a kJ·mol﹣1;途径II:C3H8(g)═C3H6(g)+H2(g)△H=+b kJ·mol﹣1;2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=﹣c kJ·mol﹣1;2H2(g)+O2(g)═2H2O(l)△H=﹣d kJ·mol﹣1(abcd均为正值)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量
II、利用如图所示装置测定中和热的实验步骤如下:

①用量筒量取50 mL 0.50 mol·L−1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L−1 NaOH溶液,并用同一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)为什么所用NaOH溶液要稍过量?
(2)假设盐酸和氢氧化钠溶液的密度都是1 g·cm−3,又知中和反应后生成溶液的比热容c=4.18 J·g−1·℃−1。为了计算中和热,某学生实验记录数据如下:
| 实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | ||
| 1 | 20.0 | 20.0 | 23.0 |
| 2 | 20.1 | 20.1 | 23.2 |
| 3 | 20.1 | 20.1 | 24.2 |
| 4 | 20.2 | 20.2 | 23.4 |
(3)不能用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.作为国之重器,火箭的发射牵动了亿万人民的心。就像汽车、飞机需要添加汽油、航空煤油一样,火箭专用燃料被称为“推进剂”。在火箭推进器中装有强还原剂肼 和强氧化剂
和强氧化剂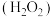 ,当它们混合时,即产生大量的
,当它们混合时,即产生大量的 和水蒸气,并放出大量热。已知
和水蒸气,并放出大量热。已知 液态肼和足量
液态肼和足量 反应,生成氮气和水蒸气,放出
反应,生成氮气和水蒸气,放出 的热量。
的热量。
(1)写出该反应的热化学方程式___________ 。
(2)已知
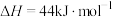 ,则
,则 液态肼燃烧生成氮气和液态水时,放出的热量是
液态肼燃烧生成氮气和液态水时,放出的热量是___________ kJ。(计算保留1位小数)
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是___________ 。
II.“长征五号”被称为“冰箭”,这缘于长征五号“肚子”里满满的深低温液氢液氧燃料,填补了我国大推力无毒无污染液体火箭发动机的空白,实现了绿色环保的研制理念。氢能是一种极具发展潜力的清洁能源,发展氢能正受到世界各国广泛关注。
(4)中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如图所示。下列说法不正确 的是___________。

 和强氧化剂
和强氧化剂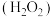 ,当它们混合时,即产生大量的
,当它们混合时,即产生大量的 和水蒸气,并放出大量热。已知
和水蒸气,并放出大量热。已知 液态肼和足量
液态肼和足量 反应,生成氮气和水蒸气,放出
反应,生成氮气和水蒸气,放出 的热量。
的热量。(1)写出该反应的热化学方程式
(2)已知

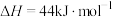 ,则
,则 液态肼燃烧生成氮气和液态水时,放出的热量是
液态肼燃烧生成氮气和液态水时,放出的热量是(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是
II.“长征五号”被称为“冰箭”,这缘于长征五号“肚子”里满满的深低温液氢液氧燃料,填补了我国大推力无毒无污染液体火箭发动机的空白,实现了绿色环保的研制理念。氢能是一种极具发展潜力的清洁能源,发展氢能正受到世界各国广泛关注。
(4)中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水,主要过程如图所示。下列说法

| A.整个过程实现了光能向化学能的转化 |
| B.过程II吸收能量 |
C.III发生的反应: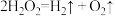 |
D.过程的总反应: |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】能源危机当前是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是__________________ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)水既是人们每天赖以生存的资源,也是工业生产的必要溶剂。
①已知H2 (g)+ O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
O2(g)=H2O(g)反应过程中能量变化如图,图中a代表____________________________________ ;
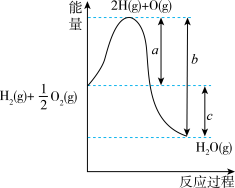
②已知:2H2(g)+O2(g)═2H2O(l) ΔH1=-285.8kJ∙mol﹣1;H2(g)═H2(l) ΔH2=-0.92kJ∙mol﹣1;O2(g)═O2(l) ΔH3=-6.84kJ∙mol﹣1;H2O(l)═H2O(g) ΔH4=+44.0kJ∙mol﹣1,请写出液氢和液氧生成气态水的热化学方程式:__________________________ 。
(3)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,金刚石和石墨相比较,________ (填”金刚石”或”石墨”)更稳定,石墨的燃烧热为________ kJ∙mol-1。
②12g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为________ kJ。
(1)下列做法有助于能源“开源节流”的是
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)水既是人们每天赖以生存的资源,也是工业生产的必要溶剂。
①已知H2 (g)+
 O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
O2(g)=H2O(g)反应过程中能量变化如图,图中a代表
②已知:2H2(g)+O2(g)═2H2O(l) ΔH1=-285.8kJ∙mol﹣1;H2(g)═H2(l) ΔH2=-0.92kJ∙mol﹣1;O2(g)═O2(l) ΔH3=-6.84kJ∙mol﹣1;H2O(l)═H2O(g) ΔH4=+44.0kJ∙mol﹣1,请写出液氢和液氧生成气态水的热化学方程式:
(3)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。

①在通常状况下,金刚石和石墨相比较,
②12g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为
您最近一年使用:0次



