下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题。
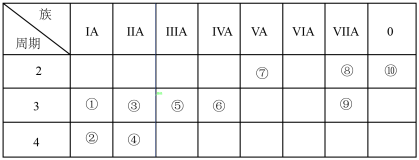
(1)③的原子结构示意图是___________ 。
(2)①~⑨中非金属性最强的元素是___________ (填化学式)。
(3)①和⑨两种元素组成的化合物中含有的化学键是___________ (填“共价键”或“离子键”)。
(4)①、⑤的最高价氧化物对应的水化物相互反应的离子方程式为___________ 。

(1)③的原子结构示意图是
(2)①~⑨中非金属性最强的元素是
(3)①和⑨两种元素组成的化合物中含有的化学键是
(4)①、⑤的最高价氧化物对应的水化物相互反应的离子方程式为
更新时间:2021/09/09 09:08:31
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分,请回答下列有关问题
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为_______ 。
(2)由元素①和④形成的四核分子的结构式为_______ 。
(3)由上述元素构成的淡黄色固体化合物的电子式为_______ ,该化合物所含的化学键类型为_______ (填“离子键”、“极性键”或“非极性键”),若将少量该固体投入到含有 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有_______ (用离子符号表示)。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑧_______ ⑩(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素①和④形成的四核分子的结构式为
(3)由上述元素构成的淡黄色固体化合物的电子式为
 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起。据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示。
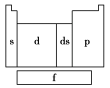
(1)在s区中,族序数最大、原子序数最小的元素,原子的价电子的电子云形状为___________ 。
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为 Fe2+:1s22s22p63s23p63d6,Fe3+:1s22s22p63s23p63d5,其中较稳定的是___________ 。
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为___________ 。
(4)在p区中,第二周期第ⅤA族元素原子的轨道表示式为___________ 。
(5)当今常用于核能开发的元素是铀和钚,它们在___________ 区中。

(1)在s区中,族序数最大、原子序数最小的元素,原子的价电子的电子云形状为
(2)在d区中,族序数最大、原子序数最小的元素,常见离子的电子排布式为 Fe2+:1s22s22p63s23p63d6,Fe3+:1s22s22p63s23p63d5,其中较稳定的是
(3)在ds区中,族序数最大、原子序数最小的元素,原子的价电子排布式为
(4)在p区中,第二周期第ⅤA族元素原子的轨道表示式为
(5)当今常用于核能开发的元素是铀和钚,它们在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】结合元素周期表,用化学用语回答下列问题:
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。_______

(2)表中所列元素,属于短周期元素的有____ ,属于主族元素的有___ 种;i元素位于第_____ 周期第______ 族。
(3)元素f是第____ 周期____ 族元素,请在如图方框中按氮元素的式样写出该元素的原子序数、元素符号、元素名称、相对原子质量。______
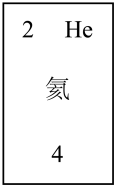
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是_______ (填标号)。
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
(1)表中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界。

(2)表中所列元素,属于短周期元素的有
(3)元素f是第

(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是
A. He和Ne B. B和Mg C. Al和Si D. F和Cl
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】元素在元素周期表中的位置,反映了元素的原子结构和元素的性质,如下图所示是短周期元素在周期表中的位置。
请回答以下问题:
(1)碳元素在元素周期表中的位置为___________ ,第三周期ⅥA族的元素是___________ (写元素名称)。
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4___________ (填“>”或“<”)HNO3;
②稳定性强弱:H2O___________ (填“>”或“<”)H2S;
③离子半径大小关系:O2-___________ (填“>”或“<”)Mg2+。
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为___________ ,甲的单质与水反应的离子方程式___________ 。
(4)标准状况下,22.4 LCl2的物质的量为___________ mol,质量为___________ g,含有的原子总数为___________ (用NA表示阿伏加德罗常数的数值)。
| 周期 | ⅠA | 0 | ||||||||
| 1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | He | ||
| 2 | Li | Be | B | C | N | O | F | Ne | ||
| 3 | Na | Mg | …… | Al | Si | P | S | Cl | Ar | |
(1)碳元素在元素周期表中的位置为
(2)根据元素周期律,请判断下列关系:
①酸性强弱:H3PO4
②稳定性强弱:H2O
③离子半径大小关系:O2-
(3)元素甲的原子是第三周期中半径最大的,该元素的核外电子排布示意图为
(4)标准状况下,22.4 LCl2的物质的量为
您最近一年使用:0次

 ”或“
”或“ ”)。
”)。

