铁是人类较早使用的金属之一。运用所学知识回答下列问题。
(1)用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液的操作是_______ (写出具体实验操作,结论)。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:_______ 。
(3)某研究性学习小组为检验FeCl3腐蚀铜后所得溶液中是否含有Fe2+,正确的实验方法是_______ (写出具体实验操作、现象、结论)。
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:
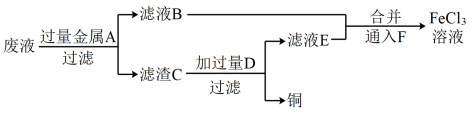
①滤渣C的成分为_______ (填化学式)。
②加过量D发生反应的离子方程式为_______ 。
③通入F发生反应的离子方程式为_______ 。
(1)用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液的操作是
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
(3)某研究性学习小组为检验FeCl3腐蚀铜后所得溶液中是否含有Fe2+,正确的实验方法是
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案:

①滤渣C的成分为
②加过量D发生反应的离子方程式为
③通入F发生反应的离子方程式为
更新时间:2021-09-22 18:49:42
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】明胶磷酸盐缓冲液可以用于肉毒梭菌检样的制备、微生物的分离和鉴别等。
I.央视《每周质量报告》曝光了少数明胶企业将皮革废料熬制成工业明胶,出售给个别制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为_______ ,Fe(CrO2)2属于_______ (填“酸”“碱”“盐”或“氧化物”)。
(2)明胶溶于水形成胶体,与溶液相比,胶体最本质的特征是_______ 。
(3)将饱和FeCl3溶液分别滴入下述液体中,并继续加热,能形成胶体的是_______ 。
II.磷元素的含氧酸有H3PO4、H3PO3 (亚磷酸)、H3PO2(次磷酸)等多种。其中已知H3PO2+NaOH(过量)=NaH2PO2+H2O。回答下列问题:
(4)H3PO2中磷元素的化合价是_______ ;上述反应______ (填“属于”或“不属于”)氧化还原反应。
(5)H3PO2属于______ (选填“一”“二”或“三”)元酸。NaH2PO2属于______ (填“正盐”或“酸式盐”)。
(6)H3PO2可将溶液中的Ag+转化为银,自身变为H3PO4,可用于化学镀银。利用H3PO2进行化学镀银的反应中,氧化剂与还原剂的个数比为_______ 。
I.央视《每周质量报告》曝光了少数明胶企业将皮革废料熬制成工业明胶,出售给个别制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知有毒胶囊中含有Fe(CrO2)2,其中铬元素是+3价,则其中铁元素的化合价为
(2)明胶溶于水形成胶体,与溶液相比,胶体最本质的特征是
(3)将饱和FeCl3溶液分别滴入下述液体中,并继续加热,能形成胶体的是
| A.冷水 | B.沸水 | C.NaCl溶液 | D.NaOH溶液 |
II.磷元素的含氧酸有H3PO4、H3PO3 (亚磷酸)、H3PO2(次磷酸)等多种。其中已知H3PO2+NaOH(过量)=NaH2PO2+H2O。回答下列问题:
(4)H3PO2中磷元素的化合价是
(5)H3PO2属于
(6)H3PO2可将溶液中的Ag+转化为银,自身变为H3PO4,可用于化学镀银。利用H3PO2进行化学镀银的反应中,氧化剂与还原剂的个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将饱和氯化铁溶液滴入沸水时,液体变为___ 色,得到的是___ ,反应的化学方程式为___ 。用此分散系进行实验:
(1)将其装入U形管内,用石墨作电极,接通直流电源,通电一段时间后发现阴极附近颜色___ ,这表明___ ,这种现象称为___ 。
(2)向其中加入饱和的硫酸铵溶液,发生的现象是___ ,原因是___ 。
(1)将其装入U形管内,用石墨作电极,接通直流电源,通电一段时间后发现阴极附近颜色
(2)向其中加入饱和的硫酸铵溶液,发生的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是______ 价。CrO2-是一种酸根离子,则Fe(CrO2)2属于________ (填“酸”“碱”“盐”或“氧化物”)。
(2)区分明胶的水溶液和K2SO4溶液的方法是_________ 。分离提纯明胶的水溶液和K2SO4溶液的混合物方法是______________ 。
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明SO42-能够透过半透膜:_____________________ 。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(2)区分明胶的水溶液和K2SO4溶液的方法是
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计一个实验证明SO42-能够透过半透膜:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】在两份完全相同的 溶液中,分别滴入
溶液中,分别滴入 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

(1)水溶液中 的电离方程式为
的电离方程式为___________ ;
(2)图示中曲线①表示的是___________ 溶液滴入 溶液中(填写化学式);
溶液中(填写化学式);
(3)用离子方程式表示 段的反应
段的反应___________ ;
(4)b点溶液中大量存在的离子是___________ (填写离子符号);
(5)对应溶液呈中性的曲线上的点为___________(填写选项字母)。
 溶液中,分别滴入
溶液中,分别滴入 、
、 溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
溶液,其导电能力随滴入溶液体积变化的曲线如图所示。
(1)水溶液中
 的电离方程式为
的电离方程式为(2)图示中曲线①表示的是
 溶液中(填写化学式);
溶液中(填写化学式);(3)用离子方程式表示
 段的反应
段的反应(4)b点溶液中大量存在的离子是
(5)对应溶液呈中性的曲线上的点为___________(填写选项字母)。
| A.a点 | B.b点 | C.c点 | D.d点 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室制备Cl2有三种常用方法:
a.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
b. KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
c.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是______ ,属于混合物的是______ ,属于电解质的是______ 。
(2)写出反应c对应的离子方程式:______ [已知HCl(浓)可拆分为H+和Cl-]。
(3)配平反应b的方程式______ 。
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应______ (填“a”“b”或“c”,下同);当得到等质量的Cl2时,消耗HCl的质量最多的是反应______ 。
a.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2Ob.
 KMnO4+
KMnO4+ HCl(浓)=
HCl(浓)= KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2Oc.KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
(1)常温下,医用酒精、Cl2、KMnO4、MnCl2、浓盐酸中能导电的是
(2)写出反应c对应的离子方程式:
(3)配平反应b的方程式
(4)当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】以下为中学化学中常见的几种物质;① ;②熔融NaCl;③
;②熔融NaCl;③ 固体:④
固体:④ ;⑤
;⑤ ;⑥75%的酒精;⑦
;⑥75%的酒精;⑦ 溶液;⑧NaOH溶液;⑨稀盐酸;⑩Fe。回答下列问题:
溶液;⑧NaOH溶液;⑨稀盐酸;⑩Fe。回答下列问题:
(1)上述物质中属于电解质的有___________ (填序号,下同);上述条件下能导电的有___________ 。
(2)写出 溶液和⑧反应的离子方程式:
溶液和⑧反应的离子方程式:___________ 。
(3)写出⑦与⑧反应的离子方程式___________ 。
(4)已知还原性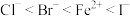 ,氧化性
,氧化性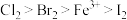 ,有一混合溶液,其中只含有
,有一混合溶液,其中只含有 、
、 、
、 ,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是___________ 。
 ;②熔融NaCl;③
;②熔融NaCl;③ 固体:④
固体:④ ;⑤
;⑤ ;⑥75%的酒精;⑦
;⑥75%的酒精;⑦ 溶液;⑧NaOH溶液;⑨稀盐酸;⑩Fe。回答下列问题:
溶液;⑧NaOH溶液;⑨稀盐酸;⑩Fe。回答下列问题:(1)上述物质中属于电解质的有
(2)写出
 溶液和⑧反应的离子方程式:
溶液和⑧反应的离子方程式:(3)写出⑦与⑧反应的离子方程式
(4)已知还原性
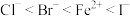 ,氧化性
,氧化性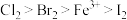 ,有一混合溶液,其中只含有
,有一混合溶液,其中只含有 、
、 、
、 ,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是________ 。
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是______ 。
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是_____ (填离子符号);实验①和③说明:在I- 过量的情况下,溶液中仍含有______ (填离子符号),由此可以证明该氧化还原反应为______ 。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为________ ;
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为
(3)乙组同学认为甲组的实验不够严谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是
(4)丙组同学取10 mL0.1mol/LKI溶液,加入6mL0.1mol/LFeCl3溶液混合。分别取2mL此溶液于3 支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀:
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组用下列装置(铁架台等支撑仪器略)探究氧化铁与乙醇的反应,并检验反应产物。

(1)组装好仪器后必须进行的操作是________________________ ,用2%的CuSO4溶液和10%的NaOH溶液配制Cu(OH)2悬浊液的注意事项是_________________________ 。
(2)为快速得到乙醇气体,可采取的方法是______________________ 。
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。取下小试管,加热,有砖红色沉淀生成,小试管中发生反应的化学方程式是:________________________ 。
(4)为了检验M的组成,进行下列实验:
① M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
② 经检验溶液中有铁离子和亚铁离子,检验铁离子的方法是________________________ ; 能得出的结论是______ (填写编号)。
a.M中一定有+3价和+2价铁,无0价铁
b.M中一定有+3价和0价铁,无+2价铁
c.M中一定有+3价,0价和+2价铁至少有一种
d.M中一定有+3价、+2价和0价铁
(5)若M的成分可表达为FeXOY,用CO还原法定量测定其化学组成。称取m g M样品进行定量测定,实验装置和步骤如下:

① 组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。正确的操作顺序是___________ (填写编号)
a.①⑤④③②⑥⑦⑧ b. ①⑤③④②⑥⑦⑧ c. ①③⑤④②⑦⑥⑧ d.①③⑤②④⑥⑦⑧
(6)若实验中每步反应都进行完全,反应后M样品质量减少了n g,则FeXOY中 =
=___________

(1)组装好仪器后必须进行的操作是
(2)为快速得到乙醇气体,可采取的方法是
(3)如图实验,观察到红色的Fe2O3全部变为黑色固体(M),充分反应后停止加热。取下小试管,加热,有砖红色沉淀生成,小试管中发生反应的化学方程式是:
(4)为了检验M的组成,进行下列实验:
① M能被磁铁吸引;加入足量稀硫酸,振荡,固体全部溶解,未观察到有气体生成;
② 经检验溶液中有铁离子和亚铁离子,检验铁离子的方法是
a.M中一定有+3价和+2价铁,无0价铁
b.M中一定有+3价和0价铁,无+2价铁
c.M中一定有+3价,0价和+2价铁至少有一种
d.M中一定有+3价、+2价和0价铁
(5)若M的成分可表达为FeXOY,用CO还原法定量测定其化学组成。称取m g M样品进行定量测定,实验装置和步骤如下:

① 组装仪器;②点燃酒精灯;③加入试剂; ④打开分液漏斗活塞;⑤检查气密性;⑥停止加热;⑦关闭分液漏斗活塞;⑧……。正确的操作顺序是
a.①⑤④③②⑥⑦⑧ b. ①⑤③④②⑥⑦⑧ c. ①③⑤④②⑦⑥⑧ d.①③⑤②④⑥⑦⑧
(6)若实验中每步反应都进行完全,反应后M样品质量减少了n g,则FeXOY中
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题:
(1)按要求书写下列方程式:
①向Ba(HCO3)2溶液中滴加过量NaOH溶液,反应的离子方程式:_______ 。
②完成下面的化学方程式:_______ 。
______ +______H2O2+_____H+=_____Mn2++_______H2O+_______
+______H2O2+_____H+=_____Mn2++_______H2O+_______
③完成下面的化学方程式:_______ 。
_____Na2Cr2O7+_____KI+_____HCl=_______CrCl3+____NaCl+_______KCl+_______I2+______
(2)铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场一种常见的补铁药品。
【规格】每片含琥珀酸亚铁0.1g
【适应症】用于缺铁性贫血症的预防及治疗。
【用量用法】成人治疗量0.2g/日~0.4g/日,小儿治疗量0.1g/日~0.3g/日。
【贮藏】避光、密封、在干燥处保存,该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率超过10.00%时不能再服用。
①为了检验某药店出售的“速力菲”是否被完全氧化,实验室应选用的检验试剂为_______ ;
②实验室可采用的H2SO4酸化的KMnO4溶液,对“速力菲”的Fe2+进行滴定(假设药品中,其他成分不与KMnO4反应)。请写出该离子方程式:_______ 。
③称量上述含铁元素质量分数为20.00%的“速力菲”10.00g,将其全部溶于稀H2SO4中,配制成1000.00mL溶液,取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。该药品中Fe2+的氧化率为_______ ,该药品可以服用吗?_______ (填“可以”“不可以”)。
(1)按要求书写下列方程式:
①向Ba(HCO3)2溶液中滴加过量NaOH溶液,反应的离子方程式:
②完成下面的化学方程式:
______
 +______H2O2+_____H+=_____Mn2++_______H2O+_______
+______H2O2+_____H+=_____Mn2++_______H2O+_______③完成下面的化学方程式:
_____Na2Cr2O7+_____KI+_____HCl=_______CrCl3+____NaCl+_______KCl+_______I2+______
(2)铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场一种常见的补铁药品。
【规格】每片含琥珀酸亚铁0.1g
【适应症】用于缺铁性贫血症的预防及治疗。
【用量用法】成人治疗量0.2g/日~0.4g/日,小儿治疗量0.1g/日~0.3g/日。
【贮藏】避光、密封、在干燥处保存,该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率超过10.00%时不能再服用。
①为了检验某药店出售的“速力菲”是否被完全氧化,实验室应选用的检验试剂为
②实验室可采用的H2SO4酸化的KMnO4溶液,对“速力菲”的Fe2+进行滴定(假设药品中,其他成分不与KMnO4反应)。请写出该离子方程式:
③称量上述含铁元素质量分数为20.00%的“速力菲”10.00g,将其全部溶于稀H2SO4中,配制成1000.00mL溶液,取出20.00mL,用0.01mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL。该药品中Fe2+的氧化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学与我们的生活、生产、环境、资源利用等息息相关。回答下列问题:
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是_______ ,会造成酸雨的物质是_______ ,会导致光化学烟雾的物质是_______ 。
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式_______ 。
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是_______ (填化学式)。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl—形式存在。现要消毒1.00 m3生活污水,分别用Cl2和ClO2来消毒处理,所耗Cl2与ClO2的质量比值为 _______ (保留小数点后2位)。
(1)大气中下列气体含量的升高会对环境产生一定的影响,用物质的序号填空,过量会导致温室效应加剧的主要物质是
①二氧化碳 ②二氧化硫 ③氮氧化物NOx
(2)电子工业常用质量分数为30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与铜反应的离子方程式
(3)饮用水消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一,漂白粉是常用的消 毒剂,其有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】结合所学内容,完成下列问题:
(1)刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出反应的离子反应方程式_______ 。
(2)呼吸面具中,Na2O2起反应的化学方程式_______ 。
(3)在标准状况下,112mL某气体的质量为0.32g,试计算这种气体的相对分子质量_______ 。
(4)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓) CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为__ ;如果产生标准状况下22.4LCO2,则转移的电子的物质的量为__ mol。
(1)刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2,请写出反应的离子反应方程式
(2)呼吸面具中,Na2O2起反应的化学方程式
(3)在标准状况下,112mL某气体的质量为0.32g,试计算这种气体的相对分子质量
(4)红热的木炭与浓硝酸反应的化学方程式为:C+4HNO3(浓)
 CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
CO2↑+4NO2↑+2H2O,该反应中氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】铁是人类较早使用的金属之一,请按要求完成下列问题。
(1)在自然界中,铁元素主要以___ (填写“游离态”或“化合态”)形式存在
(2)下列铁的化合物中,不能直接化合得到的是___ (用字母代号填)。
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.Fe(OH)3
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:4FeO +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
①Fe(OH)3胶体分散质粒子的直径范围是___ 。
②该反应中H2O是___ 。
A.氧化剂 B.还原剂 C.被氧化 D.被还原
③高铁酸钾(K2FeO4)能杀灭水中细菌的原因是___ 。
(4)电子工业常用30%左右的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,某同学设计下列方案:
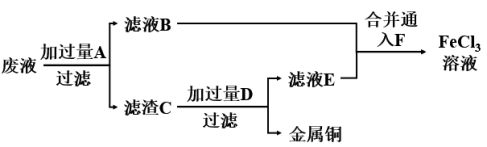
①实验室用无水氯化铁固体粗略配制30%的FeCl3溶液,需要的主要玻璃仪器除了量筒外还有___ 。
②写出FeCl3溶液与铜箔发生反应的离子方程式___ 。
③滤渣C的成分___ (填写化学式)。
④现用500g32.5%FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的FeCl3的质量至少为___ g。
(1)在自然界中,铁元素主要以
(2)下列铁的化合物中,不能直接化合得到的是
A.Fe3O4 B.FeCl2 C.Fe(OH)2 D.Fe(OH)3
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,与水反应可生成透明的红褐色胶体,反应原理:4FeO
 +10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-①Fe(OH)3胶体分散质粒子的直径范围是
②该反应中H2O是
A.氧化剂 B.还原剂 C.被氧化 D.被还原
③高铁酸钾(K2FeO4)能杀灭水中细菌的原因是
(4)电子工业常用30%左右的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。为了从腐蚀废液中回收铜,并重新获得FeCl3溶液,某同学设计下列方案:

①实验室用无水氯化铁固体粗略配制30%的FeCl3溶液,需要的主要玻璃仪器除了量筒外还有
②写出FeCl3溶液与铜箔发生反应的离子方程式
③滤渣C的成分
④现用500g32.5%FeCl3溶液制造印刷电路板,生产后的腐蚀废液用该同学设计方案处理,最终获得氯化铁溶液中的FeCl3的质量至少为
您最近一年使用:0次



