现有Al3+、NH 、CO
、CO 、HCO
、HCO 等离子,回答下列问题:
等离子,回答下列问题:
(1)在强酸性条件下能够存在的离子是___________ ;
(2)在强碱性条件下能够存在的离子是___________ ;
(3)在强酸性和强碱性条件下都不能存在的离子是___________ ,写出对应离子方程式:___________ ;___________ ;
(4)由Na+、NH 、Ba2+、Cu2+、OH-、Fe3+、SO
、Ba2+、Cu2+、OH-、Fe3+、SO 、Cl-等八种离子中的六种两两组成的A、B、C三种化合物(它们不含有共同离子,已知NH
、Cl-等八种离子中的六种两两组成的A、B、C三种化合物(它们不含有共同离子,已知NH 与OH-反应有碱性气体生成)。
与OH-反应有碱性气体生成)。
①A、B、C均易溶于水,形成无色溶液;
②将A、B、C三种物质的溶液相互作用时,发现A与B混合后产生有刺激性气味的气体,此气体使湿润红色石蕊试纸变蓝,B与C混合产生白色沉淀,则:A、B、C的化学式分别为___________ 、___________ 、___________ 。
 、CO
、CO 、HCO
、HCO 等离子,回答下列问题:
等离子,回答下列问题:(1)在强酸性条件下能够存在的离子是
(2)在强碱性条件下能够存在的离子是
(3)在强酸性和强碱性条件下都不能存在的离子是
(4)由Na+、NH
 、Ba2+、Cu2+、OH-、Fe3+、SO
、Ba2+、Cu2+、OH-、Fe3+、SO 、Cl-等八种离子中的六种两两组成的A、B、C三种化合物(它们不含有共同离子,已知NH
、Cl-等八种离子中的六种两两组成的A、B、C三种化合物(它们不含有共同离子,已知NH 与OH-反应有碱性气体生成)。
与OH-反应有碱性气体生成)。①A、B、C均易溶于水,形成无色溶液;
②将A、B、C三种物质的溶液相互作用时,发现A与B混合后产生有刺激性气味的气体,此气体使湿润红色石蕊试纸变蓝,B与C混合产生白色沉淀,则:A、B、C的化学式分别为
更新时间:2021-09-28 20:48:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】工厂的工业废水,不可直接往江河排放,否则会造成严重公害。某河道两旁有甲、乙两厂,它们排出的工业废水各含有K+、Fe3+、Ba2+、Ag+、Cl-、 、
、 、OH-中的四种。又知甲厂污水pH>7。
、OH-中的四种。又知甲厂污水pH>7。
(1)甲厂污水中含有的四种离子可能是:_______ 。
(2)乙厂污水中含有的四种离子可能是:_______ 。
(3)乙厂进行废水处理的方法之一,是可往废水中加入一定量的_______ (选填;活性炭、硫酸亚铁、铁粉),可以回收其中的金属_______ (填元素符号)。
(4)消除污染的另一种重要措施是将甲、乙两厂的废水按比例混合,可使废水中的_____ (填离子符号)转化为沉淀,再排放则大大降低污染程度。过滤,所得废水主要含______ ,可用于浇灌农田。
 、
、 、OH-中的四种。又知甲厂污水pH>7。
、OH-中的四种。又知甲厂污水pH>7。(1)甲厂污水中含有的四种离子可能是:
(2)乙厂污水中含有的四种离子可能是:
(3)乙厂进行废水处理的方法之一,是可往废水中加入一定量的
(4)消除污染的另一种重要措施是将甲、乙两厂的废水按比例混合,可使废水中的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示,请回答:
(1)三次检测结果中第__________ 次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(可选试剂:盐酸、硝酸、氯化钡、硝酸钡、硝酸银):首先,向溶液中滴加_______ 溶液(填化学式),其目的是_________ ;其次,然后继续加入过量的该溶液,其目的是_______________ ;第三,向滤液中加入___________ 溶液(填化学式),其目的是_______________ ;第四,过滤,再向滤液中加入_________ 溶液(填化学式),其目的是____________ 。
| 检测次数 | 溶液中检测出的溶质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子(可选试剂:盐酸、硝酸、氯化钡、硝酸钡、硝酸银):首先,向溶液中滴加
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某工厂废液中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,为确定废液中离子组成,设计了如下实验:
中的几种离子,为确定废液中离子组成,设计了如下实验:
(1)取 废液于锥形瓶中,逐滴加入足量
废液于锥形瓶中,逐滴加入足量 溶液并加热,生成标准状况下的气体
溶液并加热,生成标准状况下的气体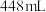 ,同时生成
,同时生成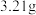 沉淀。该溶液中一定含有的阳离子是
沉淀。该溶液中一定含有的阳离子是______ (填离子符号)。
(2)另取 废液于锥形瓶中,滴加足量氯化钡溶液,生成白色沉淀
废液于锥形瓶中,滴加足量氯化钡溶液,生成白色沉淀 ;再加入足量稀盐酸,无明显变化。综合(1)(2)中实验可确定原废液中肯定含有的阴离子为
;再加入足量稀盐酸,无明显变化。综合(1)(2)中实验可确定原废液中肯定含有的阴离子为______ (填离子符号)。写出生成白色沉淀的离子方程式:______ 。
(3)综上实验,溶液中一定不存在的离子有______ (填离子符号,下同),溶液中可能存在的离子为______ ,
______  。
。
 、
、 、
、 、
、 、
、 、
、 、
、 中的几种离子,为确定废液中离子组成,设计了如下实验:
中的几种离子,为确定废液中离子组成,设计了如下实验:(1)取
 废液于锥形瓶中,逐滴加入足量
废液于锥形瓶中,逐滴加入足量 溶液并加热,生成标准状况下的气体
溶液并加热,生成标准状况下的气体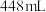 ,同时生成
,同时生成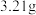 沉淀。该溶液中一定含有的阳离子是
沉淀。该溶液中一定含有的阳离子是(2)另取
 废液于锥形瓶中,滴加足量氯化钡溶液,生成白色沉淀
废液于锥形瓶中,滴加足量氯化钡溶液,生成白色沉淀 ;再加入足量稀盐酸,无明显变化。综合(1)(2)中实验可确定原废液中肯定含有的阴离子为
;再加入足量稀盐酸,无明显变化。综合(1)(2)中实验可确定原废液中肯定含有的阴离子为(3)综上实验,溶液中一定不存在的离子有

 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如下。

回答下列问题:
(1)写出N原子的结构示意图_______ ;物质A的结构式_______ 。
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(4)实验室中,检验溶液中含有NH 的操作方法是
的操作方法是_______ 。
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式_______ ,当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为_______ mol。

回答下列问题:
(1)写出N原子的结构示意图
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(4)实验室中,检验溶液中含有NH
 的操作方法是
的操作方法是(5)物质B为红棕色气体,写出该物质与水反应的离子方程式
您最近一年使用:0次
【推荐2】某混合物的溶液中可能含有以下离子中的若干种:K+、 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、 、
、 。同学甲取三份等体积溶液进行如下三组实验:
。同学甲取三份等体积溶液进行如下三组实验:
实验一:向一份溶液中加入AgNO3溶液,有白色沉淀产生;
实验二:向另一份溶液中加入足量NaOH溶液后加热,有刺激性气味的气体产生;
实验三:向第三份溶液中加入足量BaCl2溶液,得到白色沉淀,经足量盐酸洗涤后,沉淀部分溶解。
试回答下列问题:
(1)同学乙根据三组实验结果,判断肯定存在的离子有___________ ,肯定不存在的离子有___________ ,可能存在的离子是___________ 。
(2)同学乙认为设计的三组实验中,实验___________ (填实验序号)有瑕疵,无法判断某阴离子是否存在。改进后操作与现象为:另取一份原溶液,加入___________ ,证明该阴离子存在。同时同学乙还提出应补充一个实验,来完善对溶液中可能存在的阳离子的判断。补充的实验名称是___________ 。使用酒精灯完成实验,现象是___________ 时证明该阳离子存在。
 、Cl-、Ca2+、Ba2+、
、Cl-、Ca2+、Ba2+、 、
、 。同学甲取三份等体积溶液进行如下三组实验:
。同学甲取三份等体积溶液进行如下三组实验:实验一:向一份溶液中加入AgNO3溶液,有白色沉淀产生;
实验二:向另一份溶液中加入足量NaOH溶液后加热,有刺激性气味的气体产生;
实验三:向第三份溶液中加入足量BaCl2溶液,得到白色沉淀,经足量盐酸洗涤后,沉淀部分溶解。
试回答下列问题:
(1)同学乙根据三组实验结果,判断肯定存在的离子有
(2)同学乙认为设计的三组实验中,实验
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】中学化学中几种常见物质的转化关系如下图所示:
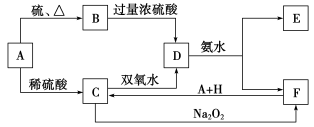
将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:___________________________ 。
(2)写出C的酸性溶液与双氧水反应的离子方程式:__________________________________ 。
(3)写出鉴定E中阳离子的实验方法和现象:_______________________________________ 。
(4)有学生利用FeCl3溶液制取FeCl3·6H2O晶体,主要操作包括:滴入过量盐酸,_________ 、冷却结晶、过滤。过滤操作除了漏斗、烧杯,还需要的玻璃仪器为_______________________ 。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,反应的离子方程式为____________________________ 。

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:
(2)写出C的酸性溶液与双氧水反应的离子方程式:
(3)写出鉴定E中阳离子的实验方法和现象:
(4)有学生利用FeCl3溶液制取FeCl3·6H2O晶体,主要操作包括:滴入过量盐酸,
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E五瓶透明溶液分别是 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种。已知:①A与D反应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
溶液中的一种。已知:①A与D反应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
(1)C的化学式为___________ ,E的名称为___________ ,B与D反应的离子方程式为___________ 。
(2)向一定量的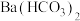 溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为___________ ,沉淀完全后,继续滴加C溶液,此时发生反应的离子方程式为___________ 。
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液中的一种。已知:①A与D反应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:
溶液中的一种。已知:①A与D反应有气体生成,②A与E反应有沉淀生成,③B与E反应有沉淀生成,④B与C反应有沉淀生成,⑤C与D反应有气体生成,⑥在②和③的反应中生成的沉淀是同一种物质。请回答下列问题:(1)C的化学式为
(2)向一定量的
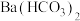 溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
溶液中逐滴加入C溶液,直至不再生成沉淀,该过程中发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】ZnO在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿[主要成分为ZnCO3,还含有Cd(II)、Fe(II)、Mn[(II)等杂质]制备。工艺如图所示:

已知:①相关金属离子[c(Mn+ )=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下表:
②“溶浸”后的溶液中金属离子主要有: Zn2+、 Fe2+、 Cd2+、 Mn2+。
③弱酸性溶液中KMnO4能将Mn2+氧化生成MnO2。
回答下列问题:
(1)“溶浸”过程中,提高浸出率的措施有___________ 。(写一条即可)
(2)“调pH”是将“溶浸”后的溶液调节至弱酸性(pH约为5),若pH过低,对除杂的影响是___________ 。
(3)加KMnO4“氧化除杂”发生反应的离子方程式分别是2MnO +3Mn2++2H2O=5MnO2↓+4H+和
+3Mn2++2H2O=5MnO2↓+4H+和___________ 。
(4)“还原除杂”中镉置换率与 的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为___________ kg。

(5)“沉锌”生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,写出加入Na2CO3溶液沉锌的化学方程式___________ 。形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是___________ 。

已知:①相关金属离子[c(Mn+ )=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ | Mn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 | 8.1 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 | 10.1 |
③弱酸性溶液中KMnO4能将Mn2+氧化生成MnO2。
回答下列问题:
(1)“溶浸”过程中,提高浸出率的措施有
(2)“调pH”是将“溶浸”后的溶液调节至弱酸性(pH约为5),若pH过低,对除杂的影响是
(3)加KMnO4“氧化除杂”发生反应的离子方程式分别是2MnO
 +3Mn2++2H2O=5MnO2↓+4H+和
+3Mn2++2H2O=5MnO2↓+4H+和(4)“还原除杂”中镉置换率与
 的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
(5)“沉锌”生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,写出加入Na2CO3溶液沉锌的化学方程式
您最近一年使用:0次
【推荐3】有一包粉末可能含有K+、Fe3+、Al3+、Cl-、SO42-、CO32-中的若干种,现进行以下实验:
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后滤液中 滴入硝酸酸化的AgNO3溶液,有白色沉淀生成;
③取②中有色沉淀加入足量稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,判断粉末中一定含有的离子是_______ , 肯定没有的离子是_____ 不能确定是否含有的离子是___________ ,通过_________ 来进一步确定该离子。
(2)写出②中生成有色沉淀反应的离子方程式:______________________ 。
①取少量固体,加入稀硝酸搅拌,固体全部溶解,没有气体放出;
②向①溶液中加入一定量Ba(OH)2溶液,生成有色沉淀,过滤后滤液中 滴入硝酸酸化的AgNO3溶液,有白色沉淀生成;
③取②中有色沉淀加入足量稀盐酸后,沉淀全部溶解;
④重新取少量固体加入适量蒸馏水搅拌后,固体全部溶解,得到澄清溶液;
⑤向④的溶液中加入氨水使溶液呈碱性,有沉淀生成,过滤,往得到沉淀中加入过量的NaOH溶液,沉淀减少。
(1)根据上述实验,判断粉末中一定含有的离子是
(2)写出②中生成有色沉淀反应的离子方程式:
您最近一年使用:0次



