ZnO在化学工业中主要用作橡胶和颜料的添加剂,医药上用于制软膏、橡皮膏等。工业上可由菱锌矿[主要成分为ZnCO3,还含有Cd(II)、Fe(II)、Mn[(II)等杂质]制备。工艺如图所示:

已知:①相关金属离子[c(Mn+ )=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下表:
②“溶浸”后的溶液中金属离子主要有: Zn2+、 Fe2+、 Cd2+、 Mn2+。
③弱酸性溶液中KMnO4能将Mn2+氧化生成MnO2。
回答下列问题:
(1)“溶浸”过程中,提高浸出率的措施有___________ 。(写一条即可)
(2)“调pH”是将“溶浸”后的溶液调节至弱酸性(pH约为5),若pH过低,对除杂的影响是___________ 。
(3)加KMnO4“氧化除杂”发生反应的离子方程式分别是2MnO +3Mn2++2H2O=5MnO2↓+4H+和
+3Mn2++2H2O=5MnO2↓+4H+和___________ 。
(4)“还原除杂”中镉置换率与 的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为___________ kg。

(5)“沉锌”生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,写出加入Na2CO3溶液沉锌的化学方程式___________ 。形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是___________ 。

已知:①相关金属离子[c(Mn+ )=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下表:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ | Mn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 | 8.1 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 | 10.1 |
③弱酸性溶液中KMnO4能将Mn2+氧化生成MnO2。
回答下列问题:
(1)“溶浸”过程中,提高浸出率的措施有
(2)“调pH”是将“溶浸”后的溶液调节至弱酸性(pH约为5),若pH过低,对除杂的影响是
(3)加KMnO4“氧化除杂”发生反应的离子方程式分别是2MnO
 +3Mn2++2H2O=5MnO2↓+4H+和
+3Mn2++2H2O=5MnO2↓+4H+和(4)“还原除杂”中镉置换率与
 的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
的关系如图所示,其中Zn的理论用量以溶液中Cd2+的量为依据。若需置换出112.0kgCd,且使镉置换率达到98%,实际加入的Zn应为
(5)“沉锌”生成碱式碳酸锌[ZnCO3·2Zn(OH)2·2H2O]沉淀,写出加入Na2CO3溶液沉锌的化学方程式
更新时间:2023-10-28 09:48:34
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组分组通过实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(1)实验小组1:向1mL0.1mol/LFeSO4溶液中加入1mL0. lmol/LAgNO3溶液,开始时,溶液无明显变化,几分钟后迅速出现大量灰黑色沉淀,反应过程中温度几乎无变化。测得溶液中Ag浓度随时间的变化如图1所示。
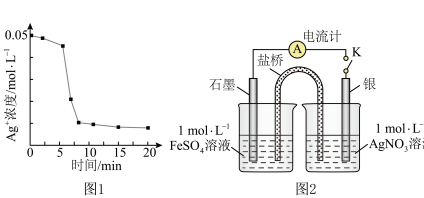
几分钟后迅速出现灰黑色沉淀的可能原因是_____________________ 。20min后取上层清液,滴加K3[Fe(CN)6]溶液,产生蓝色沉淀,说明溶液中含有_____ 。
(2)实验小组2:采用图2电化学验装置从平衡移动角度进行验证。闭合K,电流表指针发生偏转,一段时间后指针归零,证明该电池工作时能产生Fe3+操作及现象__________________ 。指针归零后再向左侧烧杯中加入较浓的Fe2(SO4)3溶液,指针变化为__________ ,综合实验Ⅰ和实验Ⅱ,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(3)实验小组3:向硝酸酸化的0.05mol/L硝酸银溶液(pH=2)中加入过量铁粉,发生反应“Fe+2Ag+=Fe2++2Ag”,静置后取上层清液,滴加KSCN溶液,溶液变红,同时发现有白色沉淀生成,说明溶液中存在________ (填离子符号) ;随静置时间延长,产生白色沉淀的量越来越少,溶液红色先变深后变浅,请结合离子方程式解释实验现象产生的原因___________________ (反应过程中忽略NO;和空气中氧气的氧化作用;查资料知Ag+与SCN-生成白色沉淀AgSCN)。
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(1)实验小组1:向1mL0.1mol/LFeSO4溶液中加入1mL0. lmol/LAgNO3溶液,开始时,溶液无明显变化,几分钟后迅速出现大量灰黑色沉淀,反应过程中温度几乎无变化。测得溶液中Ag浓度随时间的变化如图1所示。

几分钟后迅速出现灰黑色沉淀的可能原因是
(2)实验小组2:采用图2电化学验装置从平衡移动角度进行验证。闭合K,电流表指针发生偏转,一段时间后指针归零,证明该电池工作时能产生Fe3+操作及现象
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(3)实验小组3:向硝酸酸化的0.05mol/L硝酸银溶液(pH=2)中加入过量铁粉,发生反应“Fe+2Ag+=Fe2++2Ag”,静置后取上层清液,滴加KSCN溶液,溶液变红,同时发现有白色沉淀生成,说明溶液中存在
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气是一种重要的化工原料,下图为实验室制取氯气的装置。
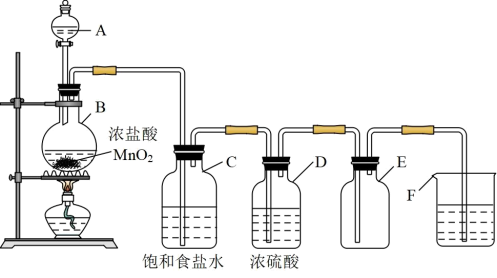
请回答下列问题:
(1)仪器E中收集的Cl2颜色是_______ ;
(2)仪器A的名称是_______ ;
(3)烧瓶中加热时发生反应的化学方程式为_______ 。
(4)仪器C中的饱和食盐水可以除去Cl2中混有的杂质气体是_______ (填化学式)。
(5)自来水厂使用ClO2给自来水进行消毒,ClO2中氯元素的化合价是_______ 。
(6)在新冠疫情防控期间,公共场所要求勤通风勤消毒,其中84消毒液经常用于公共场所消毒,制取84消毒液发生化学反应的离子方程式是_______ 。
(7)实验室检验氯气的方法是_______ 。

请回答下列问题:
(1)仪器E中收集的Cl2颜色是
(2)仪器A的名称是
(3)烧瓶中加热时发生反应的化学方程式为
(4)仪器C中的饱和食盐水可以除去Cl2中混有的杂质气体是
(5)自来水厂使用ClO2给自来水进行消毒,ClO2中氯元素的化合价是
(6)在新冠疫情防控期间,公共场所要求勤通风勤消毒,其中84消毒液经常用于公共场所消毒,制取84消毒液发生化学反应的离子方程式是
(7)实验室检验氯气的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D均为中学化学中的常见物质,它们有如图所示转化关系。A是一种常见金属,它可以与氢氧化钠溶液反应放出氢气。回答下列问题:

(1)写出C的化学式:_______________ 。
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:_____________________________ 。
(3)写出D→B的化学方程式:__________________________________ 。
(4)写出A和NaOH溶液反应的离子方程式:___________________________________ 。

(1)写出C的化学式:
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:
(3)写出D→B的化学方程式:
(4)写出A和NaOH溶液反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有一瓶澄清的溶液,其中可能含有 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、
、 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:
①用pH试纸检测,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性
b.溶液中逐渐产生沉淀
c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验现象,回答下列问题。
(1)由①可以排除______ 的存在。
(2)由②可以证明________ 的存在;同时排除_______ 的存在;理由是__________________ 。
(3)由③可以证明_________ 的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:
c.______________________ ;d.______________________ 。
 、K+、Ba2+、Al3+、Fe3+、I-、
、K+、Ba2+、Al3+、Fe3+、I-、 、
、 、
、 、
、 。取该溶液进行以下实验:
。取该溶液进行以下实验:①用pH试纸检测,溶液呈强酸性。
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色。
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性
b.溶液中逐渐产生沉淀
c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验现象,回答下列问题。
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
c.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂,常见制备方法如下。
(1)氯酸钾氧化法:化学反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KC1+3C12,每生成3mol KH(IO3)2,反应中转移的电子数为______ ,向反应后溶液中加______ 溶液得到KIO3。
(2)一种由含碘废水制取碘酸钾的工艺如图:
①进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤液中可通过滴加______ 盐溶液来检验其是否已洗涤干净。
②“制FeI2”时,发生反应的化学方程式为______ 。
③在KIO3、KHSO3的酸性混合溶液中加入少量KI(催化剂)和淀粉,不停地搅拌,反应机理为:第一步IO3-+5I-+6H+=3I2+3H2O 第二步反应的离子方程式为______ 。
当反应进行到1.5min时,溶液突然变为蓝色,随之又很快消失,则第______ 步反应速率快。
④改变反应温度,重复上述实验,得到温度(T)与溶液变蓝所需时间(t)的关系如图所示(超过50℃后溶液不会再变蓝)。根据图象,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:_________ 。
(3)山东省已下调食用盐碘含量标准每千克盐含碘25毫克(波动范围为18~33mg•kg-1)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL 6.000×10-4mol•L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-。计算该食盐试样中碘元素的含量______ mg•kg-1。
(1)氯酸钾氧化法:化学反应方程式为:6I2+11KClO3+3H2O=6KH(IO3)2+5KC1+3C12,每生成3mol KH(IO3)2,反应中转移的电子数为
(2)一种由含碘废水制取碘酸钾的工艺如图:

①进行“过滤1”时,需同时对CuI沉淀进行洗涤。在洗涤液中可通过滴加
②“制FeI2”时,发生反应的化学方程式为
③在KIO3、KHSO3的酸性混合溶液中加入少量KI(催化剂)和淀粉,不停地搅拌,反应机理为:第一步IO3-+5I-+6H+=3I2+3H2O 第二步反应的离子方程式为
当反应进行到1.5min时,溶液突然变为蓝色,随之又很快消失,则第
④改变反应温度,重复上述实验,得到温度(T)与溶液变蓝所需时间(t)的关系如图所示(超过50℃后溶液不会再变蓝)。根据图象,请你分析温度低于50℃时,溶液变蓝所需时间与反应温度的关系:

(3)山东省已下调食用盐碘含量标准每千克盐含碘25毫克(波动范围为18~33mg•kg-1)。测定食盐试样中碘元素含量的步骤如下:称取4.000g市售食盐加入锥形瓶中,依次加入适量的水、稍过量KI及稀硫酸;充分反应后,再加入12.00mL 6.000×10-4mol•L-1Na2S2O3溶液,与生成的碘恰好完全反应。有关反应原理为:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O;I2+2S2O32-=2I-+S4O62-。计算该食盐试样中碘元素的含量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测的结果如表所示,请回答:
(1)三次检测结果中第_______ 次检测结果不正确。
(2)在检测时,为了确定溶液中是否存在 、
、 和
和 (提示:
(提示: 微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的
微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的_____ (填化学式)溶液,其目的是检验 并将其除去﹔第二步加入过量的
并将其除去﹔第二步加入过量的 溶液,其目的是
溶液,其目的是______ ;第三步过滤,再向滤液中加入___ (填化学式)溶液,发生反应的离子方程式为___ 。
溶液中检测出的物质 | |
第一次 |
|
第二次 |
|
第三次 |
|
(1)三次检测结果中第
(2)在检测时,为了确定溶液中是否存在
 、
、 和
和 (提示:
(提示: 微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的
微溶于水),该小组进行了如下操作:第一步向溶液中滴加过量的 并将其除去﹔第二步加入过量的
并将其除去﹔第二步加入过量的 溶液,其目的是
溶液,其目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】利用 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
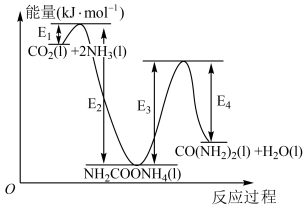
①反应物液氨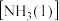 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在___________ (填作用力名称)。
②写出在该条件下由 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:___________ 。
(2)近年研究发现,电催化 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
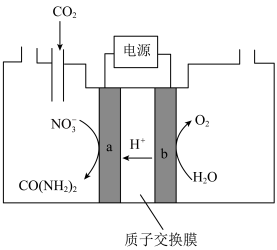
①电解过程中生成尿素的电极反应式为___________ 。
②目前以 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到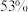 的法拉第效率
的法拉第效率 。已知:
。已知: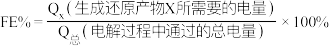 ,其中,
,其中,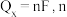 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下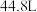 的
的 ,可获得尿素的质量为
,可获得尿素的质量为___________ 。(尿素的相对分子质量:60)
(3)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是___________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
①反应物液氨
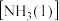 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到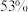 的法拉第效率
的法拉第效率 。已知:
。已知: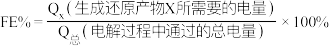 ,其中,
,其中,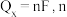 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下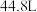 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某炼锌厂烟道灰含锌废料的主要成分是ZnO,还含有少量CuO、Fe2O3和 用其制备
用其制备 的流程图如图,请回答下列问题:
的流程图如图,请回答下列问题:
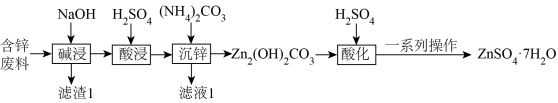
已知:ZnO为两性氧化物,能与NaOH溶液反应生成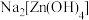
(1)“碱浸”时,加快碱浸速率的措施有_____ (写一种即可);分离出“滤渣1”的操作名称为_____ ;“滤渣1”的主要成分为CuO、_____ (填化学式)。
(2)ZnO在“碱浸”时发生反应的离子方程式为_____ ;“酸浸”时,如果加入的硫酸不足,可能生成某种不溶物,该不溶物为_____ (填化学式)。
(3)“沉锌”后洗涤获得的 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_____ 。
(4)若含锌废料中,ZnO的质量分数为81%,1t该含锌废料最后获得2.296tZnSO4·7H₂O,则锌的回收率为_____ %(锌的回收率=产物中锌元素的质量×100%)。
 用其制备
用其制备 的流程图如图,请回答下列问题:
的流程图如图,请回答下列问题: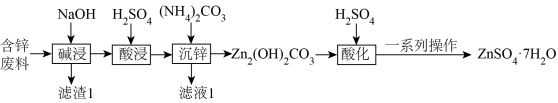
已知:ZnO为两性氧化物,能与NaOH溶液反应生成
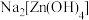
(1)“碱浸”时,加快碱浸速率的措施有
(2)ZnO在“碱浸”时发生反应的离子方程式为
(3)“沉锌”后洗涤获得的
 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(4)若含锌废料中,ZnO的质量分数为81%,1t该含锌废料最后获得2.296tZnSO4·7H₂O,则锌的回收率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐,为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:

(1)步骤①中洗去废铁屑表面的油污,可以选用的最佳试剂是_______ 。
a.热的稀硫酸 b.热水 c.热的碳酸钠溶液
(2)步骤②需要加热的目的是_______ 。
(3)步骤②温度保持80~95℃,采用的合适加热方式是_______ 。
(4)步骤③加入5%H2O2的目的是将Fe2+全部氧化为Fe3+,不引入杂质,请写出反应的离子方程式_______ 。
(5)准确称取48.2g硫酸铁铵纯样品,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、干燥、称量,得到46.6g沉淀,则[NH4Fe(SO4)2·xH2O]中x=_______ 。

(1)步骤①中洗去废铁屑表面的油污,可以选用的最佳试剂是
a.热的稀硫酸 b.热水 c.热的碳酸钠溶液
(2)步骤②需要加热的目的是
(3)步骤②温度保持80~95℃,采用的合适加热方式是
(4)步骤③加入5%H2O2的目的是将Fe2+全部氧化为Fe3+,不引入杂质,请写出反应的离子方程式
(5)准确称取48.2g硫酸铁铵纯样品,加入足量的BaCl2溶液,充分反应后,过滤、洗涤、干燥、称量,得到46.6g沉淀,则[NH4Fe(SO4)2·xH2O]中x=
您最近一年使用:0次

 、
、 、
、 、
、
 、
、 、
、


