A、B、C、D均为中学化学中的常见物质,它们有如图所示转化关系。A是一种常见金属,它可以与氢氧化钠溶液反应放出氢气。回答下列问题:

(1)写出C的化学式:_______________ 。
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:_____________________________ 。
(3)写出D→B的化学方程式:__________________________________ 。
(4)写出A和NaOH溶液反应的离子方程式:___________________________________ 。

(1)写出C的化学式:
(2)向B的溶液中逐滴加入NaOH溶液至过量的实验现象:
(3)写出D→B的化学方程式:
(4)写出A和NaOH溶液反应的离子方程式:
2021高二·陕西·学业考试 查看更多[2]
更新时间:2023-03-20 14:16:49
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫代硫酸钠( ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
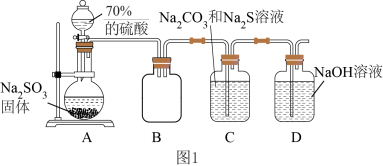
已知: 在酸性溶液中发生反应:
在酸性溶液中发生反应: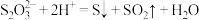
(1)实验室制备 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是_______ 。图1装置B的作用是________ 。
(2)图1装置C中发生反应生成 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是_____ 。
(3)某同学用图2中装置验证装置C中生成了 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是_______ 。
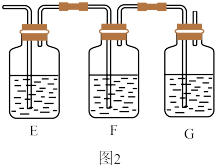
A.品红、 溶液、澄清石灰水
溶液、澄清石灰水
B.酸性 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
C. 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水
(4)从装置C中所得溶液经过结晶等操作获得的 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体,________ ,离心沉降,过滤,_______ ,若有白色沉淀生成,则原晶体中含有 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
 ),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少
),常用作纸浆漂白的脱氯剂。实验室用图1装置制备少 。
。
已知:
 在酸性溶液中发生反应:
在酸性溶液中发生反应: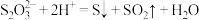
(1)实验室制备
 气体也可以用浓硫酸与Cu反应,该反应的化学方程式是
气体也可以用浓硫酸与Cu反应,该反应的化学方程式是(2)图1装置C中发生反应生成
 的同时放出
的同时放出 ,该反应的离子方程式是
,该反应的离子方程式是(3)某同学用图2中装置验证装置C中生成了
 。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
。将装置C与装置E连接,使气体依次通过装置E、F、G,则装置E、F、G中依次盛放的溶液的组合是
A.品红、
 溶液、澄清石灰水
溶液、澄清石灰水 B.酸性
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水C.
 溶液、品红、澄清石灰水
溶液、品红、澄清石灰水(4)从装置C中所得溶液经过结晶等操作获得的
 晶体中含有少量的
晶体中含有少量的 ,试检验其中含有
,试检验其中含有 的方法是:取少量固体,
的方法是:取少量固体, 。(实验中可选用的试剂:稀盐酸、稀硫酸、
。(实验中可选用的试剂:稀盐酸、稀硫酸、 溶液)
溶液)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】为了将氯化钠和氯化钙的混合物分离,并测定其中氯化钠的质量分数,兴趣小组最初设计了如下方案并进行实验:
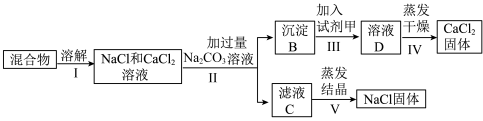
根据流程图回答:
(1)生成沉淀B的离子方程式是___________ 。
(2)步骤Ⅱ加入 溶液后,分离出沉淀B的实验操作名称是
溶液后,分离出沉淀B的实验操作名称是___________ ,该实验操作需要的玻璃仪器是___________ 。
(3)根据以上方案得到NaCl固体测定含有杂质,除去该杂质的试剂可以是___________ 。发生反应的离子方程式是___________ 。
(4)为测定原混合物中氯化钠的质量分数,同学们分别称量混合物A的总质量 和干燥的沉淀B固体的质量
和干燥的沉淀B固体的质量 ,则原混合物中NaCl的质量分数是
,则原混合物中NaCl的质量分数是___________ 。

根据流程图回答:
(1)生成沉淀B的离子方程式是
(2)步骤Ⅱ加入
 溶液后,分离出沉淀B的实验操作名称是
溶液后,分离出沉淀B的实验操作名称是(3)根据以上方案得到NaCl固体测定含有杂质,除去该杂质的试剂可以是
(4)为测定原混合物中氯化钠的质量分数,同学们分别称量混合物A的总质量
 和干燥的沉淀B固体的质量
和干燥的沉淀B固体的质量 ,则原混合物中NaCl的质量分数是
,则原混合物中NaCl的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种利用废旧三元锂离子电池正极材料(主要成分为LiCo1-x-yMnxNiyO2,还含有铝箔、炭黑、有机粘合剂等)综合回收钴、锰、镍、锂的工艺流程如图所示:
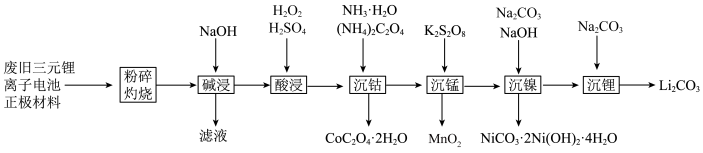
回答下列问题:
(1)Mn位于元素周期表中___________ 区,基态镍原子的核外电子排布式为___________ 。
(2)“粉碎灼烧”时,将废旧电池正极材料充分粉碎有利于加快灼烧的速率,其原理是___________ 。
(3)“碱浸”时主要反应的化学方程式为___________ 。
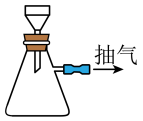
(4)“酸浸”后需要过滤,与普通过滤相比,使用如图所示装置进行过滤的优点是___________ 。
(5)“沉锰”步骤中,溶液中含Mn2+,加入K2S2O8溶液后,溶液先变为紫红色,写出该反应的离子方程式:___________ 。一段时间后溶液紫红色又褪去,有黑色沉淀生成。
(6)LiCo1-x-yMnxNiyO2的基本结构单元如图所示,则x=___________ ,y=___________ 。


回答下列问题:
(1)Mn位于元素周期表中
(2)“粉碎灼烧”时,将废旧电池正极材料充分粉碎有利于加快灼烧的速率,其原理是
(3)“碱浸”时主要反应的化学方程式为
(4)“酸浸”后需要过滤,与普通过滤相比,使用如图所示装置进行过滤的优点是

(5)“沉锰”步骤中,溶液中含Mn2+,加入K2S2O8溶液后,溶液先变为紫红色,写出该反应的离子方程式:
(6)LiCo1-x-yMnxNiyO2的基本结构单元如图所示,则x=

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】请回答:
已知:甲+X→乙+Y
(1)若甲、乙、X均是化合物,Y是单质,则Y可能是___ 。(填化学式,下同)
(2)若酸性X>Y,且甲过量,Y是白色浑浊,则Y是__________ ,乙是__________ 。
(3)若甲、乙是金属单质,X为固体,则反应的化学方程式是_______________ 。
(4)甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y是化合物。X溶液呈淡绿色,Y的溶液能使KSCN溶液变红。
①将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体丙,证明丙的操作、现象及结论是___________________________________________________ 。
②单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:______ 。(用化学式表示)
③当X与甲1:1充分反应的离子方程式:_________________________ 。
已知:甲+X→乙+Y
(1)若甲、乙、X均是化合物,Y是单质,则Y可能是
(2)若酸性X>Y,且甲过量,Y是白色浑浊,则Y是
(3)若甲、乙是金属单质,X为固体,则反应的化学方程式是
(4)甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体。X、Y是化合物。X溶液呈淡绿色,Y的溶液能使KSCN溶液变红。
①将Y的饱和溶液滴入沸水中,继续加热可得红褐色液体丙,证明丙的操作、现象及结论是
②单质甲、乙和Y溶液中的阳离子氧化性由强到弱的顺序为:
③当X与甲1:1充分反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】某合金X由常见的两种元素组成。为探究该合金X的元素组成和性质,设计并进行如下实验:
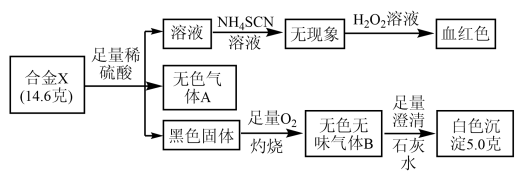
根据上述信息,回答下列问题:
(1)合金X的化学式为________ 。
(2)用离子方程式解释溶液中滴加H2O2后呈红色的原因:_______
(3)写出336 mL(标准状况)气体B通入100 mL 0.2 mol/L 的NaOH溶液中的化学反应方程式:_______

根据上述信息,回答下列问题:
(1)合金X的化学式为
(2)用离子方程式解释溶液中滴加H2O2后呈红色的原因:
(3)写出336 mL(标准状况)气体B通入100 mL 0.2 mol/L 的NaOH溶液中的化学反应方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图表示A〜E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质。试推出各物质的化学式,并写出B→C、C→D、D→E反应的化学方程式。
(1)写出B→C、C→D、D→E反应的化学方程式:
B→C:_______________ ;
C→D:_______________ ;
D→E:_______________ ;
(2)将3.9 gA投入到足量的水中充分反应,生成的气体在标准状况下的体积为_____ L,将反应后的溶液配成1000mL溶液,所得溶液的物质的避浓度为______________ 。

(1)写出B→C、C→D、D→E反应的化学方程式:
B→C:
C→D:
D→E:
(2)将3.9 gA投入到足量的水中充分反应,生成的气体在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题
(1)某无色稀溶液X中,可能含有下表所列离子中的某几种。
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂Y的体积(V)的关系如图所示。

①若Y是盐酸,则溶液中含有的金属阳离子是_________________________________ ,
ab段发生反应的总离子方程式为___________________________________
表中Oa段与Y溶液反应的离子的物质的量之比为__________ [要标明离子符号,如n(Na+)]。
②若Y是NaOH溶液,则bc段反应的离子方程式为______________________________
若不考虑离子的水解因素,忽略H+和OH-的影响,且溶液中只存在4种离子,则它们的离子个数比为___________________________________ [按阳离子在前,阴离子在后,高价在前,低价在后的顺序排列]。
(2)锡为第ⅣA族元素,锡的单质和化合物与某些物质的化学性质上有许多相似之处。已知锡元素具有如下性质:
Sn4++Sn=2Sn2+;
2Sn2++O2+4H+=2Sn4++2H2O;
2H++
 Sn(OH)2
Sn(OH)2 Sn2++2OH-。
Sn2++2OH-。
试回答:
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的离子方程式:______________________________________ ,
②将①中溶液蒸干后继续加热所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是(分子式)__________ 。
③若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2该碱是__________ 。
(1)某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 |  、 、 、 、 、Cl- 、Cl- |
| 阳离子 | Al3+、Cu2+、Mg2+、 、Na+ 、Na+ |

①若Y是盐酸,则溶液中含有的金属阳离子是
ab段发生反应的总离子方程式为
表中Oa段与Y溶液反应的离子的物质的量之比为
②若Y是NaOH溶液,则bc段反应的离子方程式为
若不考虑离子的水解因素,忽略H+和OH-的影响,且溶液中只存在4种离子,则它们的离子个数比为
(2)锡为第ⅣA族元素,锡的单质和化合物与某些物质的化学性质上有许多相似之处。已知锡元素具有如下性质:
Sn4++Sn=2Sn2+;
2Sn2++O2+4H+=2Sn4++2H2O;
2H++

 Sn(OH)2
Sn(OH)2 Sn2++2OH-。
Sn2++2OH-。试回答:
①锡溶于盐酸,再向反应后的溶液中通入氯气,有关反应类似于铁的相应变化,试写出有关反应的离子方程式:
②将①中溶液蒸干后继续加热所得固体,变化过程类似于FeCl3溶液相应的变化,则最后得到的固体物质是(分子式)
③若可用SnCl2溶液与过量的碱溶液反应的方法制Sn(OH)2该碱是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】某无色溶液中含有的金属阳离子为Mg2+、Al3+,向该溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的物质的量与加入NaOH的物质的量的关系如图所示。

(1)由此确定原溶液中一定还大量含有某阳离子,它可能是________ 。
(2)若溶质为MgCl2和Al2(SO4)3,则原溶液中铝离子的物质的量为______________ 。
(3)下列图像中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀的质量,用图像的序号或文字回答下列问题:

Ⅰ.表示向AlCl3溶液中逐渐滴加NaOH溶液的是______ ;
Ⅱ.表示向NaAlO2溶液中逐渐滴加稀盐酸的是________ ;
Ⅲ.表示向NaAlO2溶液中通入CO2的是________ ;
Ⅳ.③图____________ (填“能”或“不能”)代表向含NaOH的澄清石灰水中通入CO2。

(1)由此确定原溶液中一定还大量含有某阳离子,它可能是
(2)若溶质为MgCl2和Al2(SO4)3,则原溶液中铝离子的物质的量为
(3)下列图像中,横坐标表示加入试剂或通入气体的物质的量,纵坐标表示产生沉淀的质量,用图像的序号或文字回答下列问题:

Ⅰ.表示向AlCl3溶液中逐渐滴加NaOH溶液的是
Ⅱ.表示向NaAlO2溶液中逐渐滴加稀盐酸的是
Ⅲ.表示向NaAlO2溶液中通入CO2的是
Ⅳ.③图
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
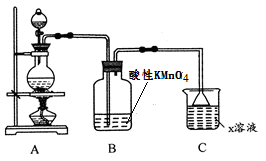
【推荐3】某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为_____________________ 。
(2)C装置的作用___________________ 。
(3)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是_______________ 。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为_______ 。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、Al2O3及不溶于强酸的SiO2)可制备Fe2O3。①用稀盐酸浸取炉渣,过滤;②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
a.除去Al3+的离子方程式是______________________________ 。
b.步骤②中滤液氧化的目的是_____________________________ 。
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为
(2)C装置的作用
(3)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、Al2O3及不溶于强酸的SiO2)可制备Fe2O3。①用稀盐酸浸取炉渣,过滤;②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
a.除去Al3+的离子方程式是
b.步骤②中滤液氧化的目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有甲、乙、丙、丁四种物质,乙、丁的焰色反应均为黄色。丙是一种强酸的酸式盐,将丙加入BaCl2溶液有不溶于盐酸的白色沉淀生成,丁晶体在干燥空气中容易逐渐失去结晶水变成白色粉末。对甲、乙、丙、丁进行下列实验,实验过程和记录如下图所示(无关物质已略去),请回答:

(1)将D溶液蒸干得到的固体是:____________ (写化学式)。
(2)C的结构式是______ 。
(3)写出D溶液与过量的C反应的离子方程式______________________________ 。
(4)电解戊的水溶液一段时间后,收集到的三种气体为无色气体B和两种单质气体,写出电解戊溶液的总方程式:_________________________ 。
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280 300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:
300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:___ 。

(1)将D溶液蒸干得到的固体是:
(2)C的结构式是
(3)写出D溶液与过量的C反应的离子方程式
(4)电解戊的水溶液一段时间后,收集到的三种气体为无色气体B和两种单质气体,写出电解戊溶液的总方程式:
(5)有人设想在适当大小的管道中填充一定量的丁的晶体(摩尔质量在280
 300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:
300之间),管道环绕在一个房子的周围,这样的房子白天晚上室内温度可保持相对恒定,请简述其原理:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝是一种应用广泛的金属,工业上用铝土矿提纯出 ,再和冰晶石(Na3AlF6)混合熔融电解制得铝单质。铝土矿的主要成分是
,再和冰晶石(Na3AlF6)混合熔融电解制得铝单质。铝土矿的主要成分是 ,此外还含有少量SiO2、Fe2O3等杂质。以铝土矿为原料用拜耳法生产
,此外还含有少量SiO2、Fe2O3等杂质。以铝土矿为原料用拜耳法生产 的流程如下图所示:
的流程如下图所示:
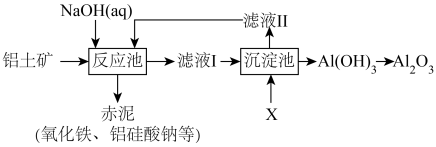
(1) 电解制Al的化学方程式是
电解制Al的化学方程式是__________ ,该反应属于______ 反应(选填“吸热”或“放热”),说明反应物的能量______ 生成物的量(选填“高于”、“等于”或“低于”)。AlCl3的熔点远低于 ,工业上不采用电解熔融AlCl3的方法制备铝的原因是
,工业上不采用电解熔融AlCl3的方法制备铝的原因是______________ 。
(2)反应池中 溶于NaOH的离子方程式是
溶于NaOH的离子方程式是__________ 。
(3)该生产过程中,需向沉淀池中加入X。
①X可为过量的的CO2,则滤液Ⅱ中主要的溶质是________ ,为了使滤液Ⅱ循环利用应补充的物质是______ 。
A.CaO B.HCl C.Na2CO3
②X也可为少量Al(OH)3晶种(晶种可加速沉淀的生成),其优点是___________ 。
 ,再和冰晶石(Na3AlF6)混合熔融电解制得铝单质。铝土矿的主要成分是
,再和冰晶石(Na3AlF6)混合熔融电解制得铝单质。铝土矿的主要成分是 ,此外还含有少量SiO2、Fe2O3等杂质。以铝土矿为原料用拜耳法生产
,此外还含有少量SiO2、Fe2O3等杂质。以铝土矿为原料用拜耳法生产 的流程如下图所示:
的流程如下图所示:
(1)
 电解制Al的化学方程式是
电解制Al的化学方程式是 ,工业上不采用电解熔融AlCl3的方法制备铝的原因是
,工业上不采用电解熔融AlCl3的方法制备铝的原因是(2)反应池中
 溶于NaOH的离子方程式是
溶于NaOH的离子方程式是(3)该生产过程中,需向沉淀池中加入X。
①X可为过量的的CO2,则滤液Ⅱ中主要的溶质是
A.CaO B.HCl C.Na2CO3
②X也可为少量Al(OH)3晶种(晶种可加速沉淀的生成),其优点是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
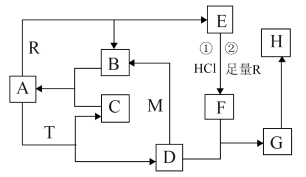
【推荐3】A常温常压下为无色液体,B、C是无色无味的气体,M、R是两种常见的金属,且M是地壳中含量最多的金属元素的单质,T是淡黄色固体,E是具有磁性的黑色晶体,G和H组成元素相同。各物质在一定条件下有如下转化关系。___________ 。
(2)D和M在溶液中反应生成B的离子反应方程式为___________ 。
(3)T和F反应只生成C、H和一种盐,其化学反应方程式为___________ 。
(4)若向E和R的混合物中加入100mL1mol/L的盐酸,恰好使混合物完全溶解,生成FeCl2并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为___________ g。
(2)D和M在溶液中反应生成B的离子反应方程式为
(3)T和F反应只生成C、H和一种盐,其化学反应方程式为
(4)若向E和R的混合物中加入100mL1mol/L的盐酸,恰好使混合物完全溶解,生成FeCl2并放出448mL(标准状况)气体。若用足量的CO在高温下还原相同质量的上述混合物,得到的固体质量为
您最近一年使用:0次



