阅读下列科普短文并填空:
海洋约占地球表面积的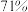 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和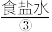 用以生产
用以生产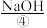 、
、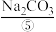 、
、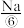 、
、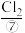 、
、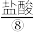 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、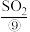 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
(1)上述标有序号的物质中属于电解质的是___________ (填序号,下同);属于非电解质的是___________ ;能导电的物质是___________ 。
(2)写出⑤溶于水的电离方程式:___________ 。将少量的⑤溶于装有 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是___________ ,写出对应反应的离子方程式:______ ,______ 。
(3)海水提溴的过程中涉及的反应有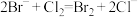 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为___________ 。
海洋约占地球表面积的
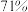 ,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如
,其中水资源和其他化学资源具有巨大的开发潜力。海水中含有多种盐类,如 、
、 等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和
等。目前,通过海水晒盐可制得食盐晶体和苦卤,食盐精制后可制成饱和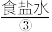 用以生产
用以生产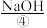 、
、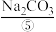 、
、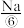 、
、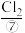 、
、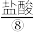 等,苦卤经过氯气氧化,热空气吹出、
等,苦卤经过氯气氧化,热空气吹出、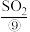 吸收等一系列操作可获得
吸收等一系列操作可获得 。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。
。海水淡化与化工生产、能源开发等相结合已经成为海水综合利用的重要方向。(1)上述标有序号的物质中属于电解质的是
(2)写出⑤溶于水的电离方程式:
 蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是
蒸馏水的烧杯中后,逐滴加入⑧观察到刚开始并没有出现气泡,一段时间后出现气泡,则出现该现象的原因是(3)海水提溴的过程中涉及的反应有
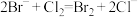 ,
, ,根据上述反应可判断
,根据上述反应可判断 、
、 、
、 的还原性由强到弱的顺序为
的还原性由强到弱的顺序为
更新时间:2021-10-17 21:37:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)在下列物质中,可以导电的是_______ (填序号,下同),是电解质的有_______ 。
① 晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
(2)某气体在标准状况下的密度为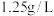 ,则14g该气体所含有的物质的量为
,则14g该气体所含有的物质的量为_______ 。
(3)从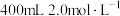 的
的 溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为_______  。
。
(4)已知 与
与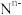 具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为_______ 。
(1)在下列物质中,可以导电的是
①
 晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨
晶体 ②熔融的氢氧化钠 ③Cu ④酒精 ⑤液氨(2)某气体在标准状况下的密度为
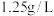 ,则14g该气体所含有的物质的量为
,则14g该气体所含有的物质的量为(3)从
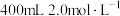 的
的 溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为 。
。(4)已知
 与
与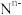 具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列填空:
(1)画出 O2﹣结构示意图:_____ ,某种核素质量数 37,中子数 20,其原子符号:_____
(2)现有以下物质:①NaCl溶液;②液态HCl;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;
⑥液氨;⑦冰醋酸;⑧石墨.
其中:属于电解质且能导电的是_____
(3)氰(CN)2 的化学性质和卤素(X2,如 Cl2)很相似,化学上称为拟卤素.试写出(CN)2与水反应的化学方程式:_____
(4)钠是一种非常活泼的金属,能与水反应,若把一小块钠投入 CuSO4 溶液中,会产生蓝色沉淀,试写出 该反应的化学方程式_____ .
(1)画出 O2﹣结构示意图:
(2)现有以下物质:①NaCl溶液;②液态HCl;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;
⑥液氨;⑦冰醋酸;⑧石墨.
其中:属于电解质且能导电的是
(3)氰(CN)2 的化学性质和卤素(X2,如 Cl2)很相似,化学上称为拟卤素.试写出(CN)2与水反应的化学方程式:
(4)钠是一种非常活泼的金属,能与水反应,若把一小块钠投入 CuSO4 溶液中,会产生蓝色沉淀,试写出 该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有下列物质:①生石灰 ② 固体 ③浓
固体 ③浓 ④单质铁 ⑤
④单质铁 ⑤ ⑥熔融
⑥熔融 ⑦石墨⑧蔗糖晶体 ⑨
⑦石墨⑧蔗糖晶体 ⑨ 固体 ⑩
固体 ⑩ 固体。请填空:
固体。请填空:
(1)上述状态下可导电的物质是_______ (填标号,下同),属于电解质的是___________ 。
(2)上述物质中属于碱性氧化物的是______ (填化学式,下同),属于酸性氧化物的是_______ 。
(3)⑥的电离方程式为___________ ,⑩溶于水时的电离方程式为___________ 。
(4)②的水溶液与④反应的离子方程式为___________ 。
 固体 ③浓
固体 ③浓 ④单质铁 ⑤
④单质铁 ⑤ ⑥熔融
⑥熔融 ⑦石墨⑧蔗糖晶体 ⑨
⑦石墨⑧蔗糖晶体 ⑨ 固体 ⑩
固体 ⑩ 固体。请填空:
固体。请填空:(1)上述状态下可导电的物质是
(2)上述物质中属于碱性氧化物的是
(3)⑥的电离方程式为
(4)②的水溶液与④反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列十种物质: ①蔗糖②熔融 NaCl③石墨④铜丝⑤NaOH固体⑥金刚石⑦NaHSO4固体⑧K2O 固体⑨液态H2SO4⑩饱和 FeCl3溶液
(1)上述物质中可导电的是__________ (填序号,下同); 属于电解质的是__________ 。
(2)上述物质中互为同素异形体的是______________________ 。
(3)NaHSO4是一种酸式盐,在水溶液中的电离方程式为______________________ ;NaHSO4与 Ba(OH)2溶液混合时溶液呈中性,该反应的离子方程式为______________________ 。
(1)上述物质中可导电的是
(2)上述物质中互为同素异形体的是
(3)NaHSO4是一种酸式盐,在水溶液中的电离方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.以下12种物质为中学化学中常见的物质:①Cu;②NaCl;③NaHSO4;④SO3;⑤H2SO4;⑥C2H5OH;⑦CaCO3;⑧BaSO4;⑨Cu(OH)2;⑩Fe(OH)3;⑪NaOH;⑫NH3·H2O。请按下列分类标准回答问题。
(1)属于电解质的是____ (填序号,下同)。
(2)能电离出H+的是____ ,属于酸的是____ 。
(3)属于碱的是____ ,其中属于难溶性碱的是____ 。
(4)属于难溶性盐的是____ 。
Ⅱ.写出下列物质在水溶液中的电离方程式:
(5)HCl:____ ;
(6)Ca(OH)2:____ ;
(7)NH4NO3:_____ ;
(8)H2SO4:____ 。
(1)属于电解质的是
(2)能电离出H+的是
(3)属于碱的是
(4)属于难溶性盐的是
Ⅱ.写出下列物质在水溶液中的电离方程式:
(5)HCl:
(6)Ca(OH)2:
(7)NH4NO3:
(8)H2SO4:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】写出下列反应的化学反应方程式及离子反应方程式:
(1)实验室制二氧化碳________
(2)氧化铁与硝酸________
(3)氯化铁溶液与氢氧化钠溶液混合________
(4)二氧化碳通入碳酸钠溶液________
(1)实验室制二氧化碳
(2)氧化铁与硝酸
(3)氯化铁溶液与氢氧化钠溶液混合
(4)二氧化碳通入碳酸钠溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业废水中的六价铬[Cr(VI)]常采用还原沉淀法和微生物法等方法进行处理。
(1)还原沉淀法:使用Na2SO3将Cr(Ⅵ)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(Ⅵ)具有很强的氧化能力,SO 将Cr2O
将Cr2O 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为___ 。
②其他条件相同,用Na2SO3处理不同初始pH的含Cr(Ⅵ)废水相同时间,当pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是____ 。
(2)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(Ⅵ)的去除率很低的原因是_________ 。

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,________________ 。

(1)还原沉淀法:使用Na2SO3将Cr(Ⅵ)还原为Cr3+,再将Cr3+转化为沉淀除去。
①酸性条件下Cr(Ⅵ)具有很强的氧化能力,SO
 将Cr2O
将Cr2O 还原为Cr3+的离子方程式为
还原为Cr3+的离子方程式为②其他条件相同,用Na2SO3处理不同初始pH的含Cr(Ⅵ)废水相同时间,当pH<2时,Cr(Ⅵ)的去除率随pH降低而降低的原因是
(2)微生物法:
①用硫酸盐还原菌(SRB)处理含Cr(Ⅵ)废水时,Cr(VI)去除率随温度的变化如图所示。55℃时,Cr(Ⅵ)的去除率很低的原因是

②水体中,Fe合金在SRB存在条件下腐蚀的机理如图所示。Fe腐蚀后生成FeS的过程可描述为:Fe失去电子转化为Fe2+,

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】二氧化氯( )具有强氧化性,是一种安全、无毒的绿色消毒剂,遇热水易分解,浓度大时易爆炸。回答下列问题:
)具有强氧化性,是一种安全、无毒的绿色消毒剂,遇热水易分解,浓度大时易爆炸。回答下列问题:
(1) 与热水反应得到
与热水反应得到 、
、 。该反应的氧化产物是一种不含氯元素的气体,其分子式为
。该反应的氧化产物是一种不含氯元素的气体,其分子式为___________ 。
(2)将1
 通入
通入 和
和 的混合溶液中,充分反应后有
的混合溶液中,充分反应后有 生成,反应中共转移5
生成,反应中共转移5 电子,则发生反应的离子方程式为
电子,则发生反应的离子方程式为___________ 。
(3) 可通过下列反应制备:
可通过下列反应制备:
①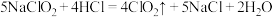
②
用上述两种方法制备等质量的 转移电子数之比为
转移电子数之比为___________ 。现在科学家研究出用草酸( )在酸性条件下还原
)在酸性条件下还原 的制备方法。已知
的制备方法。已知 被氧化生成
被氧化生成 。写出该制备方法的离子方程式:
。写出该制备方法的离子方程式:___________ 。该方法最突出的优点是___________ 。
(4)通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小。 和
和 在消毒时自身均被还原为
在消毒时自身均被还原为 ,则
,则 的消毒效率是
的消毒效率是 的
的___________ 倍(保留两位小数)。
 )具有强氧化性,是一种安全、无毒的绿色消毒剂,遇热水易分解,浓度大时易爆炸。回答下列问题:
)具有强氧化性,是一种安全、无毒的绿色消毒剂,遇热水易分解,浓度大时易爆炸。回答下列问题:(1)
 与热水反应得到
与热水反应得到 、
、 。该反应的氧化产物是一种不含氯元素的气体,其分子式为
。该反应的氧化产物是一种不含氯元素的气体,其分子式为(2)将1

 通入
通入 和
和 的混合溶液中,充分反应后有
的混合溶液中,充分反应后有 生成,反应中共转移5
生成,反应中共转移5 电子,则发生反应的离子方程式为
电子,则发生反应的离子方程式为(3)
 可通过下列反应制备:
可通过下列反应制备:①
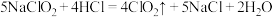
②

用上述两种方法制备等质量的
 转移电子数之比为
转移电子数之比为 )在酸性条件下还原
)在酸性条件下还原 的制备方法。已知
的制备方法。已知 被氧化生成
被氧化生成 。写出该制备方法的离子方程式:
。写出该制备方法的离子方程式:(4)通常用单位质量的消毒剂得到电子的多少来衡量消毒效率的大小。
 和
和 在消毒时自身均被还原为
在消毒时自身均被还原为 ,则
,则 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在工农业生产、日常生活中具有广泛用途。
(1)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断 Na2SeO3的作用是作___________ (填“氧化剂”或“还原剂”)
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO +3Cl-+5H2O。请注明该反应中电子转移的方向和数目
+3Cl-+5H2O。请注明该反应中电子转移的方向和数目___________ 。
(3)H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
①消除废液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O=X+NH3↑,则生成物X的化学式为___________ ,H2O2被称为“绿色氧化剂”的理由是___________ 。
②从H2O2氧元素的化合价可推测,H2O2既具有氧化性,又具有还原性。某实验小组同学设计实验探究H2O2在某强酸性反应体系中的性质。
实验Ⅰ:探究H2O2的氧化性。
向含5%H2O2的酸性溶液中滴加淀粉-KI溶液,溶液变蓝。写出该反应的离子方程式___________ 。
实验Ⅱ:探究H2O2的还原性。
向含5%H2O2的溶液中滴加酸性KMnO4溶液。已知反应物和生成物共有六种粒子:O2、MnO 、H2O、Mn2+、H2O2、H+。
、H2O、Mn2+、H2O2、H+。
实验Ⅱ的实验现象为a.___________ ;b.有气泡产生。
若该反应中H2O2只发生了如下过程:H2O2→O2↑,则该反应的离子方程式为___________ 。
(1)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体内的活性氧,由此推断 Na2SeO3的作用是作
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理。工业制备高铁酸钠有多种方法。其中一种方法的化学原理可用离子方程式表示为:3ClO-+2Fe3++10OH-=2FeO
 +3Cl-+5H2O。请注明该反应中电子转移的方向和数目
+3Cl-+5H2O。请注明该反应中电子转移的方向和数目(3)H2O2可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
①消除废液中的氰化物(如KCN),可经以下反应实现:KCN+H2O2+H2O=X+NH3↑,则生成物X的化学式为
②从H2O2氧元素的化合价可推测,H2O2既具有氧化性,又具有还原性。某实验小组同学设计实验探究H2O2在某强酸性反应体系中的性质。
实验Ⅰ:探究H2O2的氧化性。
向含5%H2O2的酸性溶液中滴加淀粉-KI溶液,溶液变蓝。写出该反应的离子方程式
实验Ⅱ:探究H2O2的还原性。
向含5%H2O2的溶液中滴加酸性KMnO4溶液。已知反应物和生成物共有六种粒子:O2、MnO
 、H2O、Mn2+、H2O2、H+。
、H2O、Mn2+、H2O2、H+。实验Ⅱ的实验现象为a.
若该反应中H2O2只发生了如下过程:H2O2→O2↑,则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是____________ 。
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为____________ 。
(3)根据上述反应可推知___________ 。
a.氧化性:H3AsO4>KBrO3
b.氧化性:KBrO3>H3AsO4
c.还原性:X>AsH3
d.还原性:AsH3>X
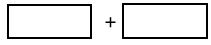
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目___________
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是
(2)已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
(3)根据上述反应可推知
a.氧化性:H3AsO4>KBrO3
b.氧化性:KBrO3>H3AsO4
c.还原性:X>AsH3
d.还原性:AsH3>X
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组学生根据氧化还原反应规律,从下列各组反应对比中,判断哪种粒子的氧化性最强,哪种粒子还原性最强。
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,___ 的还原性最强;在Cu2+、Fe2+、Ag+中,___ 的氧化性最强。
(2)铁钉在氯气中被锈蚀为棕褐色物质(FeCl3),而在盐酸中生成淡绿色溶液(FeCl2)。则在氯气分子(Cl2)、氯离子(Cl-)、氢离子(H+)中,_______ 具有氧化性,_______ 的氧化性最强。
(3)某反应体系有反应物和生成物共7种物质C、H2SO4、K2CrO4、K2SO4、CO2、Cr2(SO4)3和H2O。已知该反应中发生如下过程:C→CO2,则该反应的化学反应方程式为:_______
(1)铁钉浸入CuSO4溶液后,表面会附有红色物质;铜丝浸入AgNO3溶液后,表面会附有银白色物质。则在Cu、Fe、Ag中,
(2)铁钉在氯气中被锈蚀为棕褐色物质(FeCl3),而在盐酸中生成淡绿色溶液(FeCl2)。则在氯气分子(Cl2)、氯离子(Cl-)、氢离子(H+)中,
(3)某反应体系有反应物和生成物共7种物质C、H2SO4、K2CrO4、K2SO4、CO2、Cr2(SO4)3和H2O。已知该反应中发生如下过程:C→CO2,则该反应的化学反应方程式为:
您最近一年使用:0次



