Na、Fe、Al是中学化学常见的金属元素。回答下列问题:
(1)焰色反应的实验中,Na元素燃烧时的焰色为___________ 色,观察K元素燃烧时的焰色需要透过___________ 。
(2)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___________ ;反应化学方程式为___________ 。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打能治疗胃酸过多,请写出其反应的离子方程式___________ ;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含氢氧化铝的胃药(如胃舒平),反应的离子方程式为___________ 。
(1)焰色反应的实验中,Na元素燃烧时的焰色为
(2)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打能治疗胃酸过多,请写出其反应的离子方程式
更新时间:2021-10-18 21:47:02
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】根据所学知识,回答下列问题:
(1)用铂丝蘸取下列物质灼烧,焰色为紫色的是___________ (填序号)
a.NaCl b. c.
c.
(2)同温同压下,同体积的 和
和 气体中原子的个数比为
气体中原子的个数比为___________ 。
(3)将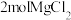 溶于水配制成1L溶液。溶液中
溶于水配制成1L溶液。溶液中 的物质的量浓度为
的物质的量浓度为___________ ;
(4) 的结构式为
的结构式为___________ 。
(1)用铂丝蘸取下列物质灼烧,焰色为紫色的是
a.NaCl b.
 c.
c.
(2)同温同压下,同体积的
 和
和 气体中原子的个数比为
气体中原子的个数比为(3)将
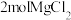 溶于水配制成1L溶液。溶液中
溶于水配制成1L溶液。溶液中 的物质的量浓度为
的物质的量浓度为(4)
 的结构式为
的结构式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】金属及其化合物在工业生产和生活中有重要用途,根据所学知识回答下列问题。
(1)将绿豆大的钠投入到水和煤油的混合体系中,观察到的现象是___________ 。
(2)CO和H2的混合气体10.0g,与足量的O2反应后,通过足量Na2O2,写出通过Na2O2时发生的化学方程式___________ 、___________ ,固体Na2O2质量增加___________ g。
(3)有一杯澄清溶液,可能含有的离子有Ca2+、Cu2+、Mg2+、K+、CO ,检验该溶液中阳离子的操作方法是
,检验该溶液中阳离子的操作方法是___________ 。
(1)将绿豆大的钠投入到水和煤油的混合体系中,观察到的现象是
(2)CO和H2的混合气体10.0g,与足量的O2反应后,通过足量Na2O2,写出通过Na2O2时发生的化学方程式
(3)有一杯澄清溶液,可能含有的离子有Ca2+、Cu2+、Mg2+、K+、CO
 ,检验该溶液中阳离子的操作方法是
,检验该溶液中阳离子的操作方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有一混合溶液,只可能含有以下离子中的若干种:H+、Na+、K+、Cl-、Ca2+、CO 、SO
、SO 取少量该混合溶液进行如下实验。
取少量该混合溶液进行如下实验。
实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有_______ (填离子符号,下同),做焰色试验前,铂丝需用_______ 清洗并灼烧至与原来的火焰颜色相同时为止。
(2)由实验②③推断该混合溶液中一定含有_______ ,一定不含有_______ 。请写出实验③中反应的离子方程式:_______ 。
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:_______ (填“是”或“否”)。若“是”本空无需作答,若“否”请写出检验该混合溶液中Cl-的实验操作及现象:_______
 、SO
、SO 取少量该混合溶液进行如下实验。
取少量该混合溶液进行如下实验。实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,火焰为黄色;
实验②:向混合溶液中加入足量BaCl2溶液后,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解,产生气泡;
实验④:向②过滤后的溶液加入硝酸银,产生白色沉淀。
根据上述实验,回答以下问题。
(1)由实验①推断该混合溶液中一定含有
(2)由实验②③推断该混合溶液中一定含有
(3)综合上述实验,是否能确定该混合溶液中含有Cl-:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学是一门以实验为基础的学科,根据图回答问题。

(1)仪器a的名称是_______ 。
(2)实验室用高锰酸钾制氧气的化学方程式为_______ ,应选用的发生装置为_______ (填序号),若用C装置收集氧气,需待_______ 再开始收集,否则收集到的气体不纯。
(3)小明用大理石和稀盐酸制备并验证二氧化碳的性质,当看到G装置中出现_______ 的现象,说明二氧化碳能与水反应。
(4)小红认为小明的实验需控制好稀盐酸的浓度,防止制得的二氧化碳中混有HCl气体,因此提议先将制得的气体通过F装置以除去氯化氢气体,则气体应从_______ (填“m”或“n”)端通入,发生反应的化学方程式为_______ 。

(1)仪器a的名称是
(2)实验室用高锰酸钾制氧气的化学方程式为
(3)小明用大理石和稀盐酸制备并验证二氧化碳的性质,当看到G装置中出现
(4)小红认为小明的实验需控制好稀盐酸的浓度,防止制得的二氧化碳中混有HCl气体,因此提议先将制得的气体通过F装置以除去氯化氢气体,则气体应从
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学在药物的开发、合成和使用中起着至关重要的作用。
(1)下面是一种常见药品说明书的部分内容,请将其补充完整。
【药品名称】碳酸氢钠。
【其他名称】重碳酸钠、酸性碳酸钠、____ 。
【功效主治】适用于胃酸过多、消化不良及碱化尿液等;静脉给药用于酸中毒;外用滴耳软化耵聍。
【不良反应】对胃溃疡的病人,中和胃酸时产生的气体会刺激溃疡面,甚至有胃穿孔的危险。其中的化学原理(用离子方程式表示)是____ 。
(2)胃舒平(复方氢氧化铝)也可以治疗胃酸过多,所依据的反应原理(用离子方程式表示)是____ 。
(3)氢氧化铝跟氢氧化钠溶液反应的离子方程式是____ 。
(4)根据金属钠的性质填空
金属钠切开后,光亮的金属断面____ ,说明常温下钠能够跟____ 反应,生成____ ;钠投入水中,钠____ 水面上,并四处游动,发出响声,这说明____ ,熔成一个闪亮的小球,说明____ ,最后向烧杯中滴加酚酞,溶液变____ ,反应的化学方程式为:____ 。
(5)用金属钠制取过氧化钠的化学方程式____ ,现象是____ 。
(1)下面是一种常见药品说明书的部分内容,请将其补充完整。
【药品名称】碳酸氢钠。
【其他名称】重碳酸钠、酸性碳酸钠、
【功效主治】适用于胃酸过多、消化不良及碱化尿液等;静脉给药用于酸中毒;外用滴耳软化耵聍。
【不良反应】对胃溃疡的病人,中和胃酸时产生的气体会刺激溃疡面,甚至有胃穿孔的危险。其中的化学原理(用离子方程式表示)是
(2)胃舒平(复方氢氧化铝)也可以治疗胃酸过多,所依据的反应原理(用离子方程式表示)是
(3)氢氧化铝跟氢氧化钠溶液反应的离子方程式是
(4)根据金属钠的性质填空
金属钠切开后,光亮的金属断面
(5)用金属钠制取过氧化钠的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】Na2CO3和NaHCO3都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)Na2CO3俗称____ ,往Na2CO3溶液中滴加酚酞,溶液呈____ 色。
(2)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈___ 色。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:_____ 。
(4)除去Na2CO3粉末中混有的少量NaHCO3的方法是____ ,化学方程式为____ 。
(1)Na2CO3俗称
(2)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:
(4)除去Na2CO3粉末中混有的少量NaHCO3的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】Ⅰ.从A组中选择一种最适宜 的试剂(每种试剂只能选用一次),以除去B组物质的少量杂质(括号内为杂质),将正确答案的序号 填入短线上。
A组:①稀盐酸 ②澄清石灰水 ③CO2 ④Cl2溶液 ⑤NaOH溶液 ⑥Fe屑
B组:(1)NaCl溶液中(Na2CO3)_____________ ;
(2)NaHCO3溶液(Na2CO3)_____________ 。
(3)镁粉(铝粉)_____________ ;
(4)FeCl2溶液(FeCl3)_____________ 。
Ⅱ.元素及其化合物在生产和生活中有广泛的用途。请按要求填写:
(1)碳酸氢钠可作发酵粉的原理(用化学方程式表示)______________________ 。
(2)胃舒平(复方氢氧化铝)治疗胃酸过多的原理(用离子方程式表示)_______ 。
(3)用氢氟酸刻蚀玻璃的原理(用化学方程式表示)______________________ 。
(4)硫酸亚铁缓释片可以补铁,治贫血,在酸性环境下很容易变质的原因(用离子方程式表示)_______________________________________ 。
A组:①稀盐酸 ②澄清石灰水 ③CO2 ④Cl2溶液 ⑤NaOH溶液 ⑥Fe屑
B组:(1)NaCl溶液中(Na2CO3)
(2)NaHCO3溶液(Na2CO3)
(3)镁粉(铝粉)
(4)FeCl2溶液(FeCl3)
Ⅱ.元素及其化合物在生产和生活中有广泛的用途。请按要求填写:
(1)碳酸氢钠可作发酵粉的原理(用化学方程式表示)
(2)胃舒平(复方氢氧化铝)治疗胃酸过多的原理(用离子方程式表示)
(3)用氢氟酸刻蚀玻璃的原理(用化学方程式表示)
(4)硫酸亚铁缓释片可以补铁,治贫血,在酸性环境下很容易变质的原因(用离子方程式表示)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】复方氢氧化铝治疗胃酸过多时,氢氧化铝作为_________ 中和过多胃酸;氢氧化铝也能跟烧碱溶液反应,反应的离子方程式为________________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】写出相关的反应方程式:
(1)由可溶性铝盐制取氢氧化铝,需加入的试剂为:________ ;反应方程式为:_____________ 。
(2)白色的Fe(OH)2在空气中发生的颜色变化为___________ 。反应的化学方程式为:________ 。
(3)氯气与铁反应:_________ 。
(1)由可溶性铝盐制取氢氧化铝,需加入的试剂为:
(2)白色的Fe(OH)2在空气中发生的颜色变化为
(3)氯气与铁反应:
您最近一年使用:0次
填空题
|
较易
(0.85)
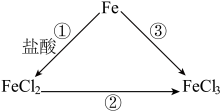
【推荐2】铁及其化合物之间的转化关系如图所示。
(1)反应①的离子方程式为_______ 。
(2)完成反应②还需加入_______ (填“氧化剂”或“还原剂”)。
(3)完成反应③还需用到的试剂为_______ (填化学式),检验 的试剂为
的试剂为_______ 。
(4)向 溶液中加入
溶液中加入 溶液的现象为
溶液的现象为_______ 。
(1)反应①的离子方程式为
(2)完成反应②还需加入
(3)完成反应③还需用到的试剂为
 的试剂为
的试剂为(4)向
 溶液中加入
溶液中加入 溶液的现象为
溶液的现象为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】铁是应用最广泛的金属,铁的氯化物、氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)在实验室中,FeCl2可用铁粉和___________ (填名称)反应制备。
(2)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___________ ,对应的化学方程式为___________ 。
(3)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:___________ 。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:___________ 。
(1)在实验室中,FeCl2可用铁粉和
(2)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(3)红砖是用黏土高温烧结而成的,因其含有Fe2O3呈红色或棕红色而得名,常用作建筑材料。请设计一个简单实验证明红砖中含有Fe3+:
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为:
您最近一年使用:0次



